Clear Sky Science · pl
Wsparty przez uczenie głębokie zintegrowany proces do projektowania i syntezy od podstaw peptydów przeciwbakteryjnych
Dlaczego nowe środki przeciwbakteryjne są ważne
W miarę jak powszechne antybiotyki tracą skuteczność wobec coraz bardziej opornych bakterii, lekarzom kończą się opcje leczenia codziennych infekcji. Obiecującą alternatywą są peptydy przeciwbakteryjne — krótkie fragmenty białek, które zamiast celować w pojedynczy enzym przebijają błony komórek bakteryjnych. Artykuł opisuje, jak naukowcy użyli sztucznej inteligencji (AI) do automatycznego projektowania i testowania nowych peptydów przeciwbakteryjnych w sposób szybszy, tańszy i bardziej ukierunkowany niż tradycyjne eksperymenty „metodą prób i błędów”.

Nowy sposób przeszukiwania ogromnej przestrzeni cząsteczek
Projektowanie użytecznych peptydów przeciwbakteryjnych przypomina poszukiwanie kilku zwycięskich losów na górze losowych numerów: możliwych sekwencji aminokwasów jest astronomicznie wiele, ale tylko ułamek z nich będzie bezpiecznymi i skutecznymi lekami. Konwencjonalne przesiewy w laboratorium są powolne i kosztowne, a nawet modele komputerowe często mają trudność z pogodzeniem siły działania z różnorodnością niezbędną do odkrycia naprawdę nowych cząsteczek. Autorzy rozwiązują to, budując trzyetapowy proces — generowanie, ocena i walidacja eksperymentalna — który pozwala AI eksplorować ogromne obszary przestrzeni sekwencji, jednocześnie koncentrując się na kandydatach, które wyglądają realistycznie i obiecująco.
Nauczanie modelu języka białek myślenia jak projektant peptydów
U podstaw pierwszego etapu leży ProtGPT2, duży „model języka białek” pierwotnie trenowany do pisania wiarygodnych sekwencji białkowych tak, jak modele tekstowe piszą zdania. Zamiast pełnego ponownego trenowania tego olbrzymiego modelu — podejścia kosztownego i podatnego na przeuczenie przy niewielkich zbiorach danych o peptydach — zespół zastosował strategię zwaną miękkim dopasowaniem promptu (soft prompt tuning). Dodają mały, trenowalny prompt na początku każdej sekwencji i aktualizują tylko ten prompt, pozostawiając stałe wewnętrzne wagi modelu. Takie delikatne sterowanie wystarczyło, by przesunąć model w kierunku generowania peptydów przypominających antybakteryjne, nie tracąc przy tym szerokiej kreatywności. Analizy wygenerowanych sekwencji wykazały, że odpowiadały one prawdziwym peptydom przeciwbakteryjnym pod kątem kluczowych właściwości, takich jak ładunek, hydrofobowość i wzorce strukturalne, będąc jednocześnie bardziej różnorodne niż sekwencje otrzymane przez pełne ponowne trenowanie.
Pozwalanie kilku „ekspertom” AI głosować nad każdym kandydatem
W drugim etapie badacze stają przed przeciwstawnym wyzwaniem: spośród 30 000 wygenerowanych sekwencji, które z nich zasługują na koszt syntezy chemicznej i testów laboratoryjnych? Zbudowali model oceniający o nazwie MCL‑AMP, który łączy trzy różne sieci neuronowe „ekspertów” — jednego skupiającego się na wzorcach lokalnych, drugiego śledzącego dalekosiężne relacje wzdłuż sekwencji i trzeciego integrującego cechy ogólne. Osobna sieć głosująca uczy się, ile ufać poszczególnym ekspertom dla każdego peptydu, a specjalna funkcja straty zniechęca system do nadmiernej pewności, gdy się myli. Korzystając z bogatych cech sekwencyjnych wyodrębnionych przez inny zaawansowany model białkowy (ESM‑2), to ensemble osiągnął wyższą dokładność niż istniejące narzędzia w rozróżnianiu sekwencji antybakteryjnych od nieantybakteryjnych i wygenerował interpretowalny wynik ufności dla każdego kandydata.
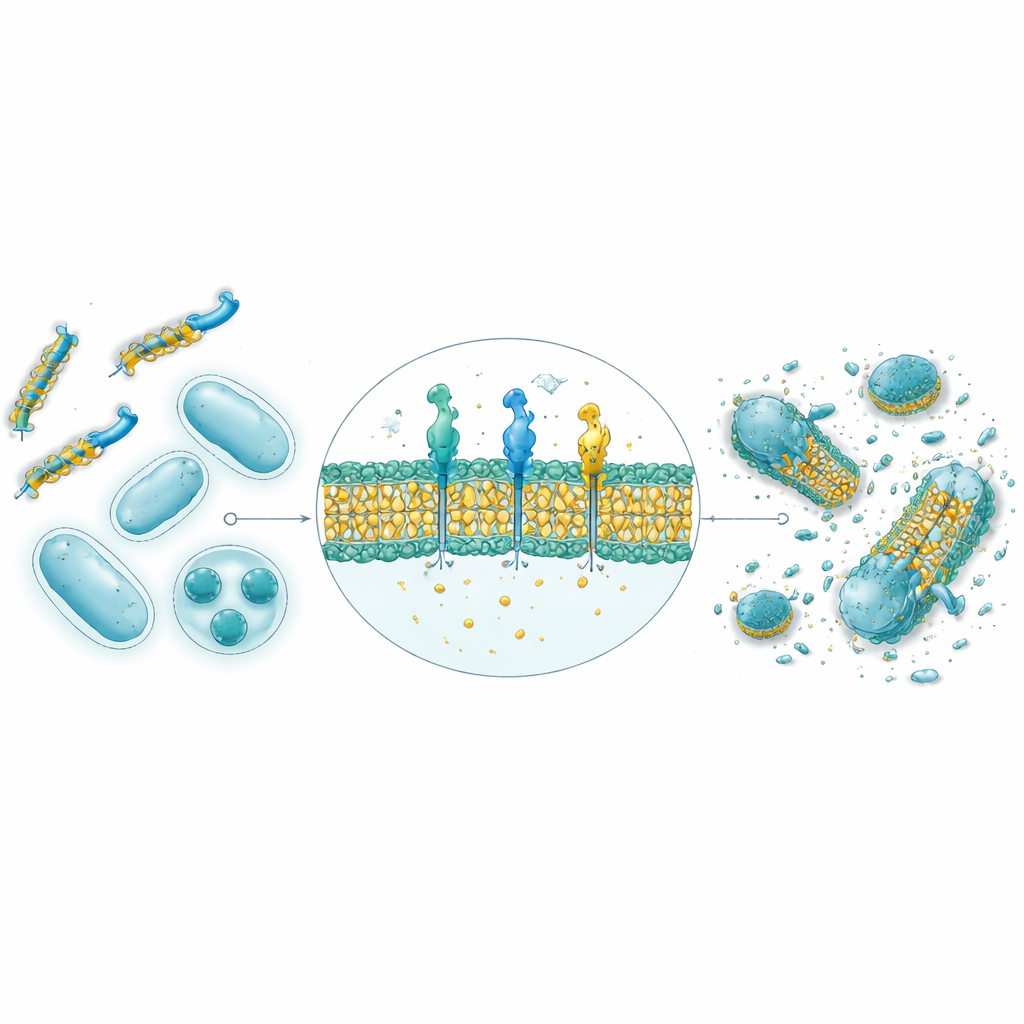
Od komputerowych przewidywań do prawdziwych bakterii w laboratorium
Spośród 30 000 sekwencji wygenerowanych przez AI, dziewięć najlepiej ocenionych peptydów zostało zsyntetyzowanych i przetestowanych przeciwko czterem szczepom bakterii, obejmującym gatunki Gram‑dodatnie i Gram‑ujemne. Przewidywania strukturalne z użyciem AlphaFold sugerowały, że osiem z dziewięciu przyjmuje amfipatyczne helikalne kształty typowe dla naturalnych peptydów przeciwbakteryjnych, z oddzielnymi ścianami hydrofilowymi i hydrofobowymi sprzyjającymi atakowi błony. W testach na płytkach Petriego cztery z dziewięciu wykazały silną aktywność antybakteryjną, a dwa z nich — nazwane GW20 i KI16 — zbliżyły się do skuteczności ustalonych antybiotyków w hamowaniu wzrostu bakterii. Mikroskopia ujawniła widoczne uszkodzenia powierzchni komórek bakteryjnych wywołane przez te peptydy, zgodne z mechanizmem uszkadzania błony. Co ważne, oba wykazały minimalne uszkodzenie czerwonych krwinek w terapeutycznie istotnych stężeniach i silną zdolność zapobiegania oraz rozbijania lepkich biofilmów bakteryjnych, często przewyższając standardowy antybiotyk.
Co to oznacza dla przyszłych leków
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że autorzy zbudowali działającą pętlę „projektuj–testuj”, w której AI proponuje wiele nowych peptydów zabijających zarazki, sortuje je za pomocą komitetu modeli, a następnie potwierdza trafienia w laboratorium. Chociaż nie każda wysoko oceniona sekwencja zadziałała, odsetek trafień — cztery aktywne peptydy na dziewięć przetestowanych — jest znacznie wyższy niż w tradycyjnym, ślepym przesiewie. Dwa najbardziej obiecujące związki już wykazują użyteczne połączenie siły działania, bezpieczeństwa i zdolności zwalczania biofilmów, co zapowiada przyszłe terapie opornych infekcji. Równo ważne jest to, że ta modułowa linia procesowa może zostać ponownie dopasowana do projektowania innych peptydów medycznych, na przykład ukierunkowanych na nowotwory lub wirusy, oferując elastyczny wzorzec dla przyspieszonego przez AI odkrywania leków w obliczu rosnącej oporności na antybiotyki.
Cytowanie: Liu, J., Chen, Y., Tang, J. et al. Deep learning-driven integrated pipeline for de novo design and synthesis of antimicrobial peptides. npj Drug Discov. 3, 15 (2026). https://doi.org/10.1038/s44386-026-00045-6
Słowa kluczowe: peptydy przeciwbakteryjne, sztuczna inteligencja, odkrywanie leków, oporność na antybiotyki, biofilmy