Clear Sky Science · ja
抗菌ペプチドのde novo設計と合成のための深層学習駆動統合パイプライン
なぜ新しい抗菌分子が重要なのか
従来の抗生物質がより強靭な細菌に対して効力を失いつつある中、日常的な感染症の治療選択肢が減少しています。有望な代替手段の一つが抗菌ペプチドです―これは単一の酵素を標的にするのではなく、細菌膜に穴を開ける短いタンパク質断片です。本稿は、研究者たちが人工知能(AI)を利用して、新しい抗菌ペプチドを従来の試行錯誤よりも速く、安価に、かつ標的化して設計・試験した方法を説明します。

膨大な分子空間を探る新たな方法
有用な抗菌ペプチドを設計することは、ランダムな数字の山の中から当たりくじを探すようなものです:アミノ酸配列の組み合わせは天文学的に多い一方で、安全で有効な薬になるものはごく一部にすぎません。従来の実験室でのスクリーニングは遅く高価で、コンピュータモデルであっても効力と新規性を見つけるために必要な多様性の両立に苦しむことがよくあります。著者らはこれに対して、生成・評価・実験検証の三段階パイプラインを構築し、AIが配列空間の広い領域を探索しつつ、現実的で有望に見える候補に収束できるようにしました。
ペプチド設計者の思考を学ばせるタンパク質言語モデル
第一段階の中心にはProtGPT2という大型の「タンパク質言語モデル」があります。これはテキストモデルが文章を書くようにもっともらしいタンパク質配列を書くように訓練されたものです。この巨大モデルを完全に再訓練することはコストが高く、抗菌データが少ない場合には過学習しやすいため、チームはソフトプロンプトチューニングと呼ばれる戦略を採りました。各配列の前に小さな訓練可能な入力プロンプトを付け、そのプロンプトだけを更新しモデルの内部重みは固定します。この穏やかな誘導によって、モデルは広い創造性を保ちながら抗菌様のペプチドを生成する方向へ十分にシフトしました。生成配列の解析では、電荷、疎水性、構造パターンなど主要な性質が実在の抗菌ペプチドと一致し、完全再訓練で得られる配列よりも多様性が高いことが示されました。
複数のAI「専門家」による候補の投票
第二段階では逆の課題が立ちはだかります:30,000個の生成配列のうち、どれを化学合成と実験検査に回す価値があるか?著者らはMCL‑AMPと呼ばれる評価モデルを構築しました。これは局所的パターンに注目するネットワーク、配列に沿った長距離関係を追うネットワーク、全体的特徴を統合するネットワークという三つのニューラルネットワーク「専門家」を組み合わせます。別の投票ネットワークが各ペプチドに対してどの専門家をどれだけ信頼するかを学習し、誤りの際に過度な自信を避ける特殊な損失関数も導入されました。別の高度なタンパク質モデル(ESM‑2)によって抽出された豊富な配列特徴を用いることで、このアンサンブルは既存ツールより抗菌/非抗菌配列の識別精度が高く、各候補に対して解釈可能な信頼度スコアを出しました。
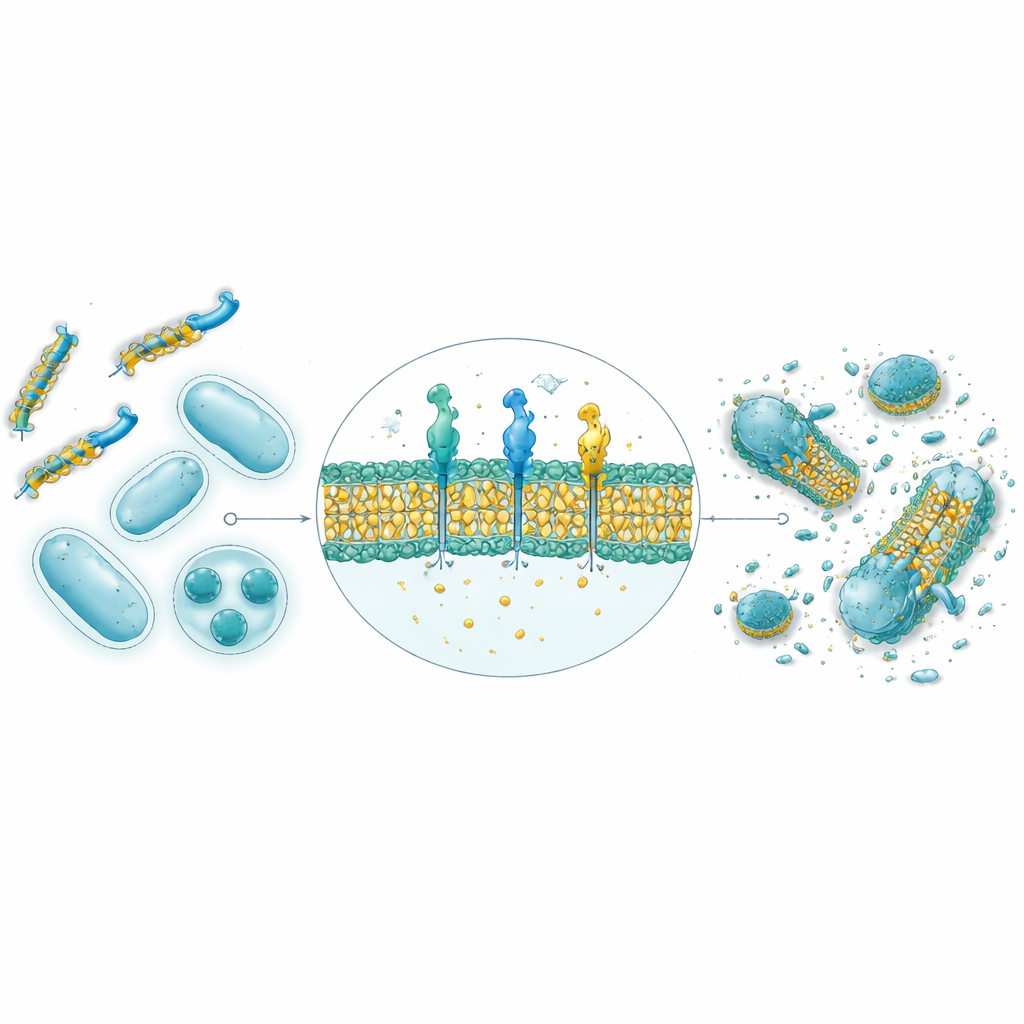
コンピュータ予測から実験室での細菌検証へ
30,000件のAI生成配列から上位9配列が合成され、グラム陽性・陰性を含む4種類の細菌株に対して試験されました。AlphaFoldによる構造予測は、9配列中8配列が天然の抗菌ペプチドに典型的な両親媒性ヘリックス形状をとることを示唆し、水を好む面と油を好む面が膜攻撃に適することが示されました。ペトリ皿試験では9配列中4配列が強い抗菌活性を示し、とりわけGW20とKI16という2配列は細菌増殖抑制の点で既存抗生物質に近い性能を示しました。顕微鏡観察ではこれらペプチドが細菌表面を明らかに破壊しており、膜破壊という作用機序と整合します。重要な点として、両者とも治療濃度で赤血球へのダメージは最小限であり、粘着性のある細菌バイオフィルムの予防・分解能力に優れ、しばしば標準的な抗生物質を上回りました。
将来の医薬品に向けての意味
非専門家向けの要点は、著者らがAIが多数の新規殺菌ペプチドを提案し、モデル委員会で選別し、実験でヒットを確認する「設計—検証」ループを実際に構築したことです。上位全てが機能したわけではありませんが、ヒット率(9試験中4活性)は従来の盲目的なスクリーニングよりずっと高いです。最も有望な2分子は既に効力、安全性、バイオフィルム抑制という有用な特性の組み合わせを示しており、頑固な感染症に対する将来の治療薬の可能性を示唆します。同様に重要なのは、このモジュール式パイプラインをがん標的や抗ウイルス分子など他の医療用ペプチド設計に再調整できる点であり、抗菌薬耐性の進行に対抗するためのAI加速型創薬の柔軟な設計図を提供することです。
引用: Liu, J., Chen, Y., Tang, J. et al. Deep learning-driven integrated pipeline for de novo design and synthesis of antimicrobial peptides. npj Drug Discov. 3, 15 (2026). https://doi.org/10.1038/s44386-026-00045-6
キーワード: 抗菌ペプチド, 人工知能, 創薬, 抗生物質耐性, バイオフィルム