Clear Sky Science · he
צינור משולב מונחה למידה עמוקה לתכנון וסינתזה דה־נובו של פפטידים אנטי־מיקרוביאליים
מדוע מולקולות חדשות נגד זיהומים חשובות
כשאנטיביוטיקה שכיחה מאבדת יעילותה מול חיידקים עמידים יותר ויותר, לרופאים נשארות פחות אפשרויות לטפל בזיהומים יומיומיים. אלטרנטיבה מבטיחה היא פפטידים אנטי‑מיקרוביאליים — חלקי חלבון קצרים שמייצרים חורים בקרומי החיידק במקום לכוון לאנזים יחיד. מאמר זה מתאר כיצד חוקרים השתמשו בבינה מלאכותית (AI) כדי לתכנן ולבחון באופן אוטומטי פפטידים אנטי‑מיקרוביאליים חדשים, במהירות ובעלות נמוכה יותר ובהתמקדות גבוהה יותר מאשר ניסויים מסורתיים של ניסוי וטעייה.

דרך חדשה לחיפוש במרחב העצום של מולקולות
תכנון פפטידים אנטי‑מיקרוביאליים שימושיים דומה לחיפוש כמה כרטיסי לוטו זוכים בתוך הררי מספרים אקראיים: קיימים מספרים אסטרונומיים של רצפי חומצות אמינו אפשריים, אך רק שבריר מהם יהיו תרופות בטוחות ויעילות. סריקות מעבדה קונבנציונליות איטיות ויקרות, ואף מודלים ממוחשבים לעיתים מתקשים לאזן בין עוצמה לגיוון הנדרש לחשוף מולקולות חדשות באמת. החוקרים מתמודדים עם זאת על‑ידי בניית צינור עבודה בשלושה שלבים — יצירה, הערכה ואימות ניסויי — שמאפשר ל‑AI לחקור אזורים עצומים במרחב הרצפים ובאותו זמן להתמקד במועמדים שנראים מציאותיים ומבטיחים.
ללמד מודל שפת חלבון לחשוב כמו מתכנן פפטידים
בליבת השלב הראשון עומד ProtGPT2, "מודל שפת חלבון" גדול שאומן במקור לכתוב רצפי חלבון סבירים באותו אופן שמודלי טקסט כותבים משפטים. במקום לאמן מחדש את המודל הענק הזה במלואו — גישה יקרה וחשופה לבעיית התאמה יתר לסטי נתונים קטנים של אנטימיקרוביאלים — הצוות משתמש באסטרטגיה שנקראת כיוון רך של פרומפט. הם מצרפים פרומפט קלט קטן שניתן לאימון לפני כל רצף ומעדכנים רק את הפרומפט הזה בעוד שמשקלות המודל נשארות קבועות. ההכוונה העדינה הזו הוכיחה עצמה כהסעה מספקת להטות את המודל לייצור פפטידים בסגנון אנטי‑מיקרוביאלי מבלי לפגוע ביצירתיות הרחבה שלו. ניתוחים של הרצפים שנוצרו הראו שהם התאימו לפפטידים אנטי‑מיקרוביאליים אמיתיים בתכונות מרכזיות כמו מטען, הידרופוביות ודפוסים מבניים, ובאותו זמן נשארו מגוונים יותר מרצפים שנוצרו על ידי אימון מלא.
לאפשר "הצבעת" של מספר "מומחי" AI על כל מועמד
בשלב השני החוקרים ניצבים באתגר ההפוך: מתוך 30,000 רצפים שנוצרו, אילו מהם מצדיקים את עלות הסינתזה הכימית והבדיקות במעבדה? הם בונים מודל הערכה בשם MCL‑AMP המשלב שלושה "מומחי" רשתות עצביות שונים — אחד המתמקד בדפוסים מקומיים, אחד שעוקב אחר יחסים לטווח ארוך לאורך הרצף, ואחד המשלב תכונות כלליות. רשת הצבעה נפרדת לומדת כמה לסמוך על כל מומחה עבור כל פפטיד, ופונקציית אובדן מיוחדת מרתיעה את המערכת מלנהוג בבטחון־יתר כשהיא טועה. באמצעות תכונות רצף עשירות המופקות על ידי מודל חלבון מתקדם נוסף (ESM‑2), האנסמבל הזה השיג דיוק גבוה יותר מאשר כלים קיימים בהבחנה בין רצפים אנטי‑מיקרוביאליים ללא‑אנטי‑מיקרוביאליים, והוא הפיק ציון אמינות מובן לכל מועמד.
מנבאים ממחשב לחיידקים אמיתיים במעבדה
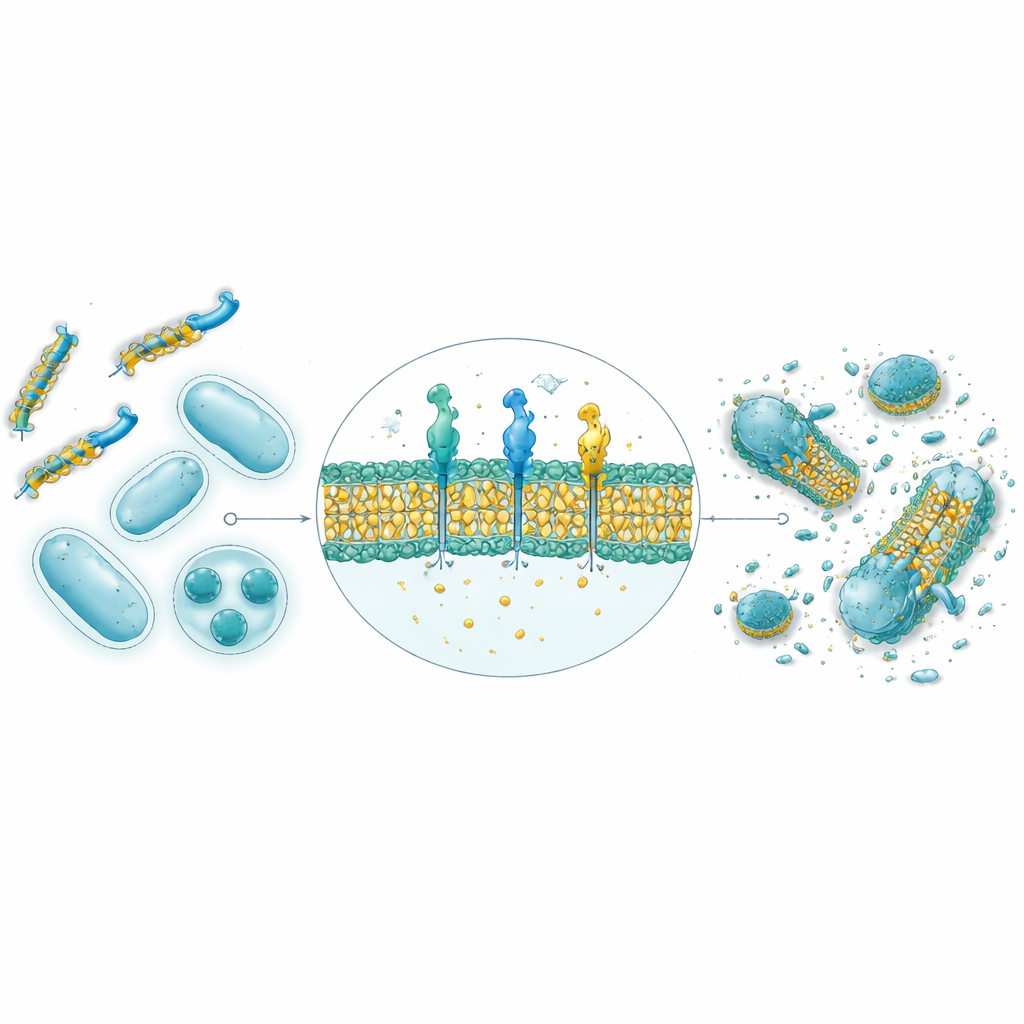
מתוך 30,000 הרצפים שנוצרו על‑ידי ה‑AI, תשעה הפפטידים בעלי הציון הגבוה ביותר סונתו וסונתזו ונבדקו מול ארבעה זנים חיידקיים, כולל מינים גרם‑חיוביים וגרם‑שליליים. תחזיות מבניות בעזרת AlphaFold הצביעו על כך ששמונה מתוך תשעתם מאמצים צורות הליקליות אמפיפתיות אופייניות לפפטידים אנטי‑מיקרוביאליים טבעיים, עם פנים הידרופיליות ופנים הידרופוביות המעדיפות מתקפת ממברנה. בבדיקות בפטרי‑דיש, ארבעה מתוך תשעתם הראו פעילות אנטיבקטריאלית חזקה, ושניים במיוחד — שנקראו GW20 ו‑KI16 — התקרבו לביצועי אנטיביוטיקות מבוססות בעיכוב צמיחת חיידקים. מיקרוסקופיה גילתה שהפפטידים האלה פגעו באופן ניכר במשטחי תאי החיידק, בהתאם למנגנון של פגיעה בממברנה. מה שחשוב — שניהם הראו נזק מינימלי לתאי דם אדומים בריכוזים טיפוליים והפגינו יכולת חזקה למנוע ולפרק ביופילמים דביקים של חיידקים, שלעיתים אף עלו על אנטיביוטיקה סטנדרטית.
מה המשמעות של זה עבור תרופות בעתיד
עבור הקוראים שאינם מומחים, המסר המרכזי הוא שהסופרים בנו לולאת "תכנון‑בדיקה" עובדת שבה ה‑AI מציע שפע של פפטידים חדשים שמורידים זיהומים, מסווג אותם באמצעות ועדת מודלים, ואז מאמת מכות עבודה במעבדה. אף על פי שלא כל רצף מדורג גבוה עבד, שיעור ההצלחה — ארבעה פפטידים פעילים מתוך תשעה שנבדקו — גבוה בהרבה מהסריקה העיוורת המסורתית. שני המולקולות המבטיחות ביותר כבר מציגות שילוב שימושי של עוצמה, בטיחות ויכולת להילחם בביופילם, ורומזות על טיפולים עתידיים לזיהומים עקשניים. לא פחות חשוב, הצינור המודולרי הזה יכול להיות מכוּון מחדש כדי לתכנן פפטידים רפואיים אחרים, כגון סוכנים המכוונים לסרטן או מולקולות אנטי‑ויראליות, ומציע מתווה גמיש לגילוי תרופות מתוגבר ב‑AI לנוכח עליית העמידות האנטימיקרוביאלית.
ציטוט: Liu, J., Chen, Y., Tang, J. et al. Deep learning-driven integrated pipeline for de novo design and synthesis of antimicrobial peptides. npj Drug Discov. 3, 15 (2026). https://doi.org/10.1038/s44386-026-00045-6
מילות מפתח: פפטידים אנטי־מיקרוביאליים, בינה מלאכותית, גילוי תרופות, עמידות אנטיביוטית, ביופילם