Clear Sky Science · pt
Pipeline integrada orientada por deep learning para o projeto de novo e síntese de peptídeos antimicrobianos
Por que novas moléculas antimicrobianas importam
À medida que antibióticos comuns perdem eficácia contra bactérias cada vez mais resistentes, os médicos ficam com menos opções para tratar infecções do dia a dia. Uma alternativa promissora são os peptídeos antimicrobianos—curtos fragmentos proteicos que perfuram membranas bacterianas em vez de mirar um único enzima. Este artigo descreve como pesquisadores usaram inteligência artificial (IA) para projetar e testar automaticamente novos peptídeos antimicrobianos de maneira mais rápida, mais barata e mais direcionada do que experimentos tradicionais por tentativa e erro.

Uma nova forma de vasculhar o vasto espaço molecular
Projetar peptídeos antimicrobianos úteis é como procurar alguns bilhetes premiados numa montanha de números aleatórios: existem astronomicamente muitas sequências possíveis de aminoácidos, mas apenas uma fração ínfima será segura e eficaz como fármaco. Triagens convencionais em laboratório são lentas e caras, e mesmo modelos computacionais frequentemente têm dificuldade em equilibrar potência com a diversidade necessária para descobrir moléculas genuinamente novas. Os autores enfrentam isso construindo um pipeline em três etapas—geração, avaliação e validação experimental—que permite à IA explorar enormes regiões do espaço de sequências enquanto ainda foca em candidatos que parecem realistas e promissores.
Ensinar um modelo de linguagem proteica a pensar como um projetista de peptídeos
No cerne da primeira etapa está o ProtGPT2, um grande “modelo de linguagem proteica” originalmente treinado para escrever sequências de proteínas plausíveis da mesma forma que modelos de texto escrevem frases. Em vez de retreinar completamente esse modelo massivo—uma abordagem custosa e sujeita a overfitting em conjuntos de dados pequenos de antimicrobianos—a equipe usa uma estratégia chamada soft prompt tuning. Eles acoplam um pequeno prompt de entrada treinável na frente de cada sequência e atualizam apenas esse prompt mantendo os pesos internos do modelo fixos. Esse direcionamento suave foi suficiente para deslocar o modelo para gerar peptídeos com características antimicrobianas sem sacrificar sua criatividade ampla. Análises das sequências geradas mostraram que elas correspondiam a peptídeos antimicrobianos reais em propriedades-chave como carga, hidrofobicidade e padrões estruturais, ao mesmo tempo em que permaneciam mais diversas do que sequências produzidas por retreinamento completo.
Deixar múltiplos “peritos” de IA votarem em cada candidato
Na segunda etapa, os pesquisadores enfrentam o desafio oposto: entre 30.000 sequências geradas, quais merecem o custo de síntese química e testes em laboratório? Eles construíram um modelo de avaliação chamado MCL‑AMP que combina três “peritos” diferentes em redes neurais—um que foca em padrões locais, outro que acompanha relações de longo alcance ao longo da sequência e um que integra características gerais. Uma rede de votação separada aprende quanto confiar em cada perito para cada peptídeo, e uma função de perda especial desencoraja o sistema de ficar excessivamente confiante quando está errado. Usando recursos de sequência ricos extraídos por outro modelo proteico avançado (ESM‑2), esse conjunto alcançou maior precisão do que ferramentas existentes ao distinguir sequências antimicrobianas de não antimicrobianas, e gerou uma pontuação de confiança interpretável para cada candidato.
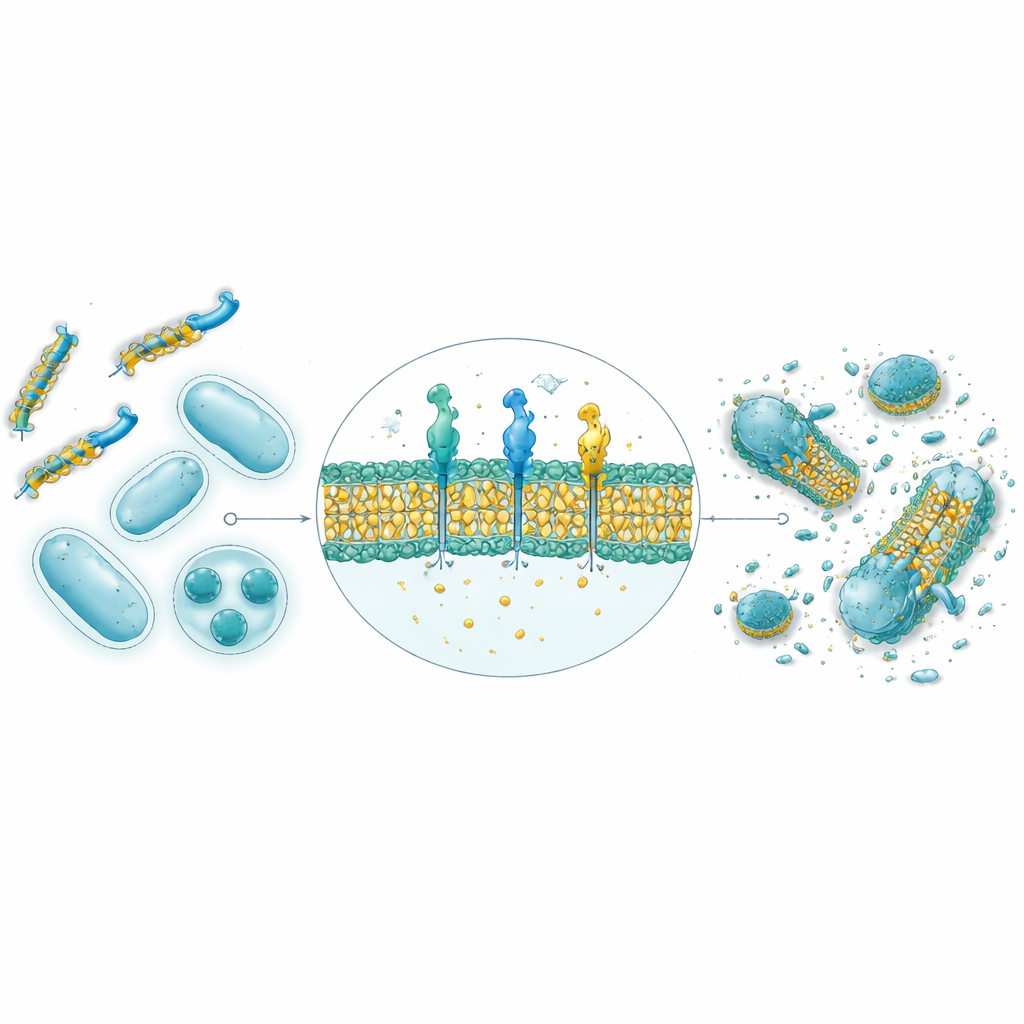
Das previsões computacionais para bactérias reais no laboratório
Das 30.000 sequências geradas pela IA, os nove peptídeos com as maiores pontuações foram sintetizados e testados contra quatro cepas bacterianas, incluindo espécies Gram‑positivas e Gram‑negativas. Predições estruturais usando AlphaFold sugeriram que oito dos nove adotam formas helicoidais anfipáticas típicas de peptídeos antimicrobianos naturais, com faces separadas que gostam de água e de gordura favorecendo o ataque à membrana. Em testes em placas de Petri, quatro dos nove mostraram forte atividade antibacteriana, e dois em particular—batizados de GW20 e KI16—atingiram desempenho próximo ao de antibióticos estabelecidos em inibir o crescimento bacteriano. Microscopia revelou que esses peptídeos danificaram visivelmente as superfícies das células bacterianas, consistente com um mecanismo de ruptura de membrana. Importante, ambos apresentaram dano mínimo às hemácias em concentrações terapeuticamente relevantes e demonstraram grande capacidade de prevenir e degradar biofilmes bacterianos pegajosos, muitas vezes superando um antibiótico padrão.
O que isso significa para medicamentos futuros
Para não especialistas, a mensagem chave é que os autores construíram um ciclo funcional de “projeto–teste” no qual a IA propõe muitos novos peptídeos que matam germes, triagem-os com um comitê de modelos e então confirma acertos no laboratório. Embora nem toda sequência mais bem ranqueada tenha funcionado, a taxa de acerto—quatro peptídeos ativos entre nove testados—é muito maior do que a triagem cega tradicional. As duas moléculas mais promissoras já exibem uma combinação útil de potência, segurança e capacidade de combater biofilmes, sugerindo futuras terapias para infecções persistentes. Tão importante quanto, o mesmo pipeline modular pode ser reconfigurado para projetar outros peptídeos médicos, como agentes direcionados ao câncer ou moléculas antivirais, oferecendo um plano flexível para a descoberta de fármacos acelerada por IA diante do aumento da resistência antimicrobiana.
Citação: Liu, J., Chen, Y., Tang, J. et al. Deep learning-driven integrated pipeline for de novo design and synthesis of antimicrobial peptides. npj Drug Discov. 3, 15 (2026). https://doi.org/10.1038/s44386-026-00045-6
Palavras-chave: peptídeos antimicrobianos, inteligência artificial, descoberta de fármacos, resistência a antibióticos, biofilmes