Clear Sky Science · it
Pipeline integrata guidata dal deep learning per il design de novo e la sintesi di peptidi antimicrobici
Perché servono nuove molecole contro i microrganismi
Con gli antibiotici comuni che perdono efficacia contro batteri sempre più resistenti, i medici stanno esaurendo le opzioni per trattare infezioni di tutti i giorni. Un’alternativa promettente sono i peptidi antimicrobici — brevi frammenti proteici che forano le membrane batteriche anziché mirare a un singolo enzima. Questo articolo descrive come i ricercatori hanno utilizzato l’intelligenza artificiale (IA) per progettare e testare automaticamente nuovi peptidi antimicrobici in modo più rapido, economico e mirato rispetto agli esperimenti tradizionali basati sul tentativo ed errore.

Un nuovo modo di esplorare l’immenso spazio delle molecole
Progettare peptidi antimicrobici utili è come cercare pochi biglietti vincenti in una montagna di numeri casuali: esistono un numero astronomico di possibili sequenze di amminoacidi, ma solo una frazione minuscola sarà sicura ed efficace come farmaco. Lo screening di laboratorio convenzionale è lento e costoso, e anche i modelli al computer spesso faticano a bilanciare potenza e la diversità necessaria per scoprire molecole davvero nuove. Gli autori affrontano questo problema costruendo una pipeline in tre fasi — generazione, valutazione e validazione sperimentale — che permette all’IA di esplorare ampie regioni dello spazio delle sequenze pur concentrandosi su candidati che appaiono realistici e promettenti.
Insegnare a un modello linguistico proteico a pensare come un progettista di peptidi
Al centro della prima fase c’è ProtGPT2, un grande “modello linguistico per proteine” originariamente addestrato a scrivere sequenze proteiche plausibili come i modelli di testo scrivono frasi. Invece di riaddestrare completamente questo enorme modello — un approccio costoso e soggetto a overfitting su piccoli dataset antimicrobici — il team utilizza una strategia chiamata soft prompt tuning. Inseriscono un piccolo prompt di input addestrabile davanti a ogni sequenza e aggiornano solo questo prompt mantenendo fissi i pesi interni del modello. Questa guida delicata si è rivelata sufficiente a indirizzare il modello verso la generazione di peptidi di tipo antimicrobico senza sacrificare la sua ampia creatività. Le analisi delle sequenze generate hanno mostrato che corrispondevano ai peptidi antimicrobici reali in proprietà chiave come carica, idrofobicità e schemi strutturali, pur restando più diversificate rispetto alle sequenze prodotte da un riaddestramento completo.
Lasciare che più “esperti” IA votino su ogni candidato
Nella seconda fase i ricercatori affrontano la sfida opposta: tra 30.000 sequenze generate, quali meritano il costo della sintesi chimica e dei test di laboratorio? Hanno costruito un modello di valutazione chiamato MCL‑AMP che combina tre diversi “esperti” basati su reti neurali — uno focalizzato su pattern locali, uno che traccia relazioni a lungo raggio lungo la sequenza e uno che integra caratteristiche globali. Una rete di voto separata impara quanto fidarsi di ciascun esperto per ogni peptide, e una funzione di perdita speciale scoraggia il sistema dall’essere troppo sicuro quando sbaglia. Utilizzando ricche caratteristiche di sequenza estratte da un altro avanzato modello proteico (ESM‑2), questo ensemble ha raggiunto una precisione superiore rispetto agli strumenti esistenti nel distinguere sequenze antimicrobiche da non antimicrobiche, producendo inoltre un punteggio di confidenza interpretabile per ogni candidato.
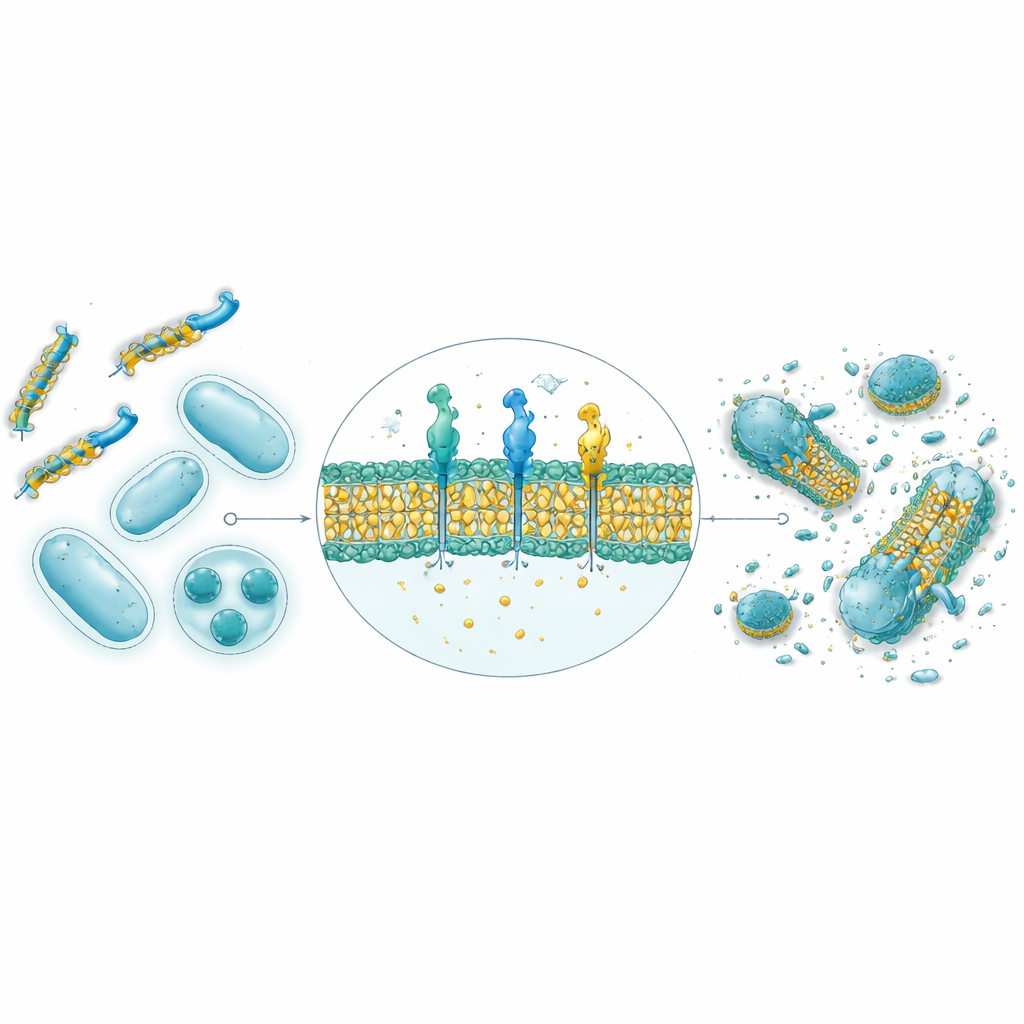
Dalle previsioni al computer ai batteri veri in laboratorio
Delle 30.000 sequenze generate dall’IA, i nove peptidi con i punteggi più alti sono stati sintetizzati e testati contro quattro ceppi batterici, incluse specie Gram‑positive e Gram‑negative. Le predizioni strutturali con AlphaFold hanno suggerito che otto dei nove adottano le forme elicoidali anfipatiche tipiche dei peptidi antimicrobici naturali, con facce separate idrofile e idrofobe che favoriscono l’attacco alla membrana. Nei test in piastra, quattro dei nove hanno mostrato forte attività antibatterica, e due in particolare — denominati GW20 e KI16 — si sono avvicinati alle prestazioni di antibiotici consolidati nell’inibire la crescita batterica. La microscopia ha rivelato che questi peptidi danneggiano visibilmente le superfici cellulari batteriche, coerentemente con un meccanismo di distruzione della membrana. Importante, entrambi hanno mostrato danni minimi ai globuli rossi a concentrazioni terapeuticamente rilevanti e hanno dimostrato una forte capacità di prevenire e degradare biofilm batterici appiccicosi, spesso superando un antibiotico standard.
Cosa significa per i medicinali del futuro
Per i non specialisti, il messaggio chiave è che gli autori hanno costruito un ciclo funzionante di “progetta‑testa” in cui l’IA propone molti nuovi peptidi uccidi‑germi, li seleziona tramite un comitato di modelli e poi conferma i successi in laboratorio. Anche se non tutte le sequenze in cima alla classifica hanno funzionato, il tasso di successo — quattro peptidi attivi su nove testati — è molto più alto rispetto allo screening cieco tradizionale. Le due molecole più promettenti mostrano già un mix utile di potenza, sicurezza e capacità di combattere i biofilm, suggerendo possibili terapie future per infezioni ostinate. Altrettanto importante, la stessa pipeline modulare potrebbe essere riadattata per progettare altri peptidi medici, come agenti mirati al cancro o molecole antivirali, offrendo un modello flessibile per la scoperta di farmaci accelerata dall’IA di fronte alla crescente resistenza antimicrobica.
Citazione: Liu, J., Chen, Y., Tang, J. et al. Deep learning-driven integrated pipeline for de novo design and synthesis of antimicrobial peptides. npj Drug Discov. 3, 15 (2026). https://doi.org/10.1038/s44386-026-00045-6
Parole chiave: peptidi antimicrobici, intelligenza artificiale, scoperta di farmaci, resistenza agli antibiotici, biofilm