Clear Sky Science · zh
对基于适配体与CRISPR-Cas12a的小分子检测生物传感器的批判性评估
为什么微量污染物和快速检测很重要
从饮用水与河流到我们盘中的食物和服用的药物,无数的小分子遍布环境与体内。有些是救命药物;有些则是有毒的污染物。测量这些化合物通常依赖体积大且价格昂贵的仪器,不易带到现场或小型诊所。本文审视了一种有前景的替代方案:使用设计的DNA链与CRISPR酶,将微量分子的存在转化为明亮光信号的紧凑生化检测。作者旨在评估这一备受宣传的方法在实际应用中的表现如何。
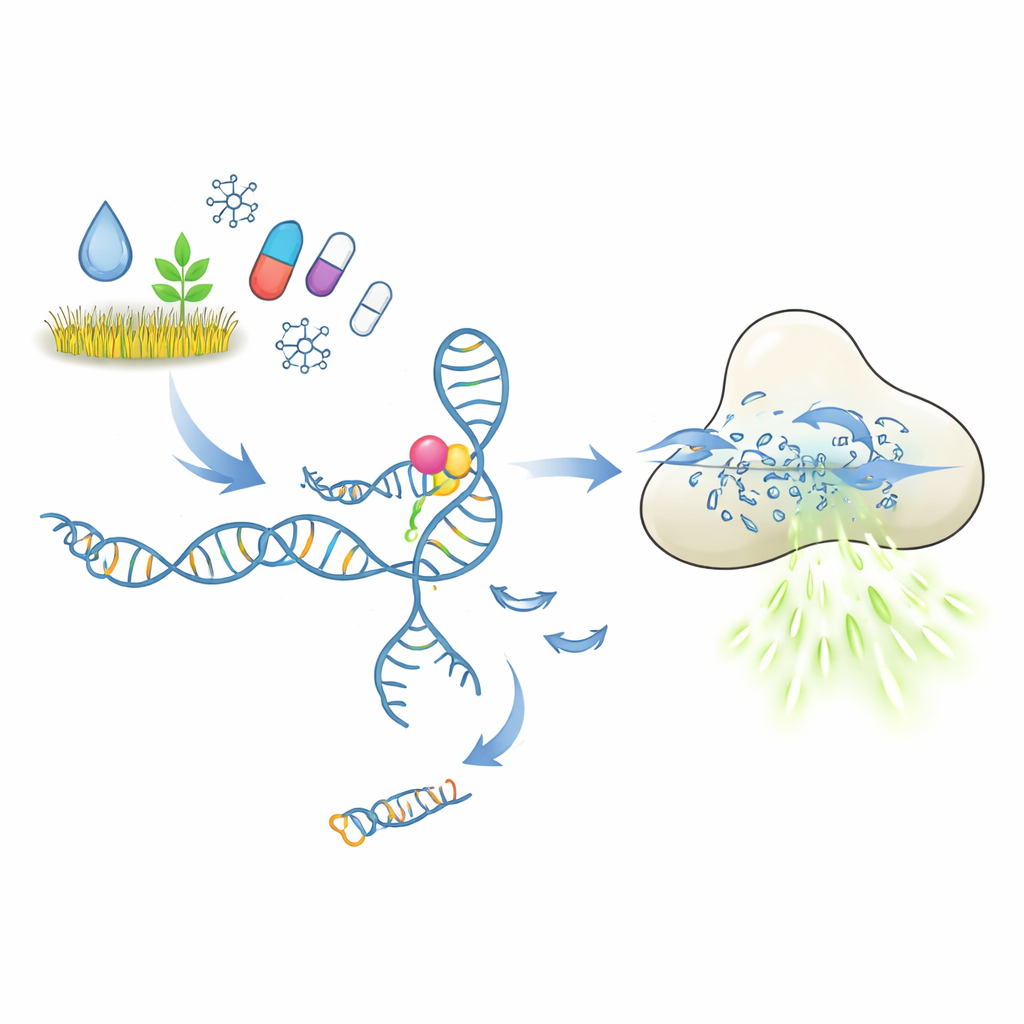
分子“锁与钥匙”检测应如何工作
这些检测的核心是适配体,即能折叠成特定结构并与目标结合的短DNA或RNA片段,功能类似抗体。在此研究中,适配体结合一段短DNA片段,作为触发子。当目标污染物或药物结合时,适配体应发生构象变化并释放该触发子。被释放的DNA随后激活CRISPR-Cas12a酶,Cas12a像分子碎纸机一样切割单链DNA。为Cas12a提供大量带荧光染料的短DNA报告分子后,每一次切割都会产生更多光信号。原则上,很少量的目标分子就能被放大为强而易测的荧光信号。
对基于CRISPR的传感器进行严格测试
研究者像机械师试验新发动机那样审慎地处理问题。首先,他们对Cas12a反应本身进行了优化:选择最佳缓冲液、金属离子、酶量和报告分子设计,以便在有触发DNA时获得强且可靠的光信号。在优化条件下,Cas12a可检测到极低水平的触发DNA,低至万亿分之一摩尔,并且具有重复性。这证明了信号放大部分——检测中的“放大器”——本身是稳健且灵敏的。
设计开始失效的地方
真正的挑战出现在他们将这一灵敏放大器与文献中报道的真实适配体连接时。团队挑选了九种适配体,据称可识别七种不同的小分子,包括农药、抗生素、来自藻类的肝毒素和抗疟药物。理论上,这些适配体在遇到目标时应释放触发DNA。作者仔细调整了触发DNA与每个适配体的结合强度,测试了不同温度、孵育时间和缓冲条件,甚至尝试了更复杂的方案:将适配体复合物固定到磁珠并在反应后分离。尽管做了大量努力,只有两种目标分子显示出明确信号。对于其余目标,加入目标分子并未导致溶液中触发DNA增加,这表明要么适配体并未如报道般结合,要么结合并未引起预期的构象变化和释放。
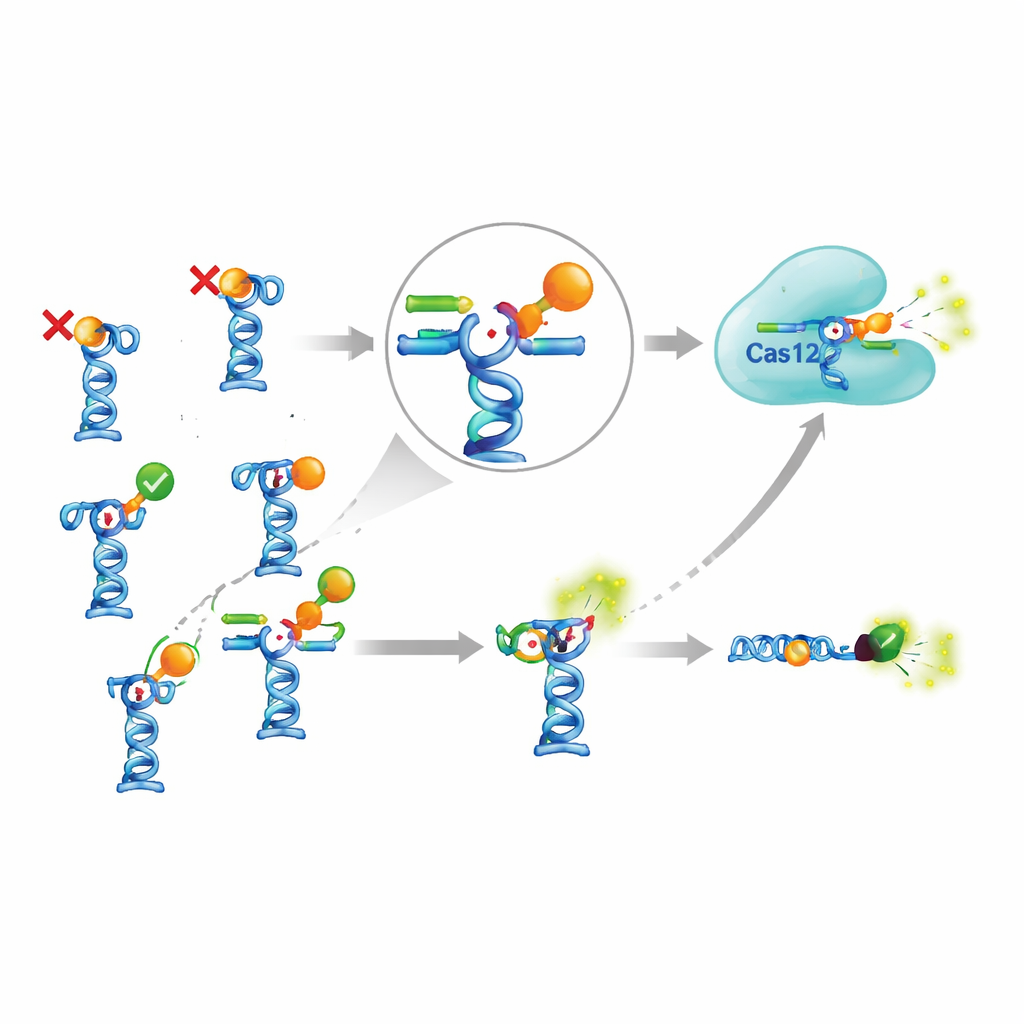
这套复杂方案值得投入吗?
为判断CRISPR附加模块是否真正划算,作者将其与不使用Cas12a的更简单适配体检测进行了比较。在这种更简单的设计中,适配体带有荧光染料,其互补短链带有猝灭基团;当互补短链被目标分子置换时,荧光直接升高。对于为数不多的可工作的目标之一——抗疟药吡喹酮,基于CRISPR的版本检测到的浓度略低于简单检测,但仅低约2到3倍。要达到这一有限提升,需要额外的酶、更多试剂、更长的流程和更多优化。同时,一些先前发表的适配体传感器(例如针对常见藻类毒素和杀虫剂氟虫腈)的结果完全无法重复,即便作者严格按照报道条件操作并使用独立方法检验结合能力。
这对未来快速检测意味着什么
研究得出的结论是:尽管Cas12a荧光系统本身很强大,但整体的适配体–CRISPR传感策略很脆弱。其成功依赖于适配体不仅能结合目标,还能可靠地释放触发DNA——这是一个苛刻的要求,许多已发表的适配体并不真正满足。当前,研究人员和以应用为导向的实验室应对即插即用的宣传保持谨慎,投入对适配体性能的彻底验证,并权衡是否采用更简单的适配体检测或质谱等既有方法更能满足需求。基于CRISPR的适配体传感器仍然是一个有吸引力的工具,但尚不是某些宣传所声称的用于小分子检测的通用解决方案。
引用: Brandenberg, O.F., Janssen, E.ML. & Schubert, O.T. A critical assessment of aptamer and CRISPR-Cas12a-based biosensors for small molecule detection. npj Biosensing 3, 28 (2026). https://doi.org/10.1038/s44328-026-00089-8
关键词: 适配体生物传感器, CRISPR-Cas12a 检测, 小分子传感, 环境污染物, 荧光测定