Clear Sky Science · tr
Aptamer ve CRISPR‑Cas12a tabanlı biyo-sensörlerin küçük molekül tespiti için eleştirel değerlendirmesi
Neden küçük kirleticiler ve hızlı testler önemli
İçme suyundan ve nehirlerden tabağımızdaki yiyeceklere ve aldığımız ilaçlara kadar sayısız küçük molekül çevremizden ve vücudumuzdan geçer. Bazıları hayat kurtarıcı ilaçlar; diğerleri zehirli kirleticilerdir. Bu bileşenlerin ölçülmesi genellikle ağır ve pahalı cihazlar gerektirir; bunları sahaya veya küçük bir kliniğe taşımak zordur. Bu makale umut vaat eden bir alternatifi inceliyor: tasarımcı DNA dizileri ve CRISPR enzimleri kullanarak küçük moleküllerin varlığını parlak bir ışık sinyaline dönüştüren kompakt biyokimyasal testler. Yazarlar, bu çok övülen yaklaşımın pratikte gerçekte ne kadar iyi çalıştığını değerlendirmeyi amaçladılar.
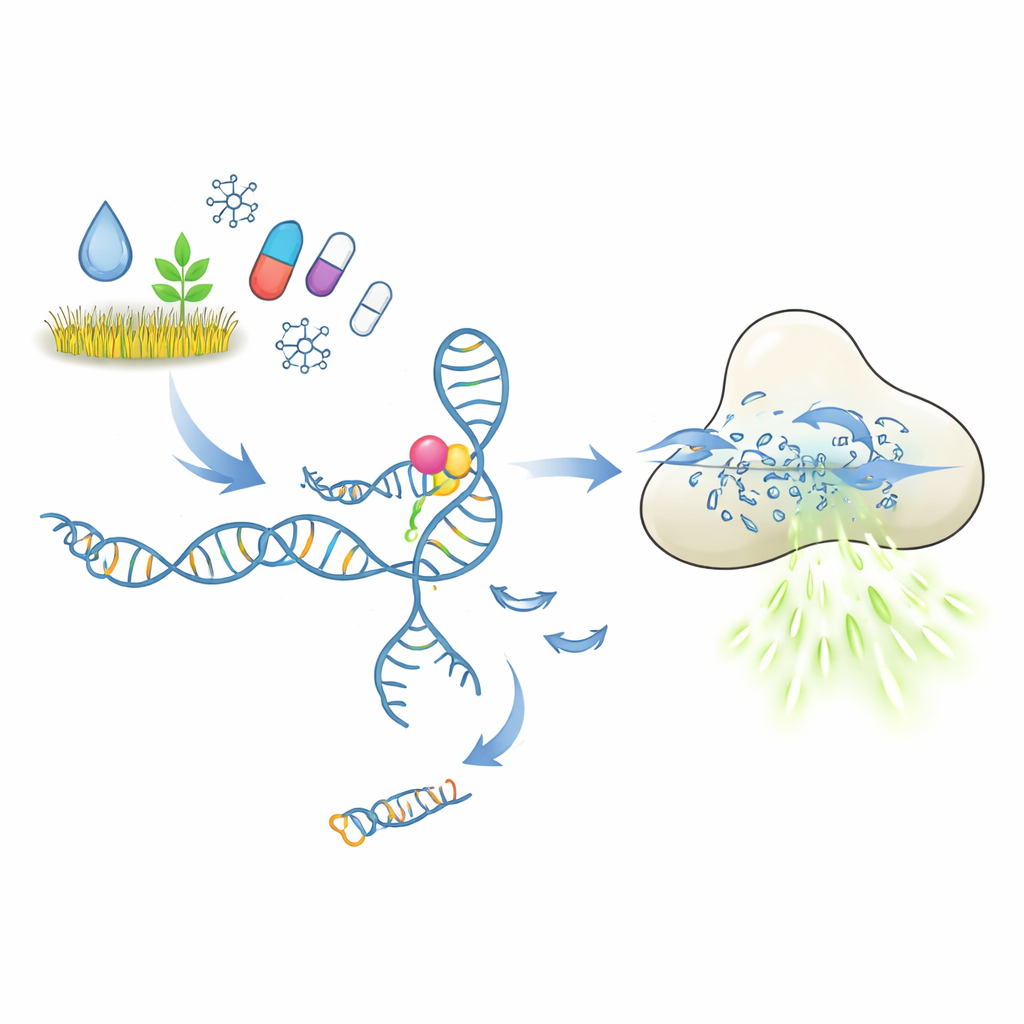
Moleküler kilit‑anahtar testinin nasıl çalışması beklenir
Bu testlerin merkezinde aptamerler bulunur; seçilmiş hedefe tutunabilecek şekilde katlanan kısa DNA veya RNA parçaları, tıpkı antikorlar gibi. Burada incelenen düzenekte bir aptamer, tetikleyici olarak görev yapan kısa bir DNA parçasına tutunur. Hedef kirletici veya ilaç bağlandığında, aptamerin şekil değiştirip bu tetikleyiciyi serbest bırakması beklenir. Serbest kalan DNA daha sonra CRISPR‑Cas12a enzimini aktive eder; Cas12a tek sarmallı DNA’yı kesen moleküler bir “kağıt öğütücü” gibi davranır. Cas12a’ya çok sayıda floresan boya taşıyan kısa DNA raporu sağlandığında, her kesim daha fazla ışık üretir. İlkeler itibarıyla, çok küçük bir hedef molekül miktarı güçlü ve kolay ölçülebilir bir floresans sinyaline dönüştürülebilir.
CRISPR tabanlı sensörü test etmek
Araştırmacılar sorunu yeni bir motoru dikkatle test eden mekanikler gibi ele aldılar. Önce Cas12a reaksiyonunu optimize ettiler: tetik DNA bulunduğunda güçlü ve güvenilir ışık sinyalleri almak için en iyi tamponu, metal iyonlarını, enzim miktarını ve rapor tasarımını seçtiler. Optimize edilmiş koşullar altında Cas12a, tetik DNA için trilyonda bir mol düzeyine kadar çok düşük seviyeleri tespit edebildi ve bunu tekrarlanabilir şekilde yaptı. Bu, sinyal verici mekanizmanın—testin “amplifikatör” kısmının—kendi başına sağlam ve hassas olduğunu doğruladı.
Tasarımın başarısız olduğu noktalar
Gerçek zorluk, bu hassas amplifikatörü bilimsel literatürdeki gerçek aptamerlere bağladıklarında ortaya çıktı. Ekip, pestisitler, antibiyotikler, alglerden kaynaklanan karaciğer toksini ve sıtma ilaçları da dahil olmak üzere yedi farklı küçük molekülü tanıdığı bildirilen dokuz aptamer seçti. Teoride bu aptamerler hedefleriyle karşılaştıklarında tetik DNA’yı serbest bırakmalıydı. Yazarlar, her aptamer için tetik DNA’nın ne kadar güçlü yapıştığını dikkatle ayarladı, farklı sıcaklıkları, inkübasyon sürelerini ve tampon koşullarını test etti ve hatta aptamer komplekslerinin manyetik boncuklara bağlandığı ve reaksiyondan sonra ayrıldığı daha karmaşık bir versiyonu denediler. Bu kapsamlı çabaya rağmen, yedi hedef molekülden yalnızca ikisi için net sinyaller ortaya çıktı. Diğerleri için hedef eklendiğinde çözeltide ek tetik DNA gözlemlenmedi; bu da ya aptamerlerin iddia edildiği gibi bağlanmadığını ya da bağlanmanın beklenen şekil değişikliğine ve serbest bırakmaya yol açmadığını düşündürüyor.
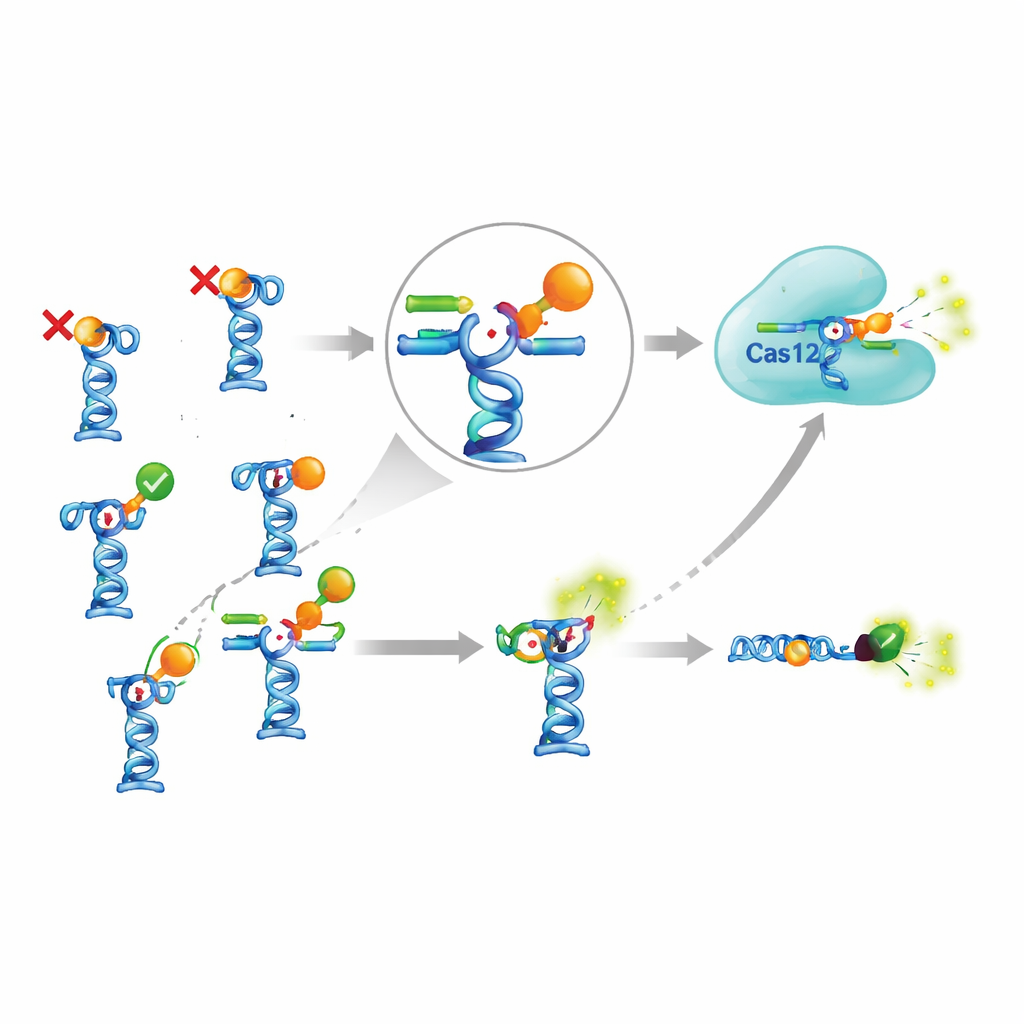
Bu karmaşık kurulum zahmete değiyor mu?
CRISPR eklentisinin gerçekten fayda sağlayıp sağlamadığını değerlendirmek için yazarlar, Cas12a’yı tamamen atlayan daha basit bir aptamer testiyle karşılaştırma yaptılar. Bu daha basit tasarımda aptamer bir floresan boya taşır ve eş parça bir ışığı söndüren grup taşır; eş parça hedef molekül tarafından yer değiştirdiğinde floresans doğrudan artar. Çalışan az sayıdaki hedeften biri olan sıtma ilacı piperaquine için, CRISPR tabanlı versiyon basit teste göre biraz daha düşük konsantrasyonları tespit etti, ama yalnızca iki ila üç kat daha hassas oldu. Bu mütevazı kazancı elde etmek ekstra enzimler, daha fazla reaktif, daha uzun protokoller ve daha fazla optimizasyon gerektirdi. Aynı zamanda, literatürde daha önce yayınlanmış bazı aptamer tabanlı sensörler—örneğin yaygın bir alg toksini ve böcek ilacı fipronil için olanlar—yazarlar bildirilen koşulları dikkatle takip edip bağımsız bir bağlanma testi yaptıklarında bile hiç yeniden üretilemedi.
Gelecekteki hızlı testler için bunun anlamı
Çalışma, Cas12a floresans sisteminin kendisinin güçlü olduğunu, ancak genel aptamer–CRISPR sensör stratejisinin kırılgan olduğunu sonucuna varıyor. Başarı, yalnızca hedeflerine bağlanmakla kalmayıp aynı zamanda güvenilir şekilde tetik DNA’yı serbest bırakabilen aptamerlere bağlıdır—bu, birçok yayımlanmış aptamerin gerçekte karşılamadığı zorlayıcı bir gerekliliktir. Şimdilik, araştırmacılar ve uygulamaya odaklı laboratuvarlar, tak-çalıştır iddialarını dikkatle ele almalı, aptamer performansının titiz doğrulamasına yatırım yapmalı ve daha basit aptamer testlerinin ya da kütle spektrometresi gibi yerleşik yöntemlerin ihtiyaçlarını daha iyi karşılayıp karşılamayacağını değerlendirmelidir. CRISPR tabanlı aptasensörler ilgi çekici bir araç olmaya devam etse de, bazen ilan edildiği kadar evrensel bir çözüm değiller.
Atıf: Brandenberg, O.F., Janssen, E.ML. & Schubert, O.T. A critical assessment of aptamer and CRISPR-Cas12a-based biosensors for small molecule detection. npj Biosensing 3, 28 (2026). https://doi.org/10.1038/s44328-026-00089-8
Anahtar kelimeler: aptamer biyosensörleri, CRISPR‑Cas12a tespiti, küçük molekül algılama, çevresel kirleticiler, floresans testleri