Clear Sky Science · fr
Une évaluation critique des biocapteurs à aptamères et basés sur CRISPR-Cas12a pour la détection de petites molécules
Pourquoi les polluants minuscules et les tests rapides comptent
De l’eau potable et des rivières aux aliments dans nos assiettes en passant par les médicaments que nous prenons, d’innombrables petites molécules circulent dans notre environnement et nos organismes. Certaines sont des médicaments vitaux ; d’autres, des contaminants toxiques. Mesurer ces composés nécessite généralement des instruments volumineux et coûteux, difficiles à transporter sur le terrain ou dans une petite clinique. Cet article examine une alternative prometteuse : des tests biochimiques compacts qui utilisent des brins d’ADN conçus et des enzymes CRISPR pour convertir la présence de minuscules molécules en un signal lumineux. Les auteurs se sont donné pour objectif d’évaluer l’efficacité réelle de cette approche très médiatisée.
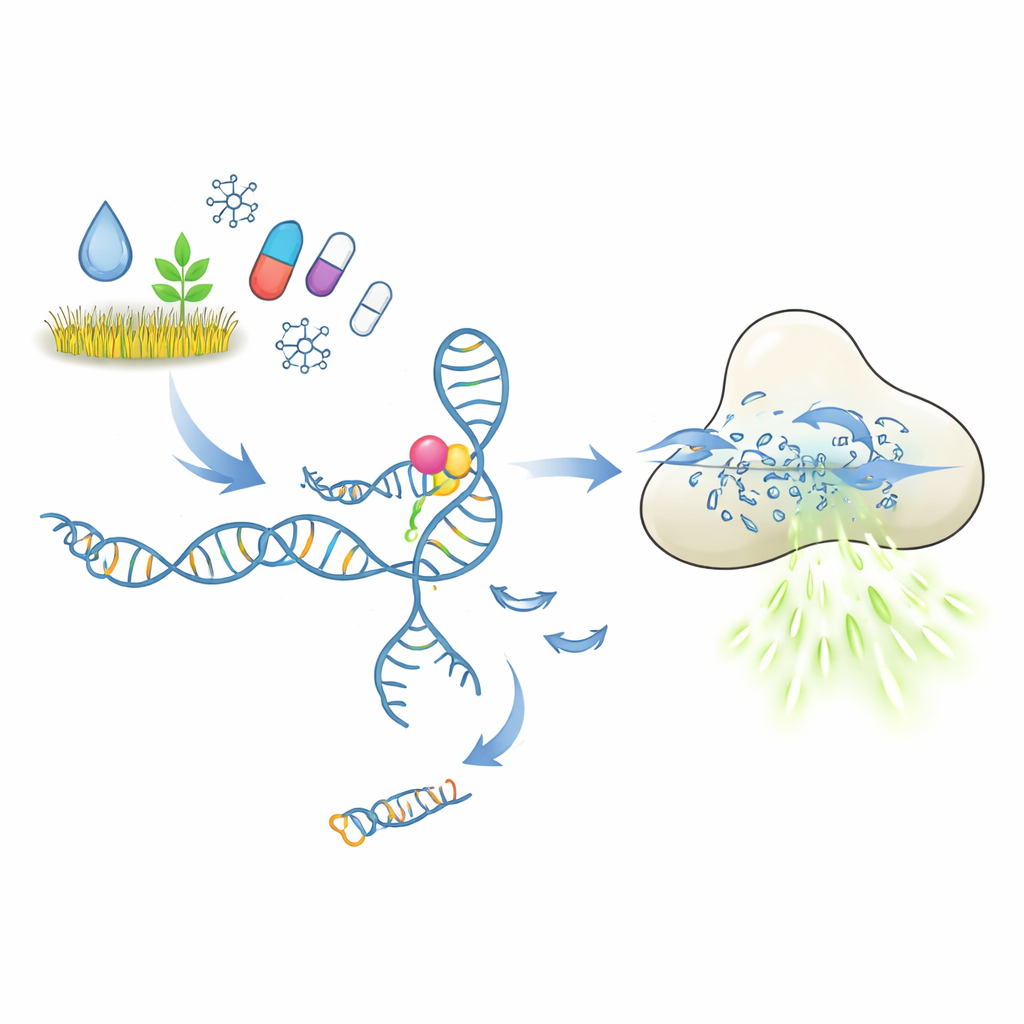
Comment un test moléculaire « serrure-et-clé » est censé fonctionner
Au cœur de ces tests se trouvent les aptamères, de courts morceaux d’ADN ou d’ARN qui se replient en formes capables de se fixer sur une cible choisie, de façon analogue aux anticorps. Dans le montage étudié ici, un aptamère maintient un court fragment d’ADN qui joue le rôle de déclencheur. Lorsque le polluant ou le médicament cible se lie, l’aptamère est censé changer de conformation et libérer ce déclencheur. L’ADN libéré active alors l’enzyme CRISPR-Cas12a, qui se comporte comme un destructeur moléculaire pour l’ADN simple brin. En fournissant à Cas12a de nombreux petits réporteurs d’ADN portant un colorant fluorescent, chaque clivage génère davantage de lumière. En principe, une quantité infime de molécule cible devrait ainsi être convertie en un signal de fluorescence fort et facile à mesurer.
Mettre le capteur à base de CRISPR à l’épreuve
Les chercheurs ont abordé le problème comme des mécaniciens testant soigneusement un nouveau moteur. D’abord, ils ont optimisé la réaction Cas12a elle-même : choix du meilleur tampon, des ions métalliques, de la quantité d’enzyme et du design des réporteurs pour obtenir des signaux lumineux forts et fiables en présence d’ADN déclencheur. Dans des conditions optimisées, Cas12a pouvait détecter des niveaux extrêmement bas d’ADN déclencheur, jusqu’à des billièmes de mole, et le faisait de façon reproductible. Cela a confirmé que la machinerie de signalisation — la partie « amplificateur » du test — était robuste et sensible en elle-même.
Où le dispositif commence à échouer
Le vrai défi est apparu lorsqu’ils ont connecté cet amplificateur sensible à de vrais aptamères issus de la littérature scientifique. L’équipe a sélectionné neuf aptamères décrits pour reconnaître sept petites molécules différentes, y compris des pesticides, des antibiotiques, une toxine hépatique produite par des algues et des antipaludiques. En théorie, ces aptamères devraient libérer l’ADN déclencheur lorsqu’ils rencontrent leurs cibles. Les auteurs ont soigneusement ajusté l’affinité entre l’ADN déclencheur et chaque aptamère, testé différentes températures, durées d’incubation et conditions de tampon, et ont même essayé une version plus complexe où les complexes d’aptamères étaient fixés sur des billes magnétiques puis séparés de la réaction. Malgré cet effort étendu, des signaux nets sont apparus pour seulement deux des sept molécules cibles. Pour les autres, l’ajout de la cible n’a pas entraîné d’augmentation d’ADN déclencheur en solution, ce qui suggère que soit les aptamères ne se liaient pas comme annoncé, soit la liaison n’induisait pas le changement de conformation attendu et la libération.
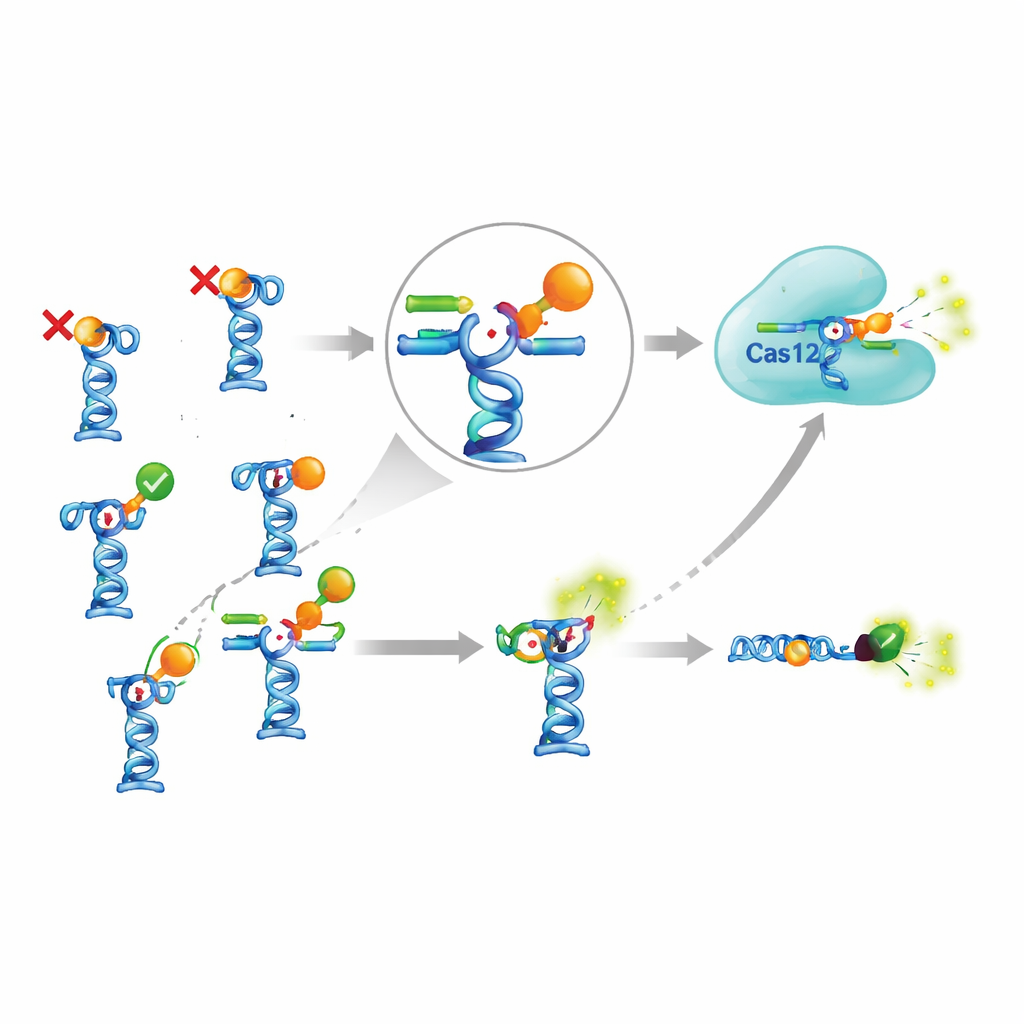
Le montage compliqué vaut‑il la peine ?
Pour juger si l’ajout de CRISPR apporte réellement un avantage, les auteurs l’ont comparé à un test aptamère plus simple qui évite complètement Cas12a. Dans ce design simplifié, l’aptamère porte un colorant fluorescent et son brin partenaire porte un groupe d’extinction ; lorsque le brin partenaire est déplacé par la molécule cible, la fluorescence augmente directement. Pour l’une des rares cibles fonctionnelles, le pipéraquine antipaludique, la version basée sur CRISPR détectait des concentrations légèrement plus basses que le test simple, mais seulement d’un facteur de deux à trois. Obtenir ce gain modeste a exigé des enzymes supplémentaires, davantage de réactifs, des protocoles plus longs et plus d’optimisation. Parallèlement, certains capteurs à base d’aptamères publiés précédemment — par exemple pour une toxine d’algue courante et l’insecticide fipronil — n’ont pu être reproduits du tout, même lorsque les auteurs ont suivi de près les conditions rapportées et utilisé une méthode indépendante pour tester la liaison.
Ce que cela implique pour les futurs tests rapides
L’étude conclut que si le système de fluorescence Cas12a est en lui‑même puissant, la stratégie globale aptamère–CRISPR est fragile. Son succès dépend d’aptamères qui non seulement lient leurs cibles mais libèrent aussi de manière fiable l’ADN déclencheur — une exigence exigeante que nombre d’aptamères publiés ne remplissent pas réellement. Pour l’heure, les chercheurs et les laboratoires orientés applications devraient considérer avec prudence les affirmations de type « branchez et utilisez », investir dans une validation approfondie des performances des aptamères et évaluer si des tests aptamères plus simples ou des méthodes établies comme la spectrométrie de masse pourraient mieux répondre à leurs besoins. Les aptasenseurs basés sur CRISPR restent un outil intrigant, mais pas encore la solution universelle pour la détection de petites molécules telle qu’on les a parfois présentés.
Citation: Brandenberg, O.F., Janssen, E.ML. & Schubert, O.T. A critical assessment of aptamer and CRISPR-Cas12a-based biosensors for small molecule detection. npj Biosensing 3, 28 (2026). https://doi.org/10.1038/s44328-026-00089-8
Mots-clés: biocapteurs à aptamères, détection CRISPR-Cas12a, détection de petites molécules, polluants environnementaux, tests de fluorescence