Clear Sky Science · es
Una evaluación crítica de biosensores basados en aptámeros y CRISPR-Cas12a para la detección de pequeñas moléculas
Por qué importan los contaminantes diminutos y las pruebas rápidas
Desde el agua potable y los ríos hasta los alimentos que consumimos y los fármacos que tomamos, innumerables pequeñas moléculas circulan por nuestro entorno y nuestros cuerpos. Algunas son medicamentos que salvan vidas; otras son contaminantes tóxicos. Medir estos compuestos suele requerir instrumentos voluminosos y caros, difíciles de llevar al campo o a una clínica pequeña. Este artículo examina una alternativa prometedora: pruebas bioquímicas compactas que usan hebras de ADN diseñadas y enzimas CRISPR para convertir la presencia de moléculas diminutas en una señal luminosa. Los autores se propusieron comprobar qué tan bien funciona en la práctica este enfoque tan promocionado.
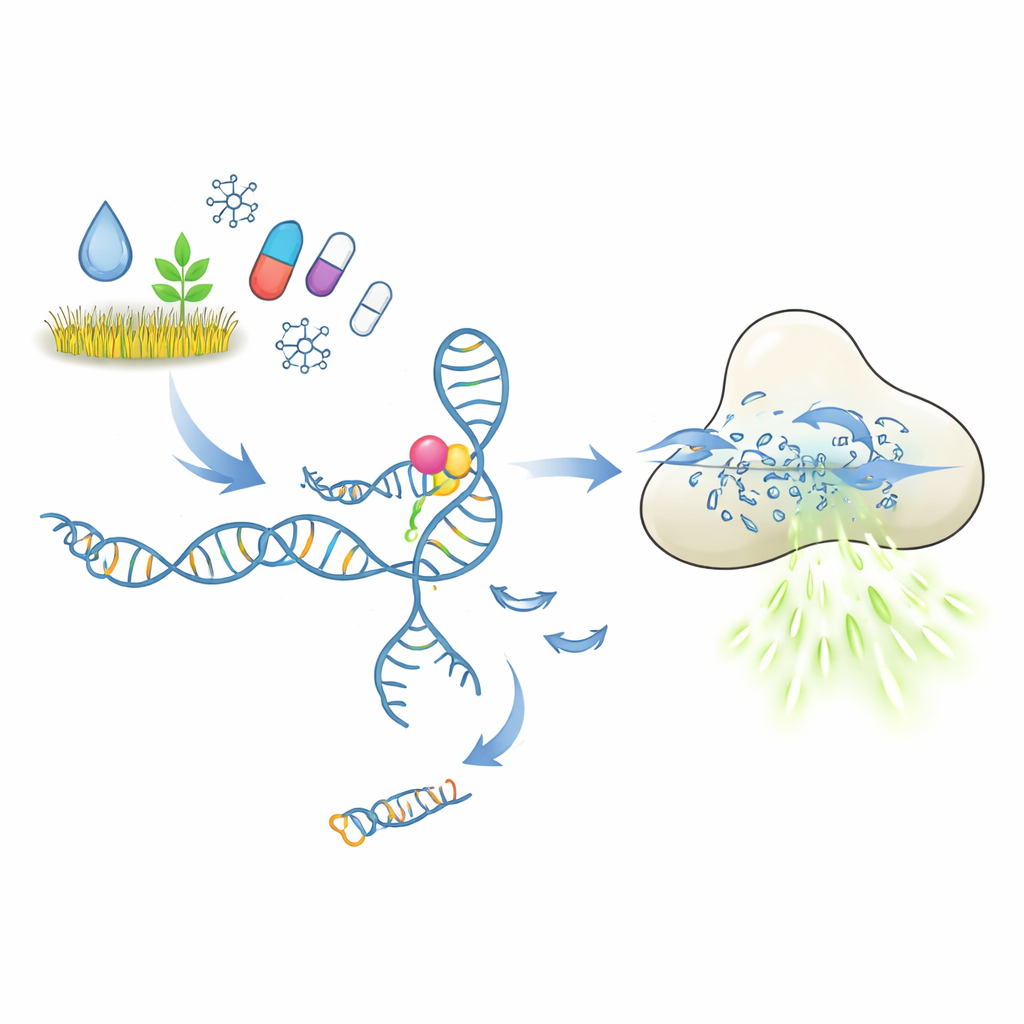
Cómo debería funcionar una prueba molecular de cerradura y llave
En el núcleo de estas pruebas están los aptámeros, fragmentos cortos de ADN o ARN que se pliegan en formas capaces de unirse a un objetivo elegido, de forma similar a los anticuerpos. En el sistema estudiado aquí, un aptámero sujeta una pieza corta de ADN que actúa como gatillo. Cuando el contaminante o fármaco objetivo se une, se espera que el aptámero cambie de forma y libere ese gatillo. El ADN liberado entonces activa la enzima CRISPR-Cas12a, que se comporta como una trituradora molecular para ADN monocatenario. Al proporcionar a Cas12a muchos reporteros de ADN cortos con una molécula fluorescente, cada corte produce más luz. En principio, una cantidad mínima de la molécula objetivo debería así convertirse en una señal de fluorescencia fuerte y fácil de medir.
Poniendo a prueba el sensor basado en CRISPR
Los investigadores abordaron el problema como mecánicos cuidadosos probando un nuevo motor. Primero, optimizaron la reacción de Cas12a: escogieron el mejor tampón, iones metálicos, cantidad de enzima y diseño de reportero para obtener señales luminosas fuertes y fiables cuando estaba presente el ADN gatillo. Bajo condiciones optimizadas, Cas12a pudo detectar niveles extremadamente bajos de ADN gatillo, hasta fracciones de mol a escala de billonésimas a trillones de mol, y lo hizo de manera reproducible. Esto confirmó que la maquinaria de señalización—la parte “amplificadora” de la prueba—era robusta y sensible por sí sola.
Dónde el diseño empieza a fallar
El verdadero desafío surgió cuando conectaron este amplificador sensible con aptámeros reales descritos en la literatura científica. El equipo seleccionó nueve aptámeros reportados para reconocer siete pequeñas moléculas distintas, incluidos pesticidas, antibióticos, una toxina hepática de algas y fármacos antipalúdicos. En teoría, estos aptámeros deberían liberar el ADN gatillo al encontrarse con sus objetivos. Los autores ajustaron cuidadosamente la fuerza con la que el ADN gatillo se adhería a cada aptámero, probaron diferentes temperaturas, tiempos de incubación y condiciones de tampón, e incluso probaron una versión más compleja donde los complejos de aptámero estaban unidos a perlas magnéticas y se separaban de la reacción después. A pesar de este esfuerzo extenso, aparecieron señales claras para solo dos de las siete moléculas objetivo. Para las demás, añadir el objetivo no produjo más ADN gatillo en solución, lo que sugiere que o bien los aptámeros no se unían como se afirmaba, o la unión no provocaba el cambio conformacional esperado y la liberación.
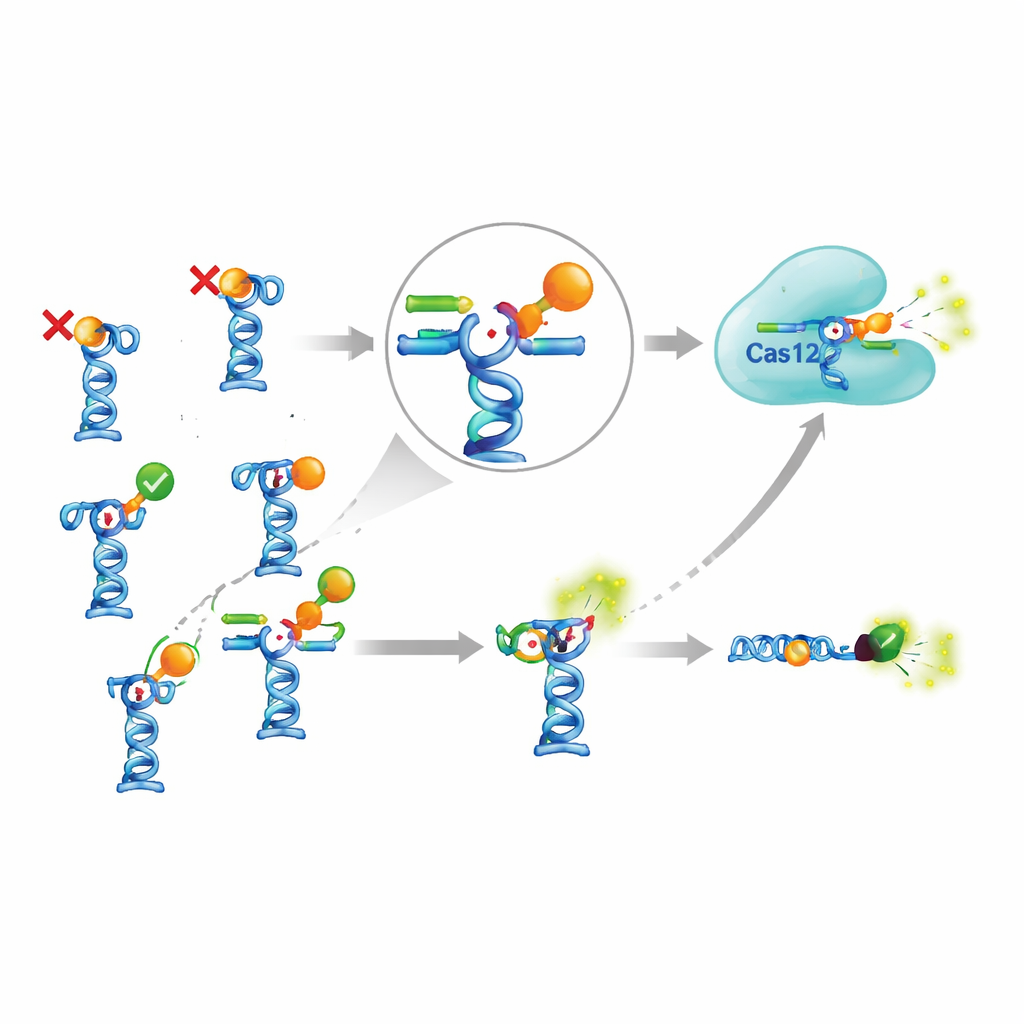
¿Vale la pena el montaje complicado?
Para juzgar si el añadido de CRISPR realmente compensa, los autores lo compararon con una prueba de aptámero más simple que prescinde de Cas12a por completo. En este diseño más sencillo, el aptámero lleva una molécula fluorescente y su hebra complementaria lleva un grupo que apaga la luz; cuando la hebra complementaria es desplazada por la molécula objetivo, la fluorescencia aumenta directamente. Para uno de los pocos objetivos que funcionaron, el antipalúdico piperaquina, la versión basada en CRISPR detectó concentraciones ligeramente más bajas que la prueba simple, pero solo por un factor de dos o tres. Lograr esta ganancia modesta requirió enzimas adicionales, más reactivos, protocolos más largos y mayor optimización. Al mismo tiempo, algunos sensores basados en aptámeros publicados anteriormente—por ejemplo, para una toxina algal común y el insecticida fipronil—no pudieron reproducirse en absoluto, incluso cuando los autores siguieron las condiciones reportadas de cerca y usaron un método independiente para probar la unión.
Qué significa esto para las pruebas rápidas del futuro
El estudio concluye que, si bien el sistema de fluorescencia Cas12a en sí es poderoso, la estrategia global de sensor aptámero–CRISPR es frágil. Su éxito depende de aptámeros que no solo se unan a sus objetivos sino que además liberen de forma fiable el ADN gatillo—un requisito exigente que muchos aptámeros publicados no cumplen realmente. Por ahora, los investigadores y los laboratorios orientados a aplicaciones deberían tratar las afirmaciones de tipo plug-and-play con cautela, invertir en una validación rigurosa del rendimiento del aptámero y sopesar si pruebas de aptámeros más simples o métodos establecidos como la espectrometría de masas pueden servirles mejor. Los aptasensores basados en CRISPR siguen siendo una herramienta intrigante, pero aún no la solución universal para la detección de pequeñas moléculas que a veces se ha anunciado como tal.
Cita: Brandenberg, O.F., Janssen, E.ML. & Schubert, O.T. A critical assessment of aptamer and CRISPR-Cas12a-based biosensors for small molecule detection. npj Biosensing 3, 28 (2026). https://doi.org/10.1038/s44328-026-00089-8
Palabras clave: biosensores de aptámeros, detección CRISPR-Cas12a, detección de pequeñas moléculas, contaminantes ambientales, ensayos de fluorescencia