Clear Sky Science · pl
Krytyczna ocena biosensorów opartych na aptamerach i CRISPR‑Cas12a do wykrywania małych cząsteczek
Dlaczego drobne zanieczyszczenia i szybkie testy mają znaczenie
Od wody pitnej i rzek po żywność na naszych talerzach i przyjmowane leki — niezliczone małe cząsteczki krążą w naszym środowisku i organizmach. Niektóre ratują życie; inne są toksycznymi zanieczyszczeniami. Pomiar tych związków zwykle wymaga masywnych i drogich urządzeń, trudnych do zabrnięcia w teren lub do małej kliniki. Niniejsza praca analizuje obiecującą alternatywę: kompaktowe testy biochemiczne, które używają zaprojektowanych nici DNA i enzymów CRISPR do zamiany obecności drobnych cząsteczek na sygnał świetlny. Autorzy postawili sobie za cel sprawdzenie, jak dobrze ta medialna koncepcja działa w praktyce.
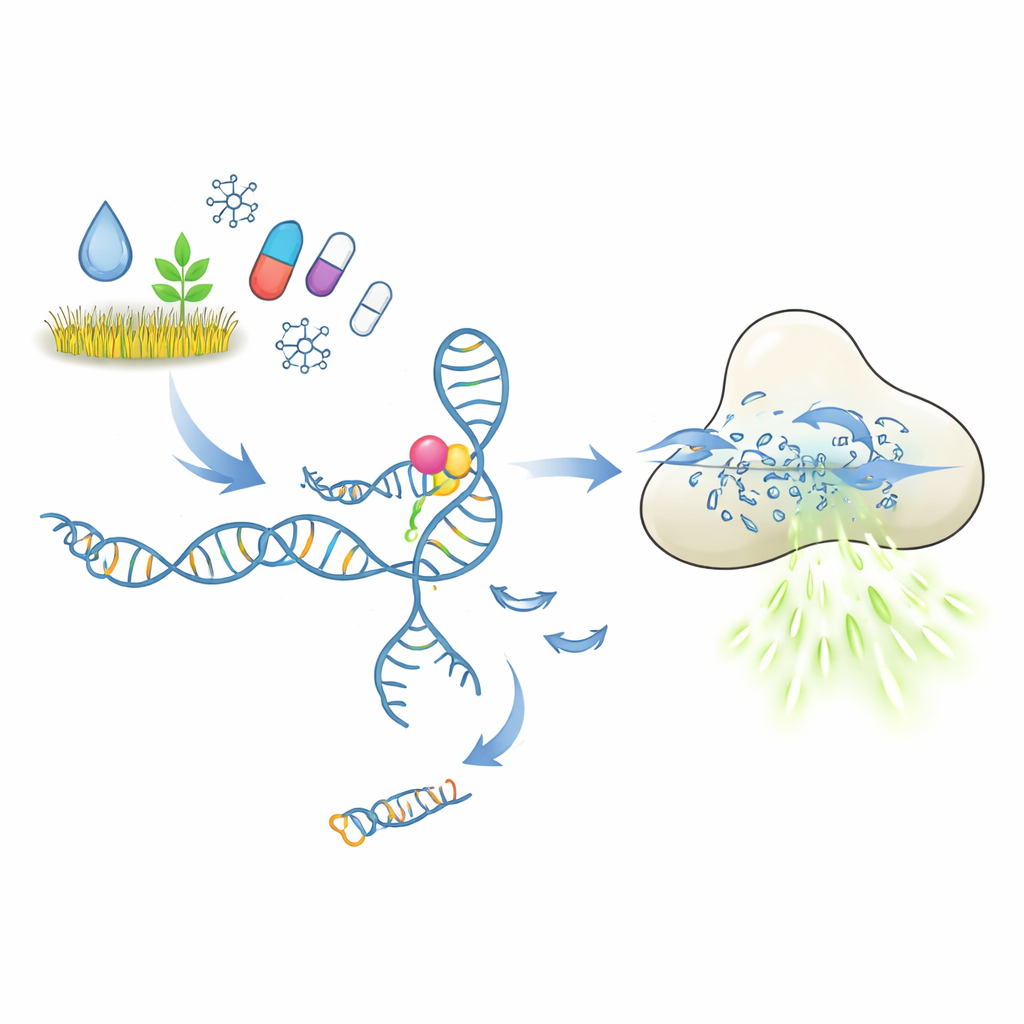
Jak ma działać molekularny test z zamkiem i kluczem
Rdzeń tych testów stanowią aptamery — krótkie fragmenty DNA lub RNA, które składają się w struktury zdolne wiązać wybrany cel, podobnie jak przeciwciała. W badanej konfiguracji aptamer utrzymuje krótki fragment DNA pełniący rolę spustu (triggera). Gdy docelowy zanieczyszczenie lub lek się zwiąże, aptamer ma zmienić konformację i uwolnić ten spust. Uwolnione DNA aktywuje enzym CRISPR‑Cas12a, który działa jak molekularna niszczarka jednoniciowego DNA. Dostarczając Cas12a wielu krótkich reporterów DNA z barwnikiem fluorescencyjnym, każde przecięcie generuje większą emisję światła. W teorii niewielka ilość cząsteczki docelowej powinna więc zostać przekształcona w silny, łatwy do zmierzenia sygnał fluorescencyjny.
Próba wydolności sensora opartego na CRISPR
Badacze podeszli do problemu jak mechanicy testujący nowy silnik. Najpierw sparametryzowali samą reakcję Cas12a: dobrali najlepszy bufor, jony metali, ilość enzymu i konstrukcję reportera, aby uzyskać silne i wiarygodne sygnały świetlne przy obecności spustu DNA. W zoptymalizowanych warunkach Cas12a potrafił wykrywać ekstremalnie niskie poziomy spustu DNA, sięgające trylionowych moli, i robił to powtarzalnie. Potwierdziło to, że układ sygnalizacyjny — „wzmacniacz” testu — sam w sobie był odporny i czuły.
Gdzie projekt zaczyna zawodzić
Prawdziwe wyzwanie pojawiło się, gdy połączyli ten czuły wzmacniacz z rzeczywistymi aptamerami z literatury naukowej. Zespół wybrał dziewięć aptamerów, które rzekomo rozpoznawały siedem różnych małych cząsteczek, w tym pestycydy, antybiotyki, toksynę wątrobową z alg oraz leki przeciwmalaryczne. W teorii aptamery te powinny uwalniać spust DNA po zetknięciu z celami. Autorzy starannie dostosowywali siłę wiązania spustu do każdego aptamera, testowali różne temperatury, czasy inkubacji i warunki buforowe, a nawet wypróbowali bardziej złożoną wersję, w której kompleksy aptamerowe były przytwierdzone do kulek magnetycznych i oddzielane z reakcji. Mimo tego rozległego wysiłku wyraźne sygnały pojawiły się tylko dla dwóch z siedmiu celów. W pozostałych przypadkach dodanie celu nie prowadziło do zwiększenia ilości spustu DNA w roztworze, co sugeruje, że aptamery nie wiązały tak, jak to zgłoszono, albo związanie nie powodowało oczekiwanej zmiany struktury i uwolnienia.
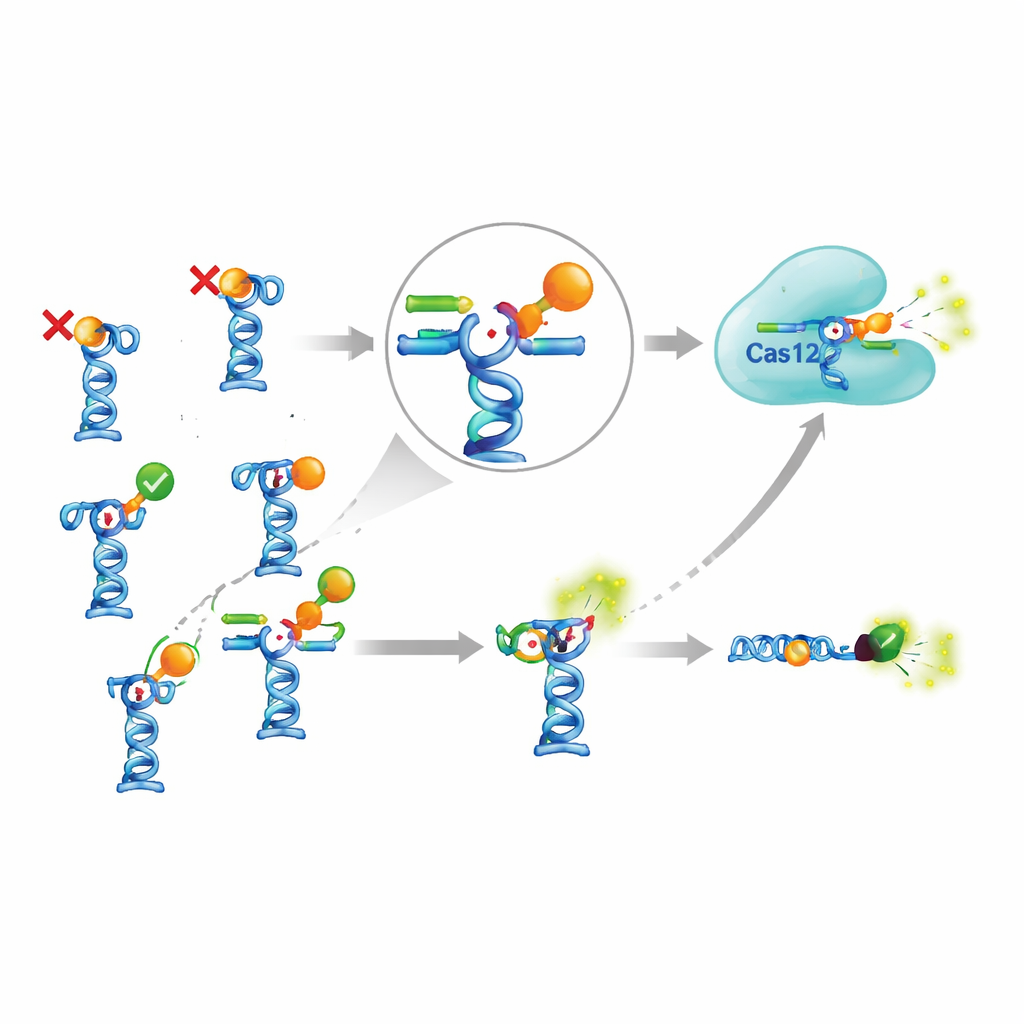
Czy skomplikowana konstrukcja jest tego warta?
Aby ocenić, czy dodatek CRISPR faktycznie się opłaca, autorzy porównali go z prostszym testem aptamerowym, który pomija Cas12a. W tej prostszej konstrukcji aptamer niesie barwnik fluorescencyjny, a jego partner ma grupę wygaszającą światło; gdy partner zostaje wyparty przez cząsteczkę docelową, fluorescencja wzrasta bezpośrednio. Dla jednego z nielicznych działających celów — przeciwmalarycznego piperaquine — wersja oparta na CRISPR wykrywała nieco niższe stężenia niż prosty test, ale tylko w przybliżeniu o czynnik dwa do trzech. Uzyskanie tego skromnego zysku wymagało dodatkowych enzymów, więcej odczynników, dłuższych protokołów i większej optymalizacji. Jednocześnie niektóre wcześniej opublikowane sensory aptamerowe — na przykład dla powszechnej toksyny algowej i insektycydu fipronilu — nie dały się wcale odtworzyć, nawet gdy autorzy dokładnie stosowali się do opisanych warunków i użyli niezależnej metody do badania wiązania.
Co to oznacza dla przyszłych szybkich testów
Badanie konkluduje, że choć system fluorescencyjny Cas12a jest sam w sobie potężny, ogólna strategia aptamer–CRISPR jest krucha. Jej powodzenie zależy od aptamerów, które nie tylko wiążą cele, lecz także niezawodnie uwalniają spust DNA — wymaganie trudne do spełnienia, którego wiele opublikowanych aptamerów faktycznie nie spełnia. Na razie badacze i laboratoria nastawione na zastosowania powinni podchodzić ostrożnie do twierdzeń o plug-and-play, inwestować w gruntowną walidację działania aptamerów i rozważyć, czy prostsze testy aptamerowe lub ustalone metody, takie jak spektrometria mas, nie będą lepiej odpowiadać ich potrzebom. Aptasensory oparte na CRISPR pozostają intrygującym narzędziem, lecz nie są jeszcze uniwersalnym rozwiązaniem do wykrywania małych cząsteczek, jak bywało to czasem przedstawiane.
Cytowanie: Brandenberg, O.F., Janssen, E.ML. & Schubert, O.T. A critical assessment of aptamer and CRISPR-Cas12a-based biosensors for small molecule detection. npj Biosensing 3, 28 (2026). https://doi.org/10.1038/s44328-026-00089-8
Słowa kluczowe: biosensory aptamerowe, wykrywanie CRISPR‑Cas12a, wykrywanie małych cząsteczek, zanieczyszczenia środowiska, testy fluorescencyjne