Clear Sky Science · de
Eine kritische Bewertung von Aptamer- und CRISPR-Cas12a-basierten Biosensoren zur Detektion von kleinen Molekülen
Warum winzige Schadstoffe und schnelle Tests wichtig sind
Vom Trinkwasser und Flüssen bis hin zu Lebensmitteln auf unseren Tellern und den Medikamenten, die wir einnehmen: Unzählige kleine Moleküle zirkulieren in unserer Umwelt und in unseren Körpern. Einige sind lebensrettende Arzneistoffe, andere toxische Kontaminanten. Das Messen dieser Verbindungen erfordert meist sperrige und teure Geräte, die sich nur schwer ins Feld oder in eine kleine Klinik bringen lassen. Dieser Artikel untersucht eine vielversprechende Alternative: kompakte biochemische Tests, die Designer-DNA-Stränge und CRISPR-Enzyme nutzen, um das Vorhandensein winziger Moleküle in ein helles Lichts signal zu verwandeln. Die Autoren wollten herausfinden, wie gut dieser stark beworbene Ansatz in der Praxis tatsächlich funktioniert.
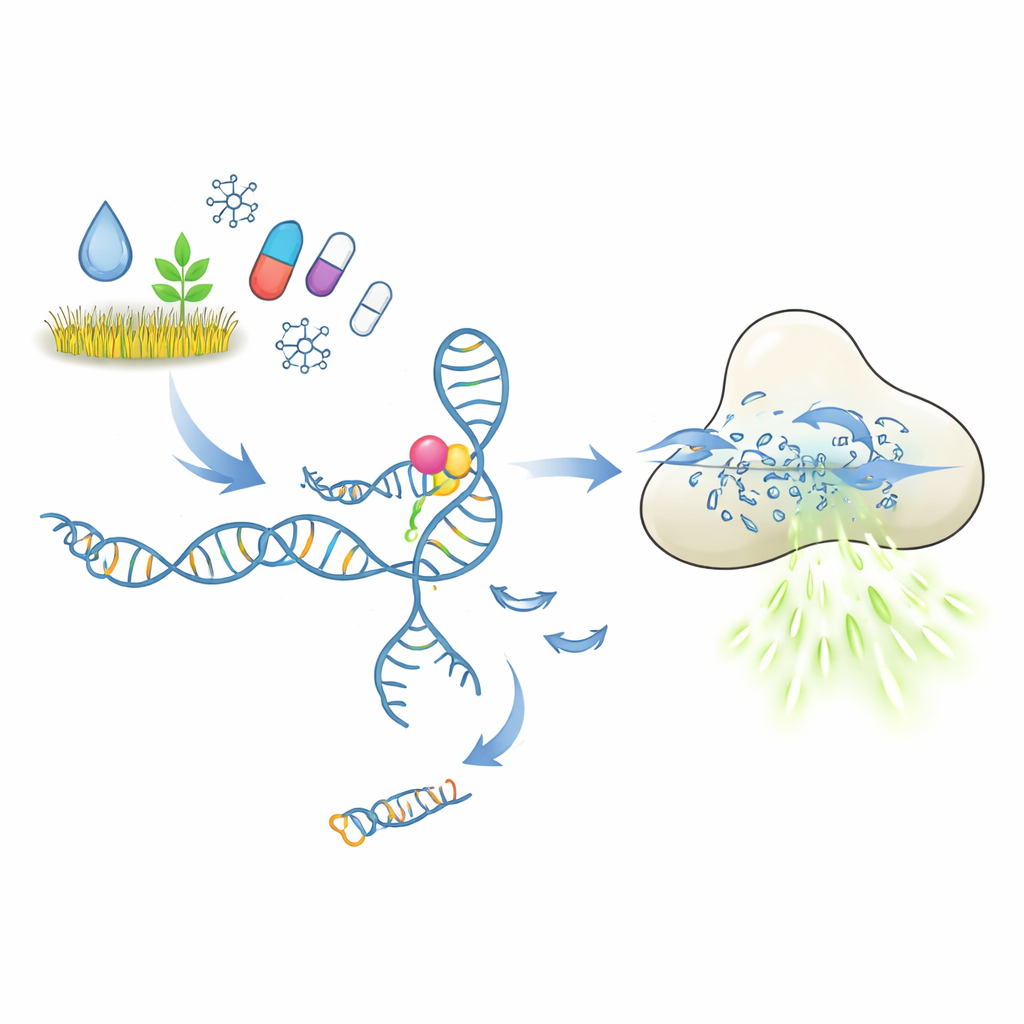
Wie ein molekulares Schloss-und-Schlüssel-Prinzip funktionieren soll
Im Zentrum dieser Tests stehen Aptamere, kurze DNA- oder RNA-Stücke, die sich zu Strukturen falten können, die an ein gewähltes Zielmolekül binden, ähnlich wie Antikörper. In dem hier untersuchten Aufbau hält ein Aptamer ein kurzes DNA-Stück fest, das als Auslöser fungiert. Bindet das Ziel-Persistenzstoff oder Medikament, soll das Aptamer seine Form ändern und diesen Auslöser freigeben. Die freigewordene DNA aktiviert dann das CRISPR-Cas12a-Enzym, das wie ein molekularer Papierschredder für einzelsträngige DNA wirkt. Indem man Cas12a viele kurze DNA-Reporter mit einem Fluoreszenzfarbstoff anbietet, erzeugt jeder Schnitt mehr Licht. Im Prinzip sollte so eine winzige Menge Zielmolekül in ein starkes, leicht messbares Fluoreszenzsignal umgewandelt werden können.
Das CRISPR-basierte Sensorprinzip auf dem Prüfstand
Die Forschenden näherten sich dem Problem wie sorgfältige Mechaniker, die einen neuen Motor testen. Zuerst optimierten sie die Cas12a-Reaktion selbst: Sie wählten das beste Puffer, Metallionen, Enzymmenge und Reporterdesign, um starke und zuverlässige Lichts ignale zu erhalten, wenn Auslöser-DNA vorhanden war. Unter optimierten Bedingungen konnte Cas12a extrem niedrige Mengen an Auslöser-DNA nachweisen, bis herunter zu Billionstel Molen, und tat dies reproduzierbar. Das bestätigte, dass die Signalisierungsmaschinerie — der „Verstärker“-Teil des Tests — für sich genommen robust und empfindlich war.
Wo das Design zu versagen beginnt
Die eigentliche Herausforderung zeigte sich, als sie diesen empfindlichen Verstärker mit realen Aptameren aus der Fachliteratur verbanden. Das Team wählte neun Aptamere aus, denen die Erkennung von sieben verschiedenen kleinen Molekülen zugeschrieben wurde, darunter Pestizide, Antibiotika, ein von Algen stammendes Lebergift und Antimalariamittel. Theoretisch sollten diese Aptamere den Auslöser-DNA freisetzen, wenn sie auf ihre Zielmoleküle treffen. Die Autoren passten sorgfältig an, wie stark die Auslöser-DNA an jedes Aptamer gebunden war, testeten verschiedene Temperaturen, Inkubationszeiten und Pufferbedingungen und versuchten sogar eine komplexere Variante, bei der Aptamer-Komplexe an Magnetkügelchen befestigt und danach aus der Reaktion entfernt wurden. Trotz dieses umfangreichen Aufwands zeigten sich deutliche Signale nur für zwei der sieben Zielmoleküle. Bei den übrigen führte das Zufügen des Targets nicht zu zusätzlicher Auslöser-DNA in Lösung, was darauf hindeutet, dass entweder die Aptamere nicht wie behauptet banden oder die Bindung nicht die erwartete Formänderung und Freisetzung auslöste.
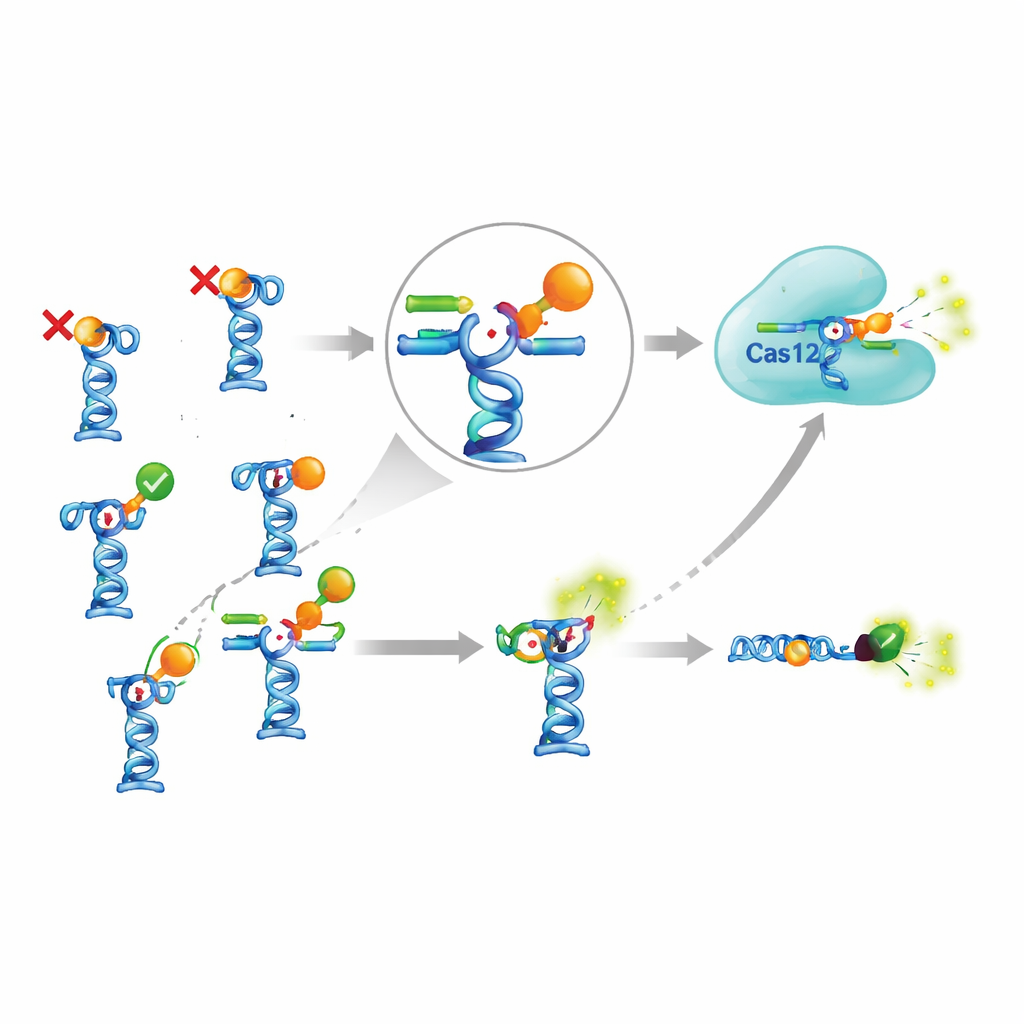
Lohnt sich der komplizierte Aufbau?
Um zu beurteilen, ob der CRISPR-Zusatz wirklich einen Mehrwert bringt, verglichen die Autoren ihn mit einem einfacheren Aptamer-Test, der Cas12a ganz weglässt. In diesem einfacheren Design trägt das Aptamer einen Fluoreszenzfarbstoff und sein Gegenstrang eine Lichtlöschgruppe; wenn der Gegenstrang durch das Zielmolekül verdrängt wird, steigt die Fluoreszenz direkt an. Für eines der wenigen funktionierenden Ziele, das Antimalariamittel Piperaquin, detektierte die CRISPR-basierte Version geringfügig niedrigere Konzentrationen als der einfache Test, jedoch nur um den Faktor zwei bis drei. Um diesen bescheidenen Gewinn zu erreichen, waren zusätzliche Enzyme, mehr Reagenzien, längere Protokolle und mehr Optimierung erforderlich. Gleichzeitig konnten einige zuvor veröffentlichte aptamerbasierte Sensoren — etwa für ein verbreitetes Algen-Toxin und das Insektizid Fipronil — überhaupt nicht reproduziert werden, selbst wenn die Autoren die berichteten Bedingungen genau befolgten und eine unabhängige Methode zur Bindungsprüfung einsetzten.
Was das für zukünftige Schnelltests bedeutet
Die Studie kommt zu dem Schluss, dass das Cas12a-Fluoreszenzsystem an sich zwar leistungsfähig ist, die kombinierte Aptamer–CRISPR-Sensorstrategie jedoch fragil bleibt. Ihr Erfolg hängt davon ab, Aptamere zu finden, die nicht nur an ihre Ziele binden, sondern auch zuverlässig den Auslöser-DNA freigeben — eine anspruchsvolle Voraussetzung, die viele veröffentlichte Aptamere offenbar nicht erfüllen. Für den Moment sollten Forschende und anwendungsorientierte Labore Plug-and-Play-Versprechen mit Vorsicht behandeln, in gründliche Validierung der Aptamer-Leistung investieren und abwägen, ob einfachere Aptamer-Tests oder etablierte Methoden wie Massenspektrometrie ihren Bedürfnissen nicht besser entsprechen. CRISPR-basierte Aptasensoren bleiben ein interessantes Werkzeug, sind aber noch nicht die universelle Lösung zur Detektion kleiner Moleküle, als die sie mitunter beworben wurden.
Zitation: Brandenberg, O.F., Janssen, E.ML. & Schubert, O.T. A critical assessment of aptamer and CRISPR-Cas12a-based biosensors for small molecule detection. npj Biosensing 3, 28 (2026). https://doi.org/10.1038/s44328-026-00089-8
Schlüsselwörter: Aptamer-Biosensoren, CRISPR-Cas12a-Detektion, Detektion kleiner Moleküle, Umweltkontaminanten, Fluoreszenz-Assays