Clear Sky Science · sv
En kritisk granskning av aptamer- och CRISPR‑Cas12a‑baserade biosensorer för detektion av små molekyler
Varför små föroreningar och snabba tester spelar roll
Från dricksvatten och floder till maten på våra tallrikar och de läkemedel vi tar—otäcka mängder små molekyler rör sig genom vår miljö och våra kroppar. Vissa är livräddande läkemedel; andra är giftiga föroreningar. Att mäta dessa föreningar kräver ofta otympliga och kostsamma instrument som är svåra att ta med ut i fält eller till en liten klinik. Denna artikel undersöker ett lovande alternativ: kompakta biokemiska tester som använder designerade DNA‑strängar och CRISPR‑enzymer för att omvandla närvaron av små molekyler till en tydlig ljussignal. Författarna ville se hur väl denna mycket hypade metod faktiskt fungerar i praktiken.
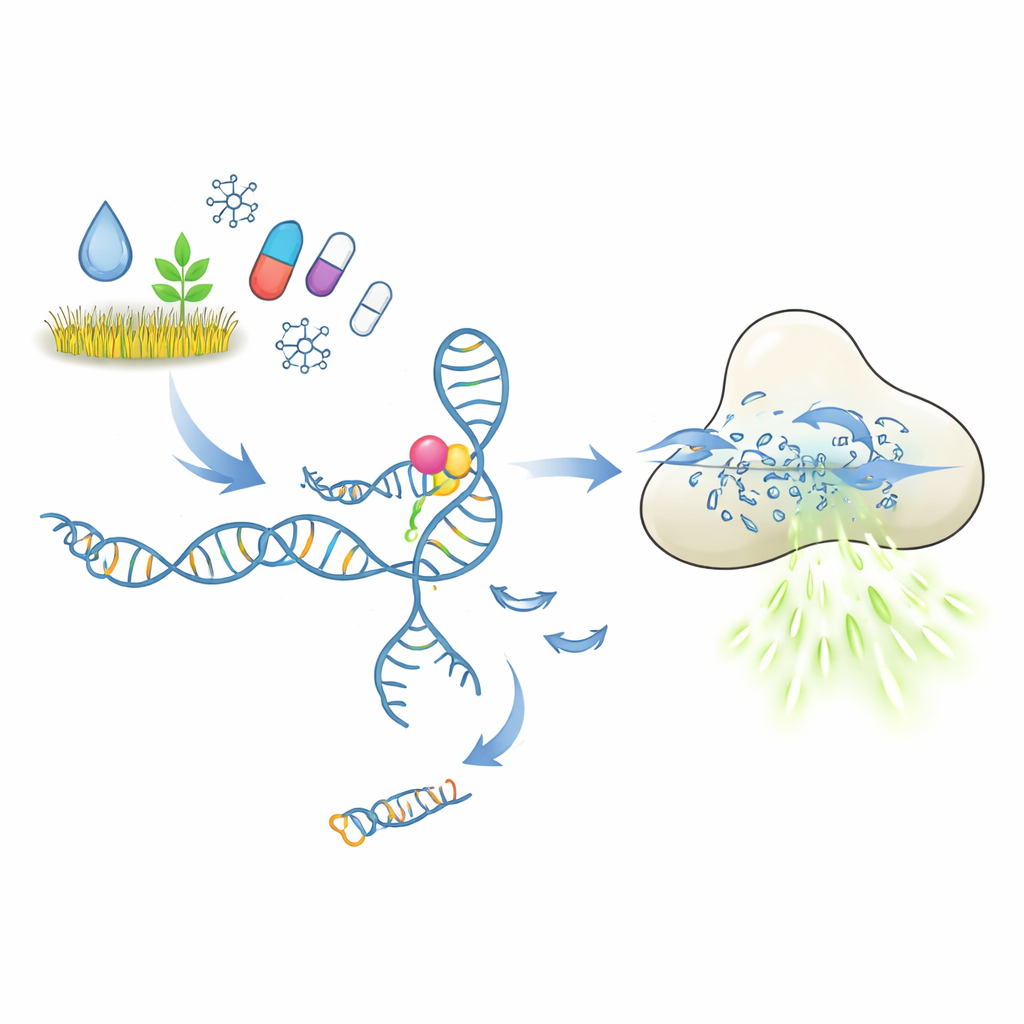
Hur ett molekylärt lås‑ och nyckeltest ska fungera
I centrum för dessa tester står aptamerer, korta DNA‑ eller RNA‑sekvenser som viks till former som kan binda ett valt mål, ungefär som antikroppar. I upplägget som undersöks här håller en aptamer fast vid en kort DNA‑bit som fungerar som en trigger. När målföroreningen eller läkemedlet binder förväntas aptamern ändra form och släppa denna trigger. Det frigjorda DNA:t aktiverar då CRISPR‑Cas12a‑enzymet, som uppträder som en molekylär dokumentförstörare för enkelsträngat DNA. Genom att ge Cas12a många korta DNA‑reportrar märkta med ett fluorescerande färgämne ger varje klipp mer ljus. I princip bör en mycket liten mängd målmolekyl därmed kunna omvandlas till en stark, lättmätt fluorescenssignal.
Att pröva CRISPR‑baserade sensorn under realistiska förhållanden
Forskarna angrep problemet som noggranna mekaniker som testar en ny motor. Först fininställde de Cas12a‑reaktionen: val av bästa buffert, metalljoner, enzymmängd och reportrdesign för att få starka och tillförlitliga ljussignaler när trigger‑DNA var närvarande. Under optimerade förhållanden kunde Cas12a upptäcka extremt låga nivåer av trigger‑DNA, ner till biljon‑dels mol, och gjorde det reproducerbart. Detta bekräftade att signaleringsmaskineriet—testets "förstärkardel"—i sig var robustt och känsligt.
Var designen börjar brista
Den verkliga utmaningen uppstod när de kopplade denna känsliga förstärkare till verkliga aptamerer från vetenskaplig litteratur. Teamet valde nio aptamerer som rapporterats känna igen sju olika små molekyler, inklusive bekämpningsmedel, antibiotika, ett levergift från alger och antimalariamedel. I teorin skulle dessa aptamerer släppa trigger‑DNA när de mötte sina mål. Författarna justerade noggrant hur starkt trigger‑DNA satt fast i varje aptamer, testade olika temperaturer, inkubationstider och buffertförhållanden, och prövade till och med en mer komplex version där aptamerkomplexen var bundna till magnetiska kulor och separerades från reaktionen i efterhand. Trots denna omfattande ansträngning framträdde tydliga signaler bara för två av de sju målen. För de övriga ledde tillsats av målet inte till mer trigger‑DNA i lösning, vilket tyder på att antingen aptamererna inte band som påståtts, eller att bindningen inte orsakade den förväntade formändringen och frisättningen.
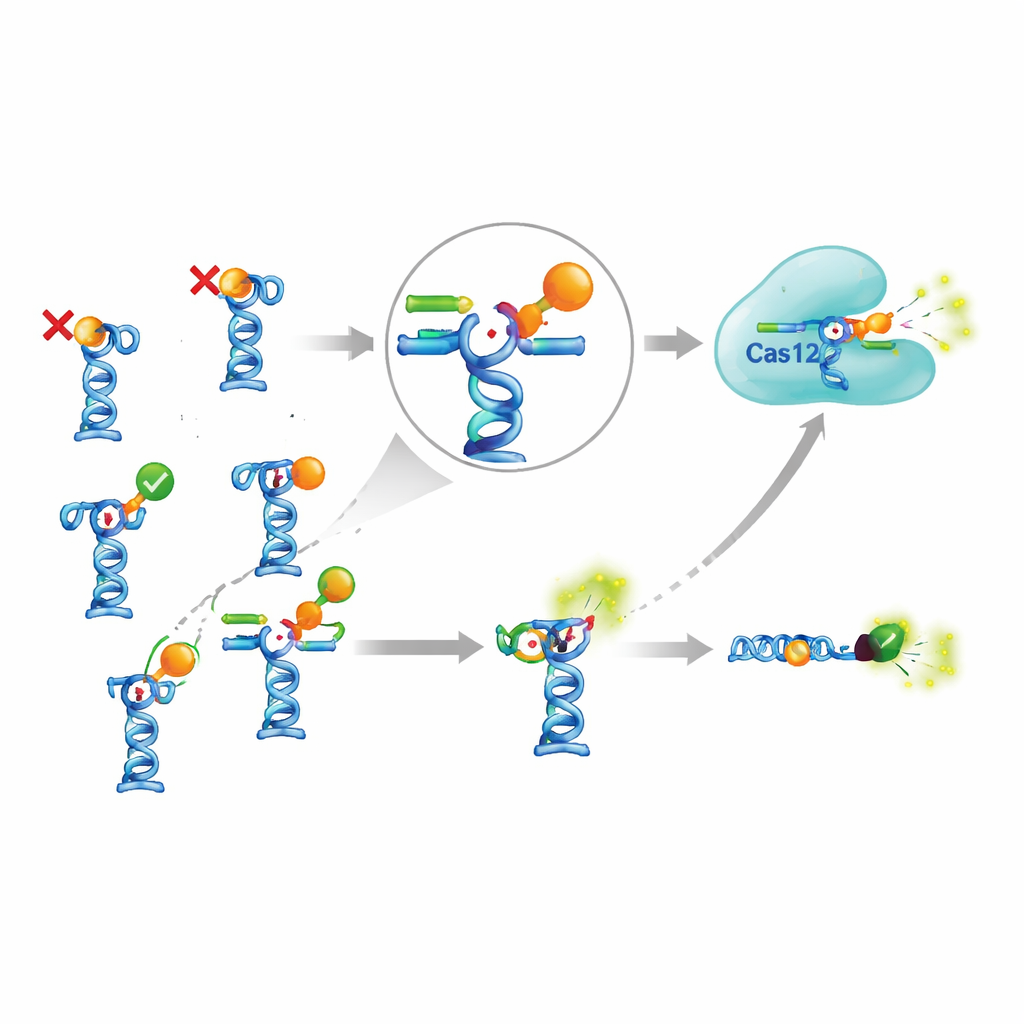
Är den komplicerade uppsättningen värd besväret?
För att bedöma om CRISPR‑tillägget verkligen lönar sig jämförde författarna det med ett enklare aptamer‑test som hoppar över Cas12a helt. I denna enklare design bär aptamern ett fluorescerande färgämne och dess komplementära sträng en dämpande grupp; när komplementsträngen trängs undan av målmolekylen ökar fluorescensen direkt. För ett av de få fungerande målen, antimalariamedlet piperaquin, detekterade den CRISPR‑baserade versionen något lägre koncentrationer än det enkla testet, men bara med en faktor på två till tre. För att uppnå denna blygsamma förbättring krävdes extra enzymer, fler reagenser, längre protokoll och mer optimering. Samtidigt kunde vissa tidigare publicerade aptamerbaserade sensorer—for exempel för ett vanligt alggift och insekticiden fipronil—inte reproduceras alls, även när författarna följde rapporterade förhållanden noggrant och använde en oberoende metod för att testa bindning.
Vad detta betyder för framtida snabba tester
Studien slutsatser är att medan Cas12a‑fluorescenssystemet i sig är kraftfullt, är den övergripande aptamer–CRISPR‑sensorstrategin skör. Dess framgång hänger på aptamerer som inte bara binder sina mål utan också pålitligt släpper trigger‑DNA—ett krävande villkor som många publicerade aptamerer faktiskt inte uppfyller. För närvarande bör forskare och tillämpningsinriktade laboratorier förhålla sig försiktigt till plug‑and‑play‑påståenden, satsa på grundlig validering av aptameregenskaper och noga överväga om enklare aptamer‑tester eller etablerade metoder som massespektrometri bättre uppfyller deras behov. CRISPR‑baserade aptasensorer förblir ett intressant verktyg, men ännu inte den universella lösningen för detektion av små molekyler som de ibland framställts som.
Citering: Brandenberg, O.F., Janssen, E.ML. & Schubert, O.T. A critical assessment of aptamer and CRISPR-Cas12a-based biosensors for small molecule detection. npj Biosensing 3, 28 (2026). https://doi.org/10.1038/s44328-026-00089-8
Nyckelord: aptamer‑biosensorer, CRISPR‑Cas12a‑detektion, detektion av små molekyler, miljökontaminanter, fluorescensanalyser