Clear Sky Science · pt
Uma avaliação crítica de biossensores baseados em aptâmeros e CRISPR-Cas12a para detecção de pequenas moléculas
Por que poluentes minúsculos e testes rápidos importam
Da água potável e rios aos alimentos em nossos pratos e aos medicamentos que tomamos, inúmeras pequenas moléculas circulam pelo ambiente e por nossos corpos. Algumas são fármacos que salvam vidas; outras são contaminantes tóxicos. Medir esses compostos normalmente exige instrumentos volumosos e caros, difíceis de levar a campo ou a uma pequena clínica. Este artigo examina uma alternativa promissora: testes bioquímicos compactos que usam fitas de DNA projetadas e enzimas CRISPR para converter a presença de moléculas minúsculas em um sinal luminoso. Os autores investigam quão bem essa abordagem muito promovida funciona, na prática.
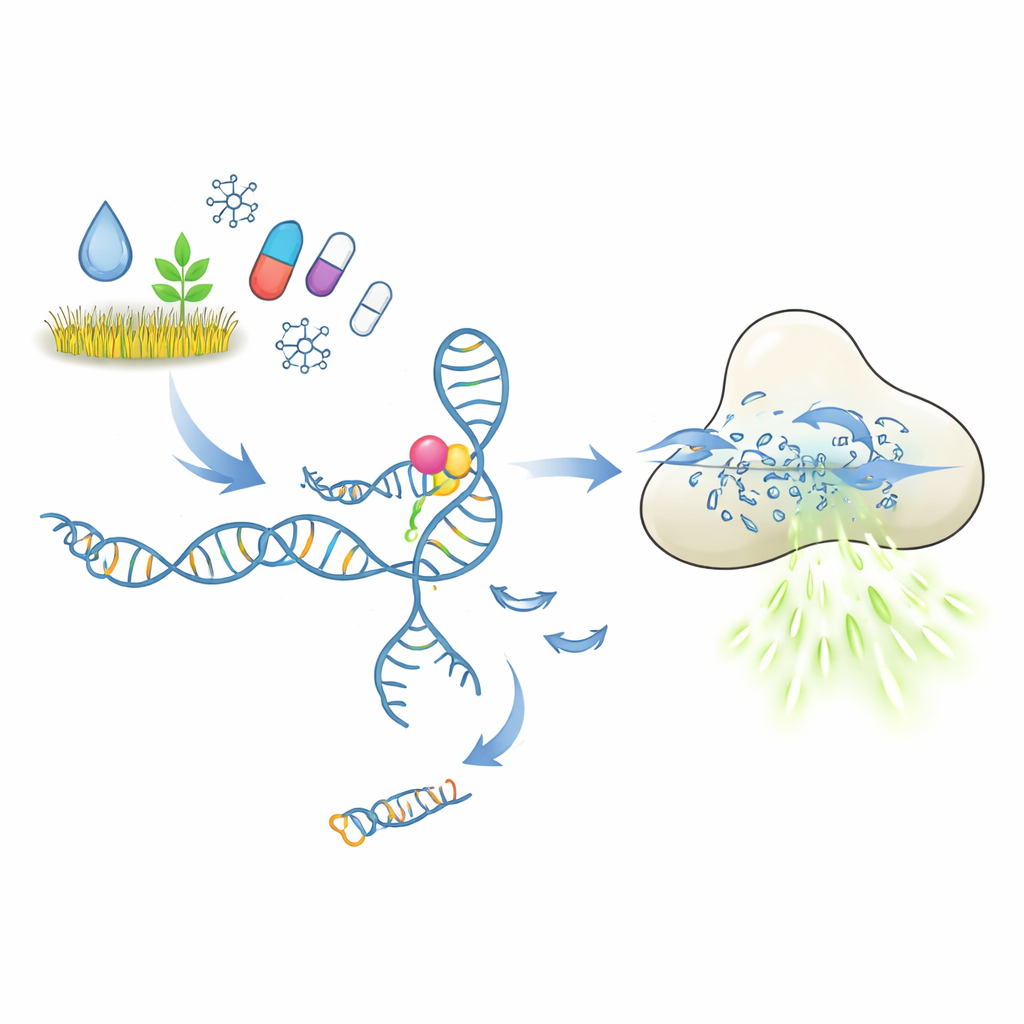
Como um teste molecular de chave-fechadura deveria funcionar
No cerne desses testes estão os aptâmeros, pequenas sequências de DNA ou RNA que se dobram em formas capazes de se ligar a um alvo escolhido, de modo semelhante a anticorpos. Na configuração explorada aqui, um aptâmero segura um pequeno pedaço de DNA que atua como gatilho. Quando o poluente ou fármaco alvo se liga, espera-se que o aptâmero mude de conformação e libere esse gatilho. O DNA liberado então ativa a enzima CRISPR-Cas12a, que se comporta como um fragmentador molecular para DNA de fita simples. Fornecendo ao Cas12a muitos repórteres curtos de DNA marcados com um corante fluorescente, cada clivagem gera mais luz. Em princípio, uma quantidade ínfima de molécula alvo deveria, assim, ser convertida em um forte sinal de fluorescência fácil de medir.
Colocando o sensor baseado em CRISPR à prova
Os pesquisadores abordaram o problema como mecânicos cuidadosos testando um novo motor. Primeiro, ajustaram a reação de Cas12a em si: escolheram o melhor tampão, íons metálicos, quantidade de enzima e o desenho dos repórteres para obter sinais de luz fortes e confiáveis quando o DNA gatilho estava presente. Em condições otimizadas, o Cas12a pôde detectar níveis extremamente baixos de DNA gatilho, até trilionésimos de mole, e o fez de forma reprodutível. Isso confirmou que a maquinaria de sinalização — a parte "amplificadora" do teste — era robusta e sensível por si só.
Onde o projeto começa a falhar
O desafio real surgiu quando conectaram esse amplificador sensível a aptâmeros reais da literatura científica. A equipe selecionou nove aptâmeros que foram relatados como capazes de reconhecer sete pequenas moléculas diferentes, incluindo pesticidas, antibióticos, uma toxina hepática de algas e drogas antimaláricas. Em teoria, esses aptâmeros deveriam liberar o DNA gatilho ao encontrarem seus alvos. Os autores ajustaram cuidadosamente a força com que o DNA gatilho se prendia a cada aptâmero, testaram diferentes temperaturas, tempos de incubação e condições de tampão, e até tentaram uma versão mais complexa em que os complexos de aptâmero estavam presos a esferas magnéticas e eram separados da reação em seguida. Apesar desse esforço extensivo, sinais claros apareceram para apenas dois dos sete alvos. Para os demais, a adição do alvo não levou a um aumento de DNA gatilho em solução, sugerindo que ou os aptâmeros não se ligavam como afirmado, ou a ligação não causava a mudança conformacional esperada e a liberação.
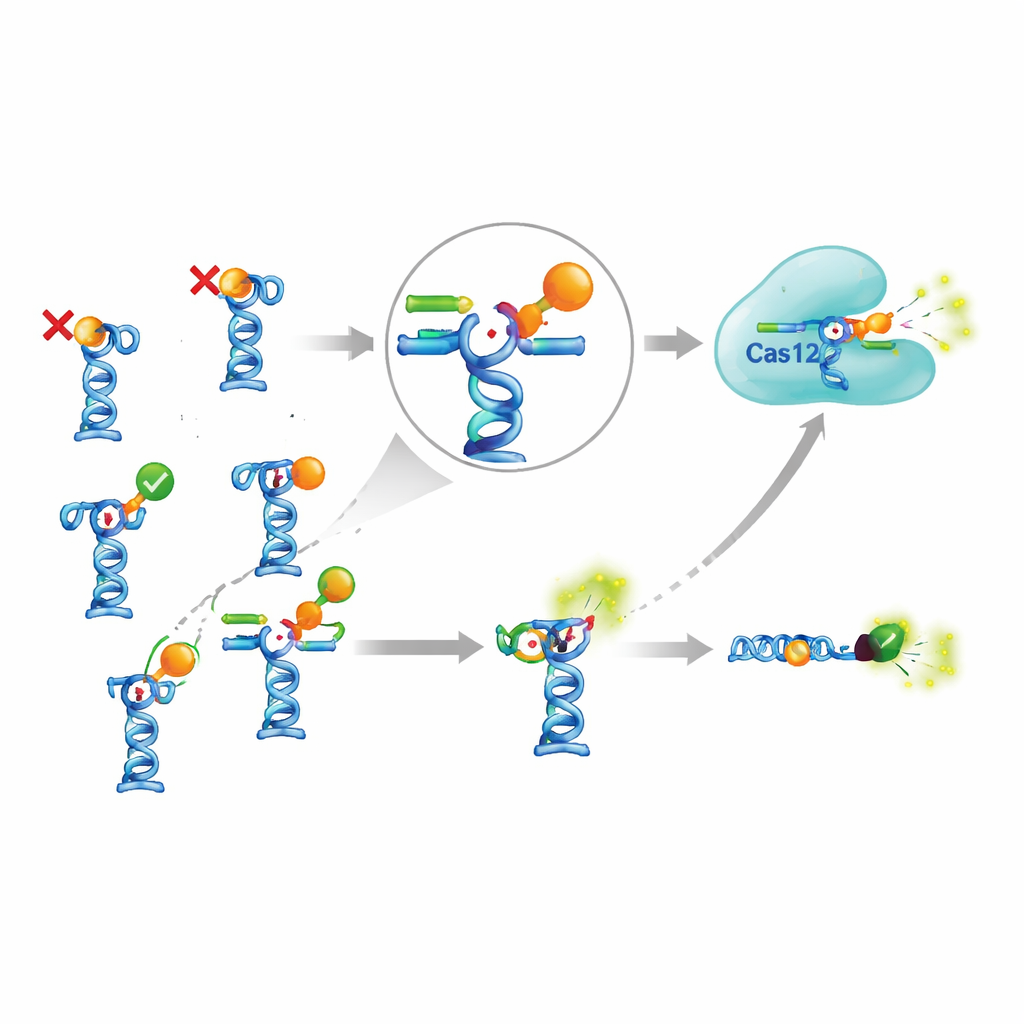
O conjunto complicado vale o esforço?
Para avaliar se o complemento CRISPR realmente compensa, os autores o compararam com um teste de aptâmero mais simples que dispensa o Cas12a por completo. Neste desenho mais simples, o aptâmero carrega um corante fluorescente e sua fita parceira carrega um grupo quencher; quando a fita parceira é deslocada pela molécula alvo, a fluorescência aumenta diretamente. Para um dos poucos alvos que funcionaram, o antimalárico piperaquina, a versão baseada em CRISPR detectou concentrações ligeiramente menores do que o teste simples, mas apenas por um fator de dois a três. Alcançar esse ganho modesto exigiu enzimas extras, mais reagentes, protocolos mais longos e mais otimização. Ao mesmo tempo, alguns sensores baseados em aptâmeros publicados anteriormente — por exemplo, para uma toxina algal comum e para o inseticida fipronil — não puderam ser reproduzidos de forma alguma, mesmo quando os autores seguiram rigorosamente as condições relatadas e usaram um método independente para testar a ligação.
O que isso significa para futuros testes rápidos
O estudo conclui que, embora o sistema de fluorescência com Cas12a seja poderoso, a estratégia completa de sensor aptâmero–CRISPR é frágil. Seu sucesso depende de aptâmeros que não apenas se liguem aos alvos, mas que também liberem de forma confiável o DNA gatilho — um requisito exigente que muitos aptâmeros publicados, na prática, não atendem. Por enquanto, pesquisadores e laboratórios voltados à aplicação devem tratar reivindicações de "plug-and-play" com cautela, investir em validação rigorosa do desempenho dos aptâmeros e ponderar se testes de aptâmero mais simples ou métodos estabelecidos como espectrometria de massas podem atender melhor às suas necessidades. Aptasensores baseados em CRISPR continuam sendo uma ferramenta intrigante, mas ainda não a solução universal para detecção de pequenas moléculas que às vezes lhes é atribuída.
Citação: Brandenberg, O.F., Janssen, E.ML. & Schubert, O.T. A critical assessment of aptamer and CRISPR-Cas12a-based biosensors for small molecule detection. npj Biosensing 3, 28 (2026). https://doi.org/10.1038/s44328-026-00089-8
Palavras-chave: biossensores com aptâmeros, detecção CRISPR-Cas12a, detecção de pequenas moléculas, contaminantes ambientais, ensaios de fluorescência