Clear Sky Science · it
Una valutazione critica dei biosensori a base di aptamer e CRISPR-Cas12a per il rilevamento di piccole molecole
Perché i piccoli inquinanti e i test rapidi sono importanti
Dall’acqua potabile e dai fiumi agli alimenti nei nostri piatti e ai farmaci che assumiamo, innumerevoli piccole molecole attraversano il nostro ambiente e i nostri organismi. Alcune sono farmaci salvavita; altre sono contaminanti tossici. Misurare questi composti di solito richiede strumenti ingombranti e costosi, difficili da portare sul campo o in una piccola clinica. Questo articolo esamina un’alternativa promettente: test biochimici compatti che utilizzano filamenti di DNA progettati e enzimi CRISPR per trasformare la presenza di piccole molecole in un segnale luminoso. Gli autori hanno cercato di capire quanto bene questo approccio molto pubblicizzato funzioni nella pratica.
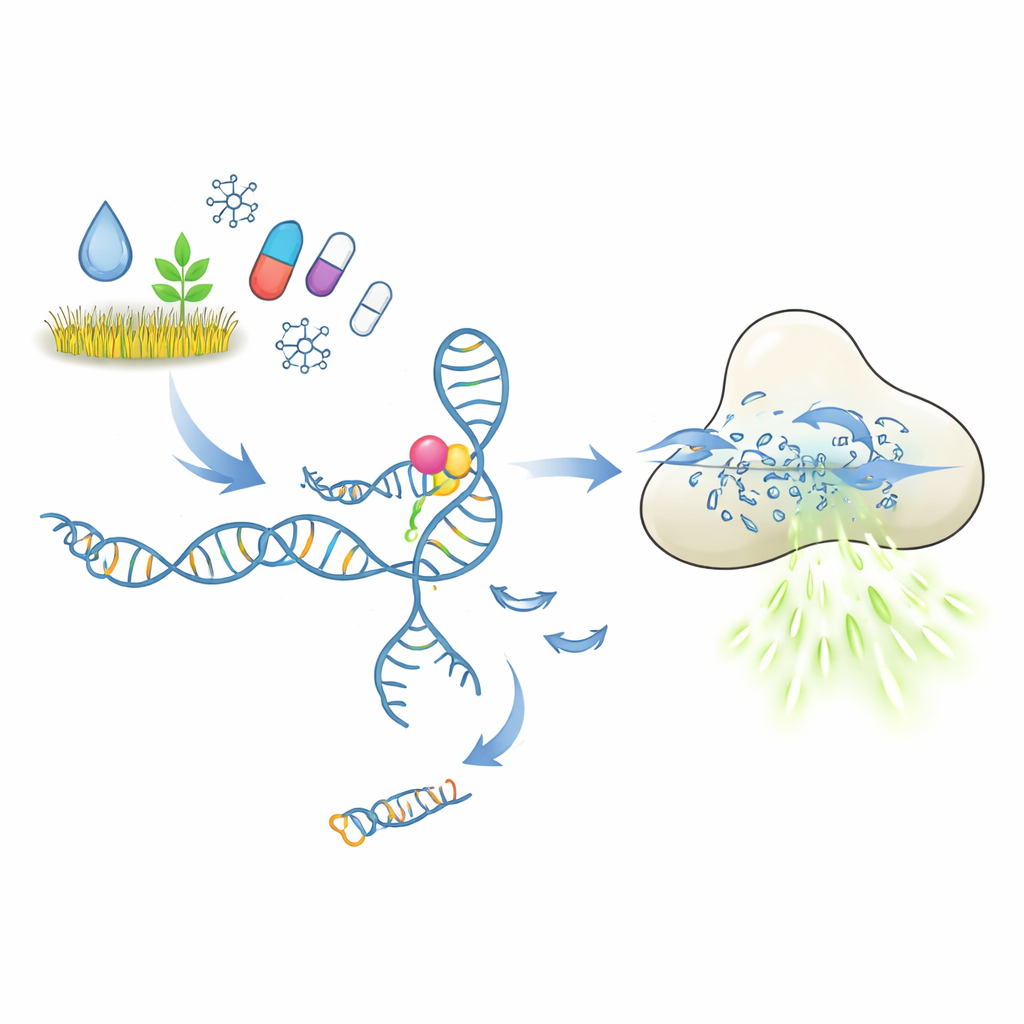
Come dovrebbe funzionare un test molecolare a chiave e serratura
Al centro di questi test ci sono gli aptameri, brevi frammenti di DNA o RNA che si ripiegano in forme capaci di legarsi a un bersaglio scelto, in modo simile agli anticorpi. Nella configurazione qui esaminata, un aptamero trattiene un breve frammento di DNA che funge da innesco. Quando il pesticida o il farmaco bersaglio si lega, l’aptamero dovrebbe cambiare forma e rilasciare questo innesco. Il DNA liberato attiva quindi l’enzima CRISPR-Cas12a, che si comporta come un trituratore molecolare per il DNA a singolo filamento. Fornendo a Cas12a molti brevi reporter di DNA con un colorante fluorescente, ogni taglio produce più luce. In linea di principio, una quantità minima di molecola bersaglio dovrebbe così essere convertita in un forte segnale di fluorescenza facile da misurare.
Mettere alla prova il sensore basato su CRISPR
I ricercatori hanno affrontato il problema come meccanici attenti che collaudano un nuovo motore. Prima di tutto hanno ottimizzato la reazione di Cas12a stessa: scegliendo il miglior tampone, gli ioni metallici, la quantità d’enzima e il disegno dei reporter per ottenere segnali luminosi forti e affidabili quando il DNA innesco era presente. In condizioni ottimizzate, Cas12a ha potuto rilevare livelli estremamente bassi di DNA innesco, fino a trilionesimi di mole, e l’ha fatto in modo riproducibile. Questo ha confermato che il meccanismo di segnalazione — la parte “amplificatrice” del test — era robusto e sensibile di per sé.
Dove il progetto comincia a fallire
La vera sfida è emersa quando hanno collegato questo amplificatore sensibile ad aptameri reali presenti in letteratura. Il team ha selezionato nove aptameri che erano stati segnalati come capaci di riconoscere sette diverse piccole molecole, compresi pesticidi, antibiotici, una tossina epatica prodotta da alghe e farmaci antimalarici. In teoria, questi aptameri dovrebbero rilasciare il DNA innesco quando incontrano i loro bersagli. Gli autori hanno regolato con cura quanto fortemente il DNA innesco si legava a ogni aptamero, hanno testato diverse temperature, tempi di incubazione e condizioni di tampone, e hanno persino provato una versione più complessa in cui i complessi aptamero-erano attaccati a perline magnetiche e separati dalla reazione in seguito. Nonostante questo ampio sforzo, segnali chiari sono comparsi solo per due dei sette bersagli. Per gli altri, l’aggiunta del bersaglio non ha portato a un aumento di DNA innesco in soluzione, suggerendo che o gli aptameri non si legavano come dichiarato, o il legame non provocava il cambiamento conformazionale e il rilascio attesi.
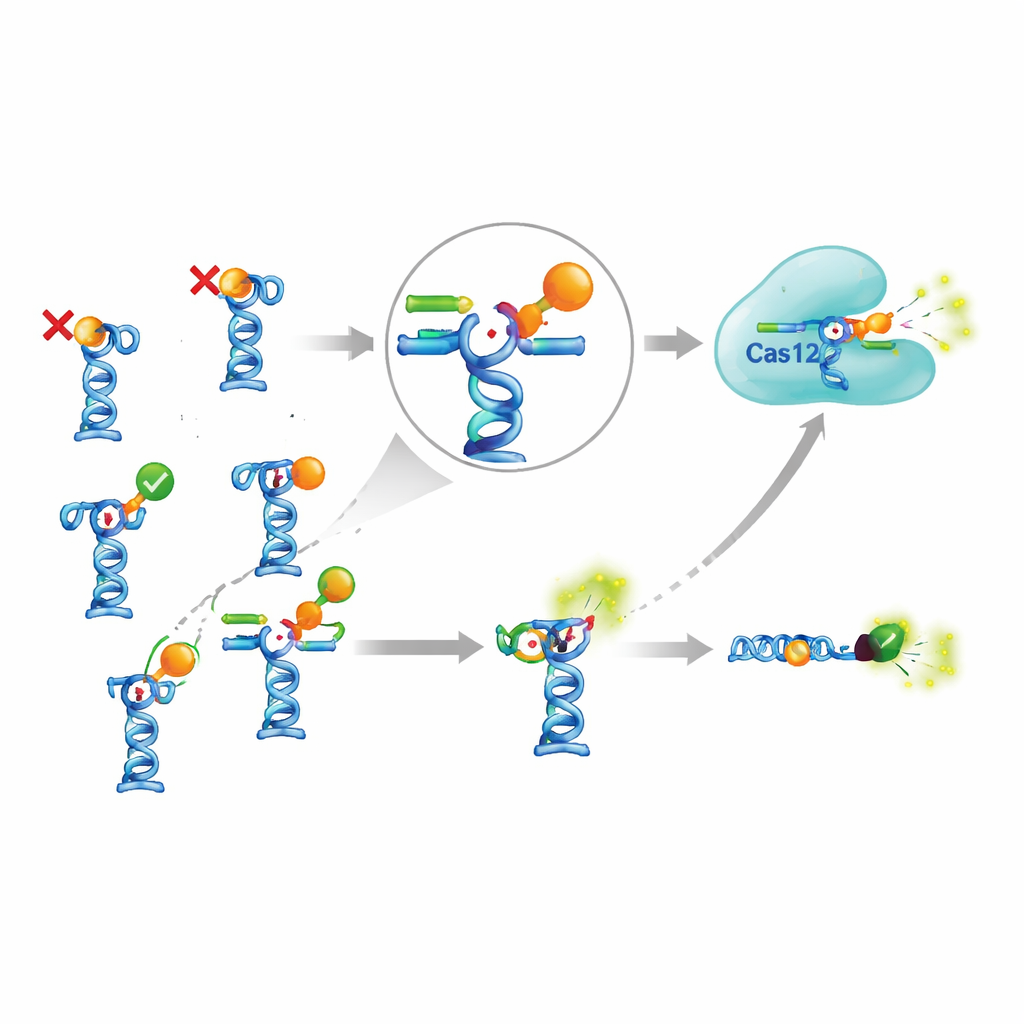
Vale la pena l’assetto complicato?
Per giudicare se l’aggiunta di CRISPR valga davvero lo sforzo, gli autori l’hanno confrontata con un test aptamero più semplice che evita completamente Cas12a. In questo design più semplice, l’aptamero porta un colorante fluorescente e la sua catena partner un gruppo che estingue la luce; quando la catena partner viene spostata dal bersaglio, la fluorescenza aumenta direttamente. Per uno dei pochi bersagli funzionanti, il antimalarico piperaquina, la versione basata su CRISPR ha rilevato concentrazioni leggermente inferiori rispetto al test semplice, ma solo di un fattore di due o tre. Ottenere questo guadagno modesto ha richiesto enzimi aggiuntivi, più reagenti, protocolli più lunghi e maggiore ottimizzazione. Allo stesso tempo, alcuni sensori a base di aptamer precedentemente pubblicati — per esempio per una comune tossina algale e per l’insetticida fipronil — non sono stati riproducibili affatto, anche quando gli autori hanno seguito attentamente le condizioni riportate e hanno utilizzato un metodo indipendente per testare il legame.
Cosa significa per i futuri test rapidi
Lo studio conclude che, sebbene il sistema di fluorescenza Cas12a sia in sé potente, la strategia complessiva aptamero–CRISPR è fragile. Il suo successo dipende da aptameri che non solo legano i loro bersagli ma rilasciano anche in modo affidabile il DNA innesco — un requisito esigente che molti aptameri pubblicati in realtà non soddisfano. Per il momento, i ricercatori e i laboratori orientati alle applicazioni dovrebbero trattare con cautela le affermazioni plug-and-play, investire in una convalida approfondita delle prestazioni degli aptameri e valutare se test aptamero più semplici o metodi consolidati come la spettrometria di massa possano servire meglio alle loro esigenze. Gli aptasensori basati su CRISPR rimangono uno strumento interessante, ma non ancora la soluzione universale per il rilevamento di piccole molecole che talvolta sono stati pubblicizzati come essere.
Citazione: Brandenberg, O.F., Janssen, E.ML. & Schubert, O.T. A critical assessment of aptamer and CRISPR-Cas12a-based biosensors for small molecule detection. npj Biosensing 3, 28 (2026). https://doi.org/10.1038/s44328-026-00089-8
Parole chiave: biosensori a aptamer, rilevamento CRISPR-Cas12a, rilevamento di piccole molecole, contaminanti ambientali, saggi di fluorescenza