Clear Sky Science · ar
تقييم نقدي لأجهزة الاستشعار البيولوجية المعتمدة على الأبتاميرات وCRISPR-Cas12a لاكتشاف الجزيئات الصغيرة
لماذا تهم الملوثات الصغيرة والاختبارات السريعة
من مياه الشرب والأنهار إلى الطعام على أطباقنا والأدوية التي نأخذها، تنتقل عبر بيئتنا وأجسامنا جزيئات صغيرة لا حصر لها. بعضها أدوية منقذة للحياة؛ وبعضها الآخر ملوثات سامة. عادةً ما يتطلب قياس هذه المركبات أجهزة ثقيلة ومكلفة يصعب نقلها إلى الميدان أو إلى عيادة صغيرة. تفحص هذه الورقة بديلًا واعدًا: اختبارات بيوكيميائية مدمجة تستخدم سلاسل DNA مصممة وإنزيمات CRISPR لتحويل وجود جزيئات صغيرة إلى إشارة ضوئية واضحة. هدف المؤلفين كان تقييم مدى فعالية هذا النهج المروج له عمليًا.
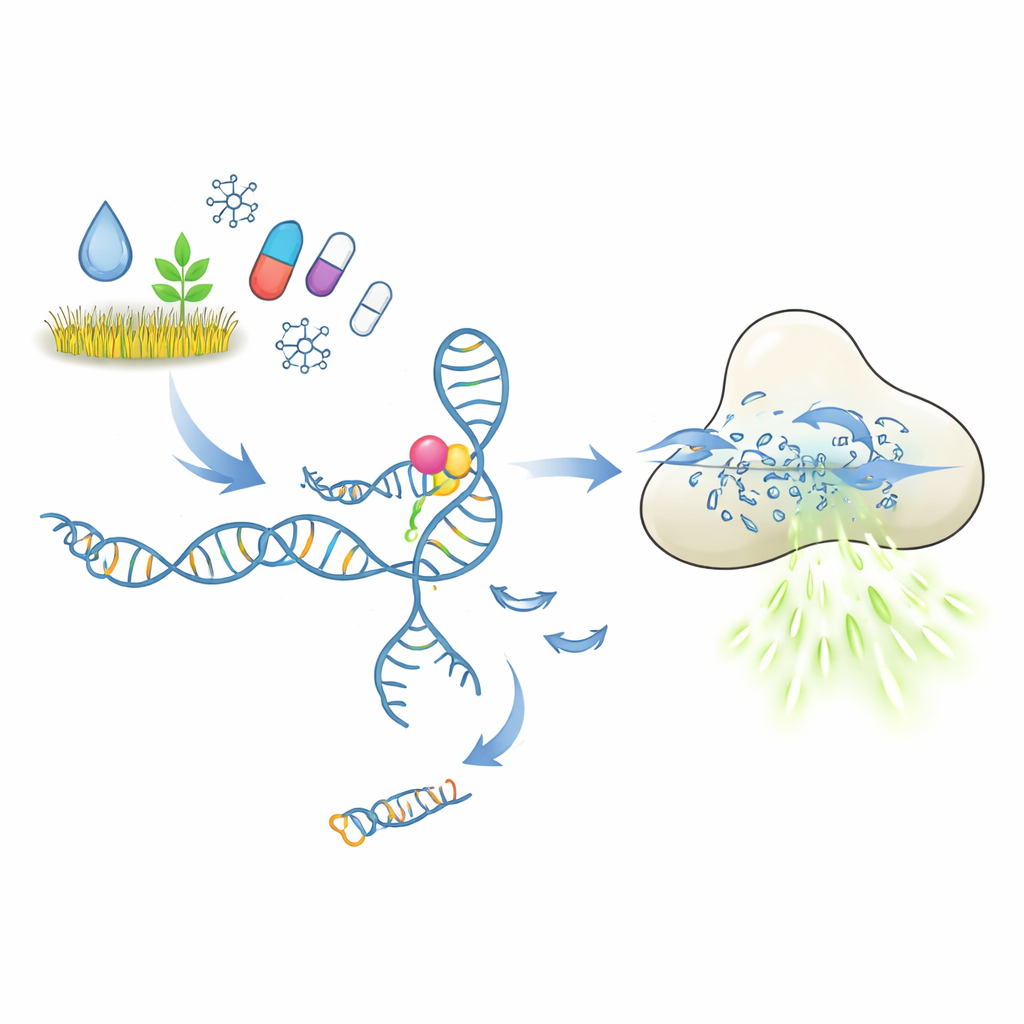
كيف من المفترض أن يعمل اختبار القفل والمفتاح الجزيئي
في قلب هذه الاختبارات توجد الأبتاميرات، وهي قطع قصيرة من DNA أو RNA تطوي نفسها إلى أشكال تستطيع الالتحام بهدف محدد، شبيهة بما تفعله الأجسام المضادة. في التصميم الذي استُكشف هنا، تمسك الأبتامير بقطعة قصيرة من الـDNA تعمل كمُحفّز. عندما يرتبط الملوث أو الدواء الهدف، من المتوقع أن يغير الأبتامير شكله ويطلق هذا المُحفّز. بعد ذلك يُفَعّل الـDNA الحر إنزيم CRISPR-Cas12a، الذي يتصرف كمَقطّع جزيئي للأحماض النووية أحادية السلسلة. بتوفير العديد من مراسِلي الـDNA القصير المحمّلين بصبغة فلورية، يؤدي كل قطع إلى مزيد من الضوء. نظريًا، يجب أن تُحوّل كمية صغيرة من جزيء الهدف إلى إشارة فلورية قوية وسهلة القياس.
عرض جهاز الاستشعار المعتمد على CRISPR للاختبار
اقترب الباحثون من المشكلة كما يفعل الميكانيكيون الحذرون عند اختبار محرك جديد. أولًا، ضبطوا تفاعل Cas12a نفسه: اختيار أفضل مخزن تفاعلي، أيونات المعادن، كمية الإنزيم، وتصميم المراسل للحصول على إشارات ضوئية قوية وموثوقة عند وجود DNA المُحفّز. في الشروط المحسنة، كان بإمكان Cas12a اكتشاف مستويات منخفضة جدًا من DNA المُحفّز، حتى تريليونات من المولات، وبشكل متكرر. هذا أكد أن آلية الإشارة — جزء "المكبر" في الاختبار — كانت متينة وحساسة بمفردها.
أين يبدأ التصميم في الفشل
الاختبار الحقيقي ظهر عندما ربطوا هذا المُكبر الحساس بأبتاميرات فعلية من الأدبيات العلمية. اختار الفريق تسعة أبتاميرات أبلغ عنها للتعرف على سبعة جزيئات صغيرة مختلفة، بما في ذلك مبيدات حشرية، مضادات حيوية، سم كبدي من الطحالب، وأدوية مضادة للملاريا. نظريًا، كان يجب على هذه الأبتاميرات أن تطلق DNA المُحفّز عند مواجهة أهدافها. عدّل المؤلفون بعناية مدى التلاصق بين DNA المُحفّز وكل أبتامير، اختبروا درجات حرارة ومُدَد احتضان وظروف مخازن مختلفة، وجربوا حتى نسخة أكثر تعقيدًا حيث رُبِطت مجمعات الأبتامير بخرزات مغناطيسية وفُصلت عن التفاعل لاحقًا. على الرغم من هذا الجهد الواسع، ظهرت إشارات واضحة فقط لاثنين من بين السبعة أهداف. بالنسبة للبقية، لم تؤدِ إضافة الهدف إلى زيادة DNA المُحفّز في المحلول، ما يوحي إما بأن الأبتاميرات لم ترتبط كما زُعم، أو أن الارتباط لم يسبب تغيير الشكل المتوقع وإطلاق المُحفّز.
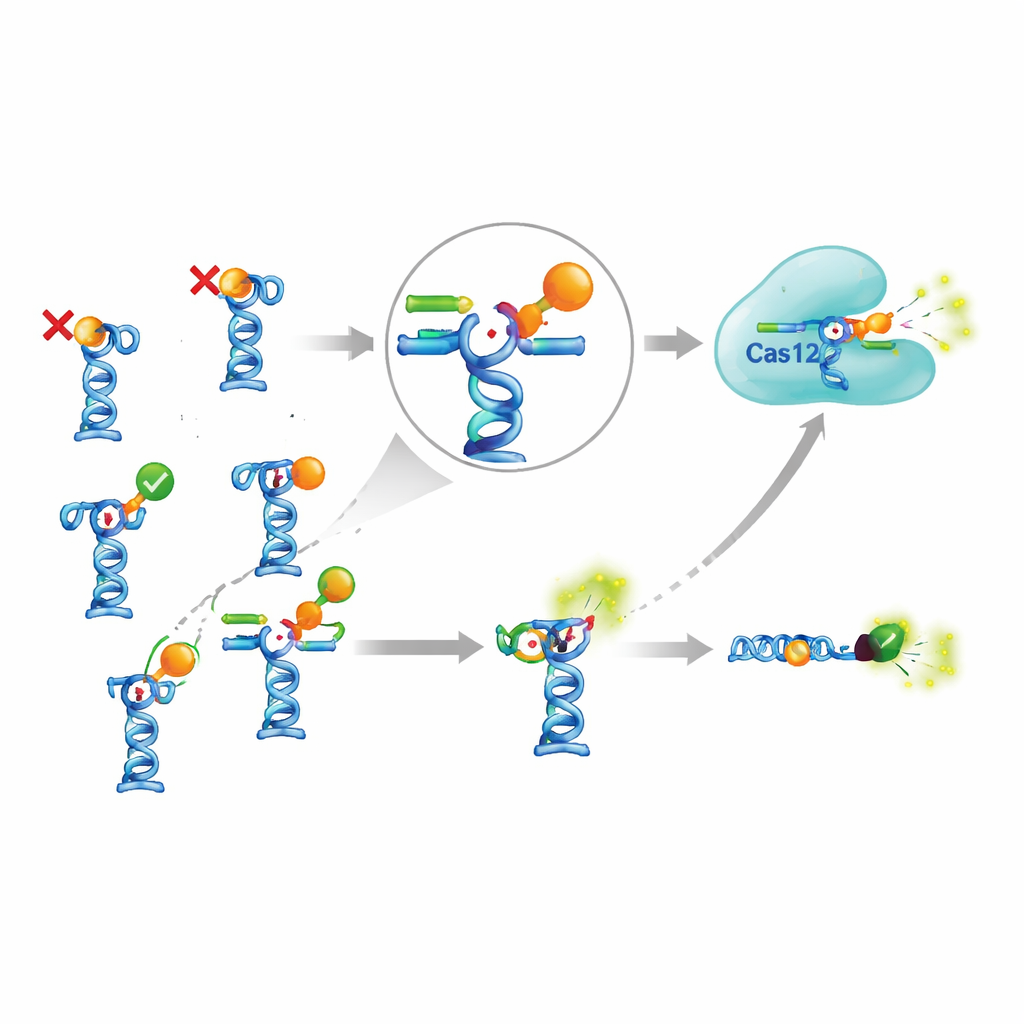
هل الإعداد المعقّد يستحق العناء؟
للحكم ما إذا كانت الإضافة المعتمدة على CRISPR تعود بالفائدة فعلاً، قارن المؤلفون بينها وبين اختبار أبتمير أبسط يتخطى Cas12a تمامًا. في هذا التصميم الأبسط، يحمل الأبتامير صبغة فلورية وتحمل السلسلة الشريكة مجموعة مطمئنة للضوء؛ عندما تُزاح السلسلة الشريكة بواسطة جزيء الهدف، تزداد الفلورية مباشرة. بالنسبة لأحد الأهداف القليلة العاملة، وهو مضاد الملاريا بيبيراكين، اكتشف الإصدار المعتمد على CRISPR تركيزات أقل قليلًا من الاختبار البسيط، لكن بفارق لا يتجاوز ببضعة أضعاف (من مرتين إلى ثلاث مرات). تحقيق هذه الزيادة المتواضعة تطلّب إنزيمات إضافية، كواشف أكثر، بروتوكولات أطول، ومزيدًا من الضبط. وفي الوقت نفسه، لم تتمكن بعض أجهزة الاستشعار القائمة على الأبتامير المنشورة سابقًا — على سبيل المثال، لتسونامي سم الطحالب الشائع والمبيد الحشري فيبرونيل — من أن تُستعاد على الإطلاق، حتى عندما اتبع المؤلفون الشروط المبلّغ عنها عن كثب واستخدموا طريقة مستقلة لاختبار الارتباط.
ماذا يعني هذا للاختبارات السريعة المستقبلية
تستنتج الدراسة أنه بينما يعد نظام الفلورية Cas12a نفسه قويًا، فإن استراتيجية جهاز الاستشعار الشامل أبتامير–CRISPR هشة. نجاحها يعتمد على أبتاميرات لا تكتفي بالارتباط بأهدافها فحسب، بل تترك أيضًا DNA المُحفّز بشكل موثوق — وهو مطلب صارم لا تلبيهه العديد من الأبتاميرات المنشورة في الواقع. في الوقت الراهن، ينبغي للباحثين والمختبرات الموجهة للتطبيق أن يتعاملوا بحذر مع ادعاءات "التوصيل والتشغيل"، وأن يستثمروا في التحقق الدقيق من أداء الأبتاميرات، وأن يوازنوا ما إذا كانت الاختبارات الأبسط للأبتامير أو الطرق الراسخة مثل التحليل الطيفي الكتلي قد تخدم احتياجاتهم بشكل أفضل. تظل أجهزة الأبتاسنسور المعتمدة على CRISPR أداة مثيرة، لكنها ليست بعد الحل الشامل لاكتشاف الجزيئات الصغيرة كما تم أحيانًا الترويج لها.
الاستشهاد: Brandenberg, O.F., Janssen, E.ML. & Schubert, O.T. A critical assessment of aptamer and CRISPR-Cas12a-based biosensors for small molecule detection. npj Biosensing 3, 28 (2026). https://doi.org/10.1038/s44328-026-00089-8
الكلمات المفتاحية: أجهزة استشعار الأبتامير, كشف CRISPR-Cas12a, استشعار الجزيئات الصغيرة, الملوثات البيئية, تحليلات الفلورية