Clear Sky Science · ru
Критическая оценка биосенсоров на основе аптамеров и CRISPR-Cas12a для обнаружения малых молекул
Почему важны мелкие загрязнители и быстрые тесты
От питьевой воды и рек до продуктов на наших тарелках и лекарств, которые мы принимаем, многочисленные малые молекулы циркулируют в окружающей среде и в наших телах. Некоторые из них — жизненно важные препараты; другие — токсичные загрязнители. Измерение этих соединений обычно требует громоздких и дорогих приборов, которые трудно взять с собой в поле или небольшую клинику. В этой статье рассматривается перспективная альтернатива: компактные биохимические тесты, использующие конструированные цепочки ДНК и ферменты CRISPR для преобразования присутствия малых молекул в яркий световой сигнал. Авторы стремились выяснить, насколько хорошо этот распиаренный подход работает на практике.
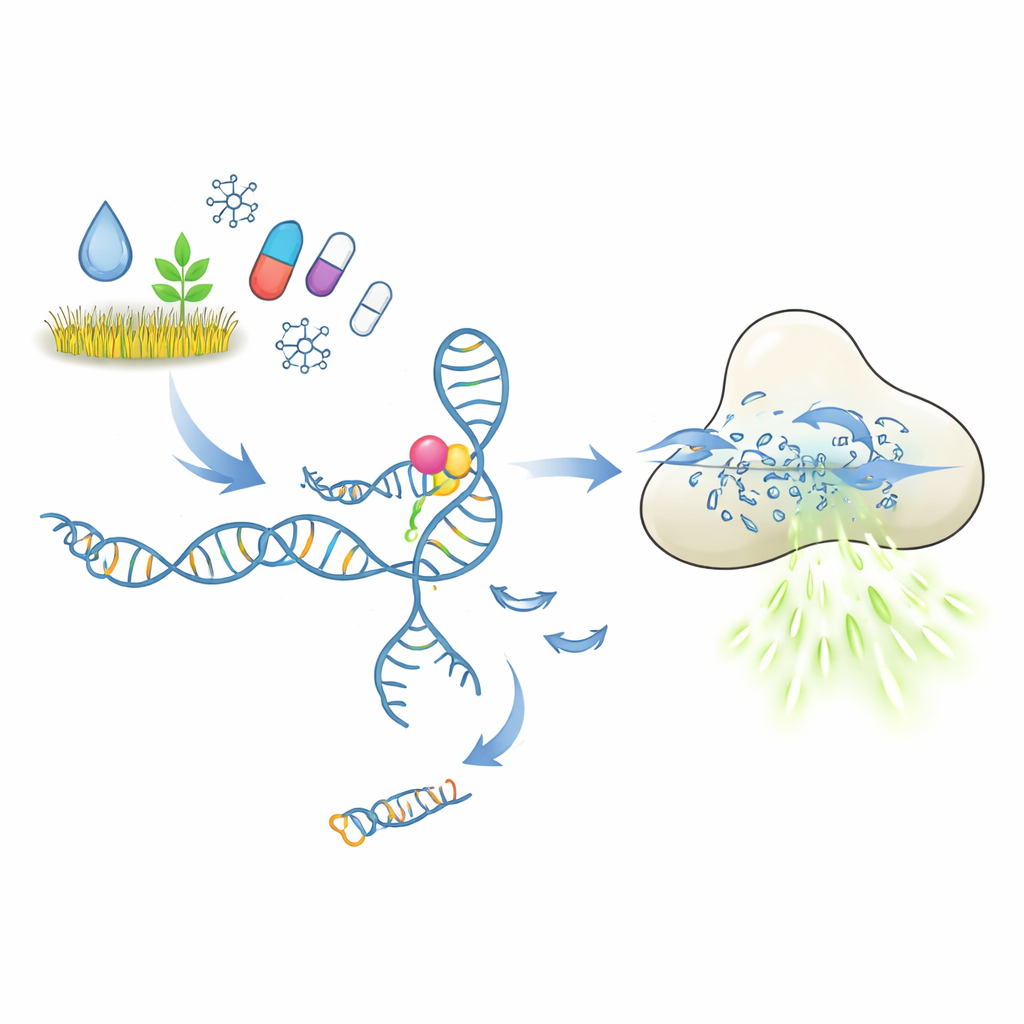
Как должен работать молекулярный тест «замок и ключ»
В основе этих тестов лежат аптамеры — короткие фрагменты ДНК или РНК, сворачивающиеся в формы, способные захватывать выбранную мишень, аналогично антителам. В рассматриваемой схеме аптамер держит короткую ДНК-стрижку, выступающую в роли триггера. Когда целевой загрязнитель или препарат связывается, аптамер должен изменить конформацию и высвободить этот триггер. Освобождённая ДНК затем активирует фермент CRISPR-Cas12a, который действует как молекулярная шредерная машина по отношению к одноцепочечной ДНК. Подав множество коротких ДНК-репортеров с флуоресцентной меткой, каждое разрезание увеличивает световой сигнал. В принципе, крошечное количество молекулы-мишени должно быть преобразовано в сильный, легко измеряемый флуоресцентный сигнал.
Испытание сенсора на основе CRISPR
Исследователи подошли к задаче как аккуратные механики, испытывающие новый двигатель. Сначала они настроили саму реакцию Cas12a: выбирали оптимальный буфер, ионы металлов, количество фермента и конструкцию репортера, чтобы получать сильные и надёжные световые сигналы при наличии триггерной ДНК. В оптимальных условиях Cas12a мог обнаруживать чрезвычайно низкие уровни триггерной ДНК — до триллионных долей моля — и делал это воспроизводимо. Это подтвердило, что сигнальная часть — «усилитель» теста — сама по себе была надёжной и чувствительной.
Где дизайн начинает давать сбой
Реальная проблема возникла, когда они соединили этот чувствительный усилитель с реальными аптамерами из научной литературы. Команда выбрала девять аптамеров, о которых сообщалось, что они распознают семь разных малых молекул, включая пестициды, антибиотики, печёночный токсин от водорослей и противомалярийные препараты. В теории эти аптамеры должны были высвобождать триггерную ДНК при встрече с мишенью. Авторы тщательно регулировали силу сцепления триггерной ДНК с каждым аптамером, проверяли разные температуры, времена инкубации и условия буфера, а также пробовали более сложную версию, где комплексы аптамер–триггер прикреплялись к магнитным шарикам и затем удалялись из реакции. Несмотря на эти обширные усилия, чёткие сигналы появились только для двух из семи целевых молекул. Для остальных добавление мишени не приводило к увеличению количества триггерной ДНК в растворе, что указывает на то, что либо аптамеры не связывались так, как заявлено, либо связывание не вызывало ожидаемого изменения формы и высвобождения.
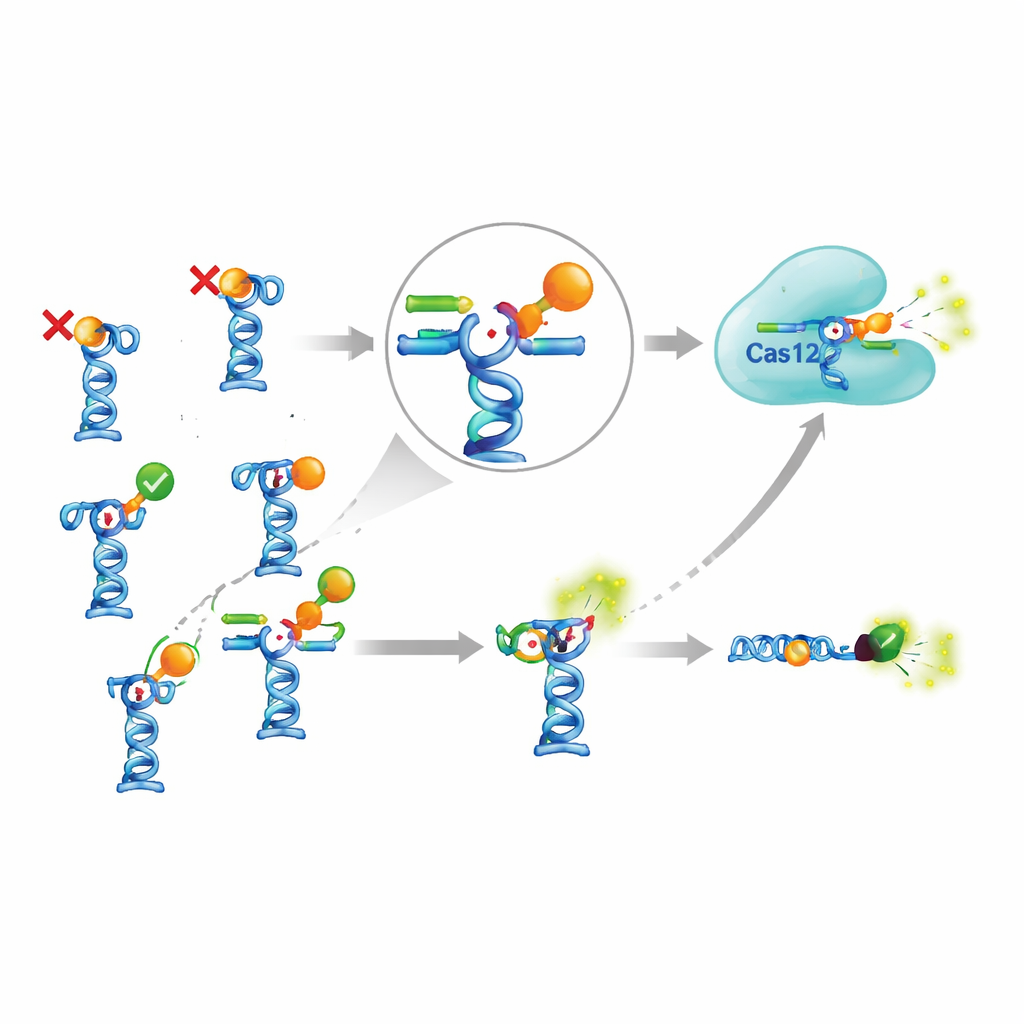
Стоит ли усложнённая схема затраченных усилий?
Чтобы оценить, действительно ли CRISPR-присадка оправдывает себя, авторы сравнили её с более простым аптамерным тестом, который полностью пропускает Cas12a. В этой упрощённой конструкции аптамер несёт флуоресцентную метку, а его комплементарная цепь — группу-агент, гасящую свет; когда комплементарная цепь вытесняется целевой молекулой, флуоресценция напрямую увеличивается. Для одной из немногих рабочих мишеней — противомалярийного пиперакина — версия на основе CRISPR обнаруживала немного более низкие концентрации, чем простой тест, но лишь примерно в 2–3 раза. Достижение этого скромного выигрыша требовало дополнительных ферментов, большего количества реагентов, более длительных протоколов и дополнительной оптимизации. При этом некоторые ранее опубликованные аптамерные датчики — например, для распространённого токсина водорослей и инсектицида фипронил — вовсе не удалось воспроизвести, даже когда авторы в точности соблюдали описанные условия и использовали независимые методы проверки связывания.
Что это значит для будущих быстрых тестов
Исследование делает вывод, что хотя флуоресцентная система Cas12a сама по себе мощна, общая стратегия аптамер–CRISPR сенсоров хрупка. Её успех зависит от аптамеров, которые не только связывают мишень, но и надёжно освобождают триггерную ДНК — требование, которое многие опубликованные аптамеры фактически не удовлетворяют. Пока исследователи и прикладные лаборатории должны относиться к заявлениям о «plug-and-play» с осторожностью, вкладывать ресурсы в тщательную валидацию работы аптамеров и оценивать, не подойдёт ли им более простой аптамерный тест или устоявшиеся методы, такие как масс-спектрометрия. Аптамерные CRISPR-сенсоры остаются интригующим инструментом, но пока не стали универсальным решением для обнаружения малых молекул, как их иногда преподносили.
Цитирование: Brandenberg, O.F., Janssen, E.ML. & Schubert, O.T. A critical assessment of aptamer and CRISPR-Cas12a-based biosensors for small molecule detection. npj Biosensing 3, 28 (2026). https://doi.org/10.1038/s44328-026-00089-8
Ключевые слова: аптамерные биосенсоры, детекция CRISPR-Cas12a, сенсоры малых молекул, загрязнители окружающей среды, флуоресцентные анализы