Clear Sky Science · nl
Een kritische beoordeling van aptameer- en CRISPR-Cas12a-gebaseerde biosensoren voor detectie van kleine moleculen
Waarom kleine verontreinigingen en snelle tests ertoe doen
Van drinkwater en rivieren tot het voedsel op ons bord en de medicijnen die we gebruiken: talrijke kleine moleculen circuleren in onze omgeving en in ons lichaam. Sommige zijn levensreddende geneesmiddelen; andere zijn giftige verontreinigingen. Het meten van deze stoffen vereist doorgaans omvangrijke en dure instrumenten, die moeilijk mee te nemen zijn naar het veld of naar een kleine kliniek. Dit artikel onderzoekt een veelbelovend alternatief: compacte biochemische tests die met ontwerp-DNA-strengen en CRISPR-enzymen de aanwezigheid van kleine moleculen omzetten in een helder lichtsignaal. De auteurs wilden nagaan hoe goed deze gehypete aanpak in de praktijk daadwerkelijk werkt.
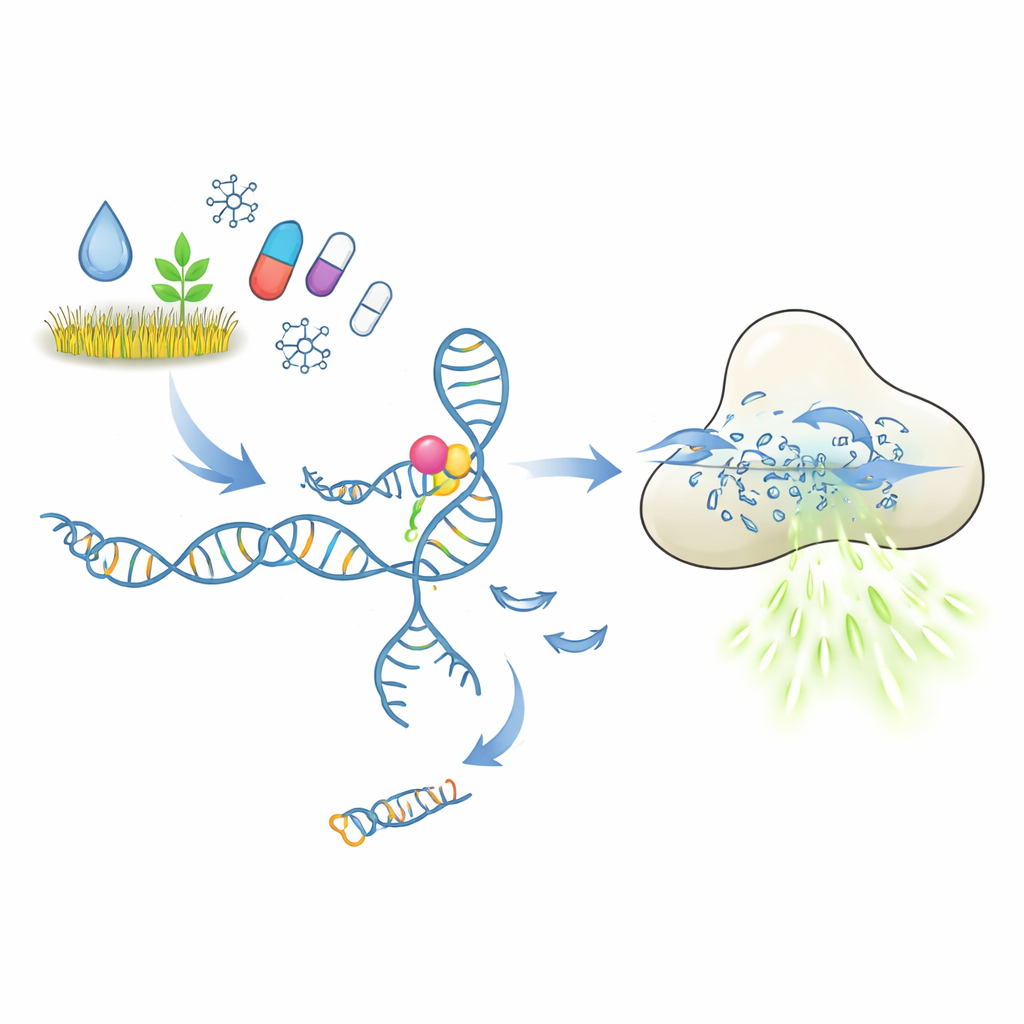
Hoe een moleculaire slot-en-sleuteltest geacht is te werken
In de kern van deze tests bevinden zich aptamers, korte stukken DNA of RNA die vouwen in structuren die zich aan een gekozen doelmolecule kunnen hechten, vergelijkbaar met antilichamen. In de hier beschreven opzet houdt een aptameer vast aan een kort DNA-stukje dat dienstdoet als trigger. Wanneer het doelpesticide of geneesmiddel bindt, zou het aptameer van vorm veranderen en deze trigger vrijgeven. Het vrijgekomen DNA activeert dan het CRISPR-Cas12a-enzym, dat zich gedraagt als een moleculaire papierversnipperaar voor enkelstrengs DNA. Door Cas12a veel korte DNA-reporters met een fluorescent kleurstof te bieden, produceert elke knip extra licht. In principe zou een kleine hoeveelheid doelmolecule zo moeten worden omgezet in een sterk, gemakkelijk meetbaar fluorescentiesignaal.
De CRISPR-gebaseerde sensor aan een test onderwerpen
De onderzoekers benaderden het probleem als nauwgezette monteurs die een nieuwe motor testen. Eerst stemden ze de Cas12a-reactie zelf af: ze kozen de beste buffer, metaalionen, hoeveelheid enzym en reporterontwerp om sterke en betrouwbare lichtsignalen te krijgen wanneer trigger-DNA aanwezig was. Onder geoptimaliseerde condities kon Cas12a extreem lage niveaus trigger-DNA detecteren, tot biljoensten van een mol, en deed dit reproduceerbaar. Dit bevestigde dat de signaaloverdrachtsmachinerie — het "versterker"-gedeelte van de test — op zichzelf robuust en gevoelig was.
Waar het ontwerp begint te falen
De echte uitdaging trad op toen ze deze gevoelige versterker koppelden aan aptamers uit de wetenschappelijke literatuur. Het team selecteerde negen aptamers die naar verluidt zeven verschillende kleine moleculen herkennen, waaronder pesticiden, antibiotica, een levertoxine uit algen en antimalariamiddelen. In theorie zouden deze aptamers de trigger-DNA moeten loslaten wanneer zij hun doel tegenkomen. De auteurs pasten zorgvuldig aan hoe sterk het trigger-DNA aan elk aptameer kleefde, testten verschillende temperaturen, incubatietijden en buffercondities, en probeerden zelfs een complexere variant waarbij de aptameercomplexen aan magnetische parels werden gebonden en daarna uit de reactie werden verwijderd. Ondanks deze uitgebreide inspanning traden duidelijke signalen slechts voor twee van de zeven doelmoleculen op. Voor de anderen leidde toevoeging van het doel niet tot extra trigger-DNA in oplossing, wat suggereert dat óf de aptamers niet binden zoals beweerd, óf dat binding niet de verwachte vormverandering en vrijgave veroorzaakt.
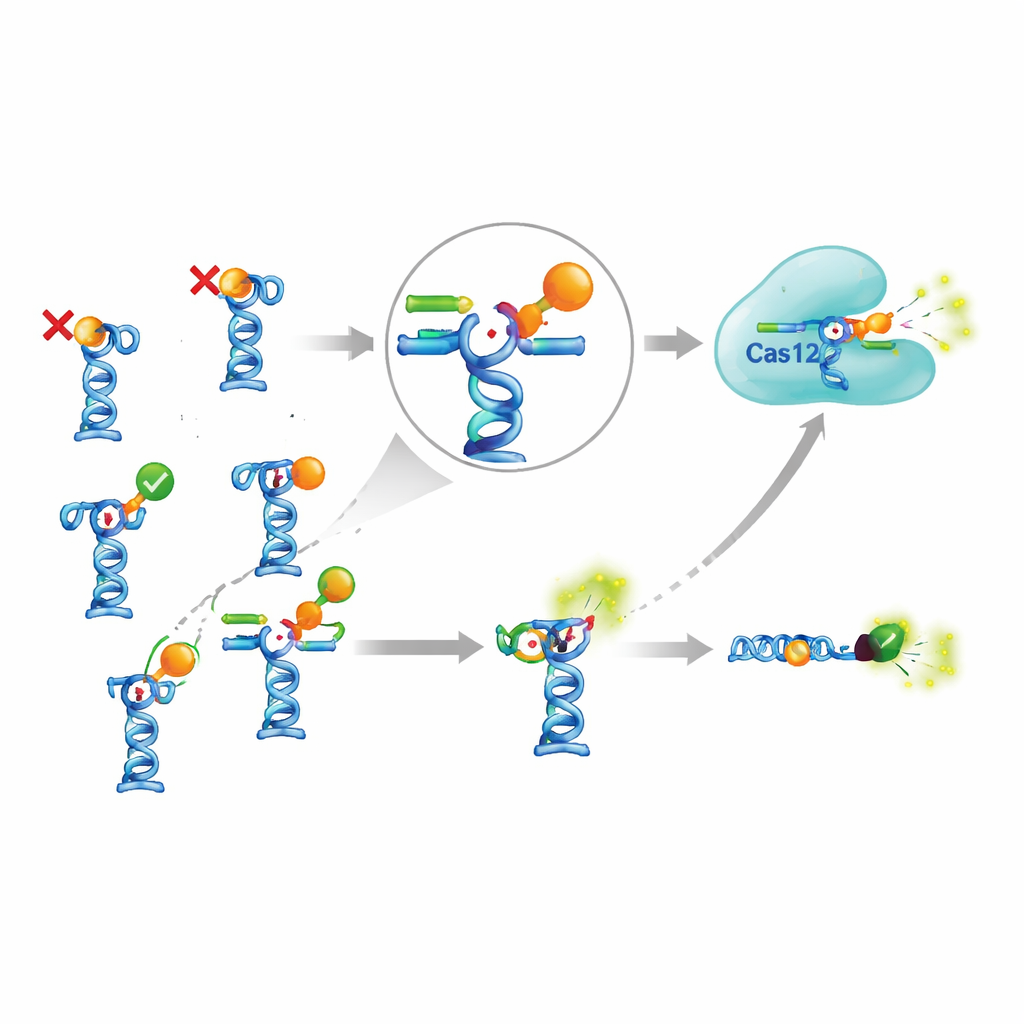
Is de ingewikkelde opzet de moeite waard?
Om te beoordelen of de CRISPR-toevoeging werkelijk de moeite waard is, vergeleken de auteurs deze met een eenvoudiger aptameertest die Cas12a helemaal overslaat. In dit eenvoudigere ontwerp draagt het aptameer een fluorescentiekleurstof en draagt de partnerstreng een lichtdempend groepje; wanneer de partnerstreng door de doelmolecule wordt verdrongen, neemt de fluorescentie direct toe. Voor één van de weinige werkende doelen, het antimalariamiddel piperaquine, detecteerde de CRISPR-gebaseerde versie iets lagere concentraties dan de eenvoudige test, maar slechts met een factor twee tot drie. Het bereiken van dit bescheiden voordeel vereiste extra enzymen, meer reagentia, langere protocollen en meer optimalisatie. Tegelijkertijd konden enkele eerder gepubliceerde aptameer-gebaseerde sensoren — bijvoorbeeld voor een veelvoorkomend algentoxine en het insecticide fipronil — helemaal niet worden gereproduceerd, zelfs niet wanneer de auteurs de gerapporteerde condities nauwgezet volgden en een onafhankelijke methode gebruikten om binding te testen.
Wat dit betekent voor toekomstige sneltesten
De studie concludeert dat hoewel het Cas12a-fluorescentiesysteem op zich krachtig is, de gecombineerde aptameer–CRISPR-sensorstrategie kwetsbaar is. Het succes hangt af van aptamers die niet alleen aan hun doelen binden maar ook betrouwbaar de trigger-DNA loslaten — een veeleisende eis die veel gepubliceerde aptamers in de praktijk niet lijken te vervullen. Voorlopig zouden onderzoekers en toepassingsgerichte laboratoria terughoudend moeten zijn bij kant-en-klare claims, grondig moeten investeren in validatie van aptameerprestaties, en afwegen of eenvoudigere aptameertests of gevestigde methoden zoals massaspectrometrie beter aan hun behoeften voldoen. CRISPR-gebaseerde aptasensoren blijven een intrigerend hulpmiddel, maar nog geen universele oplossing voor de detectie van kleine moleculen zoals ze soms wordt aangeprezen.
Bronvermelding: Brandenberg, O.F., Janssen, E.ML. & Schubert, O.T. A critical assessment of aptamer and CRISPR-Cas12a-based biosensors for small molecule detection. npj Biosensing 3, 28 (2026). https://doi.org/10.1038/s44328-026-00089-8
Trefwoorden: aptameer-biosensoren, CRISPR-Cas12a detectie, detectie van kleine moleculen, milieuverontreinigingen, fluorescentie-assays