Clear Sky Science · zh
用于通过荧光各向异性去极化高通量研究肽-脂质体相互作用的重组蛋白平台
会变形的蛋白片段如何找到合适的膜
在每个细胞内部,无数的运输、信号传递和回收事件都依赖于蛋白质在恰当的时间落在恰当的膜上。许多此类蛋白利用短小、松散的片段,这些片段只有在接触到合适的膜时才折叠成整齐的螺旋。本文介绍了一种新的、更快的方法来研究这些会变形的片段如何识别特定膜,利用一种意外的光学信号作为内置报告器。
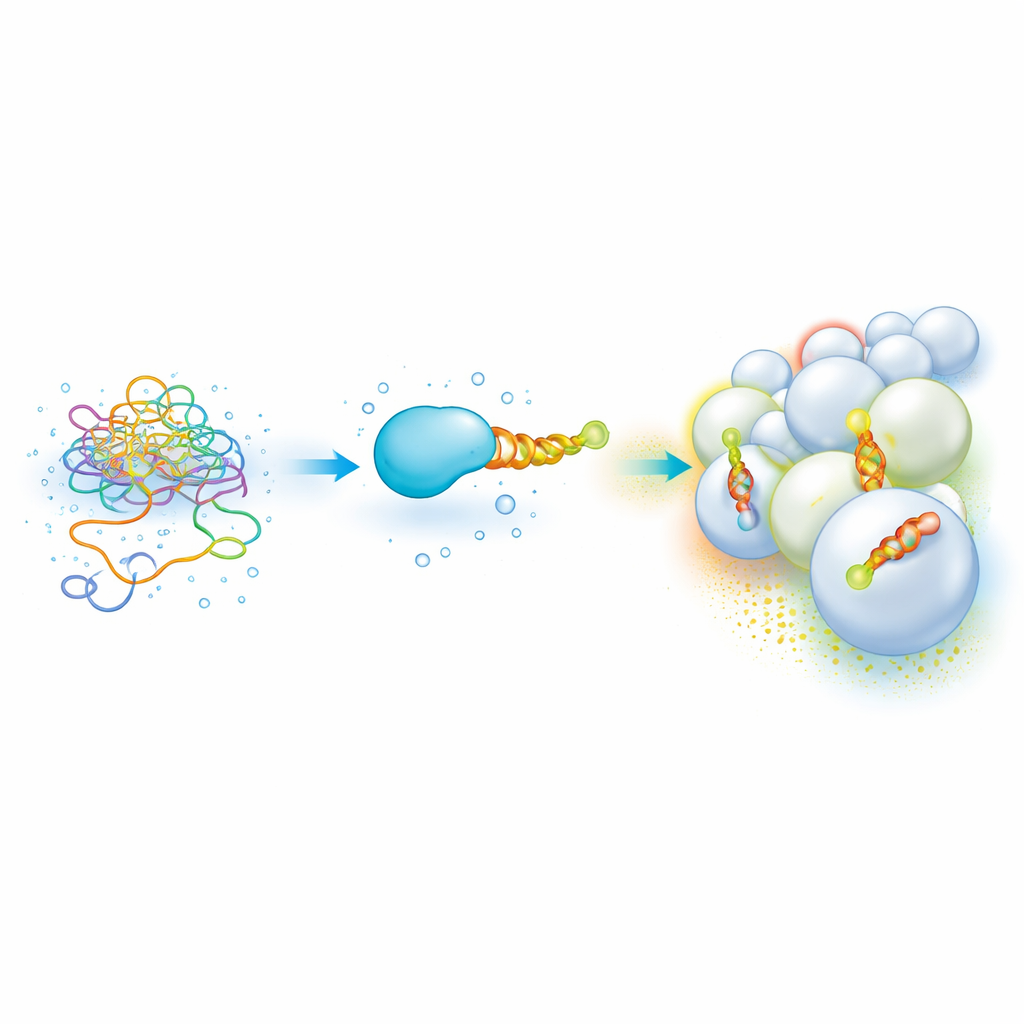
读取膜“邮编”的柔性蛋白末端
许多重要的细胞蛋白携带一段短小的无结构片段,当其停靠在膜上时会形成两亲性螺旋——一侧疏油、另一侧亲水的螺旋。这些螺旋通过感知脂质成分和曲率,帮助蛋白区分不同的细胞器,使它们能够定位到内体或线粒体等部位。但单独拿出这些黏性、部分疏油的片段来研究并不容易:它们容易聚集、沉淀,并且需要缓慢且样本消耗大的方法来测量与不同膜的结合亲和力。因此,建立将螺旋序列与膜偏好性连接起来的清晰“密码”一直很困难。
一个模块化的蛋白平台,使结合可视化
作者们构建了一个重组平台,以驯服这些难以处理的螺旋,并使它们的膜选择容易并行测量。每个测试螺旋都与一种表现良好的载体蛋白SUMO融合,SUMO提高了可溶性和表达水平,并在远端标记上荧光染料。当该构建体与人工脂质囊泡混合并在常见的微孔板读数仪中读取时,研究者们跟踪荧光各向异性——这是一种衡量染料发射光在多大程度上“记住”其偏振方向的指标,取决于染料自由旋转的程度。通过在小体积中对许多脂质混合物和囊泡尺寸进行滴定,他们快速构建了不同螺旋在广泛膜成分和曲率景观下的结合曲线。
一种反直觉的信号仍能报告结合
直觉上,人们会预期当一个小的蛋白-染料构建体与更大的囊泡结合时,其旋转变慢,因而各向异性上升。然而,作者观察到相反的现象:随着结合增加,各向异性降低。他们通过将这一奇特行为与基于色氨酸荧光的经典方法进行比较来检验它是否仍能反映真实的膜结合,后者可以报告螺旋在膜疏油核心中的埋入深度。对于几种具有生物学相关性的螺旋——来自如Amphiphysin、CHMP4B、Endophilin-B1和Huntingtin等蛋白——新平台与传统读数给出了高度匹配的结合曲线和脂质偏好,甚至揭示了新的趋势,例如Amphiphysin螺旋对富含胆固醇膜的更强结合。
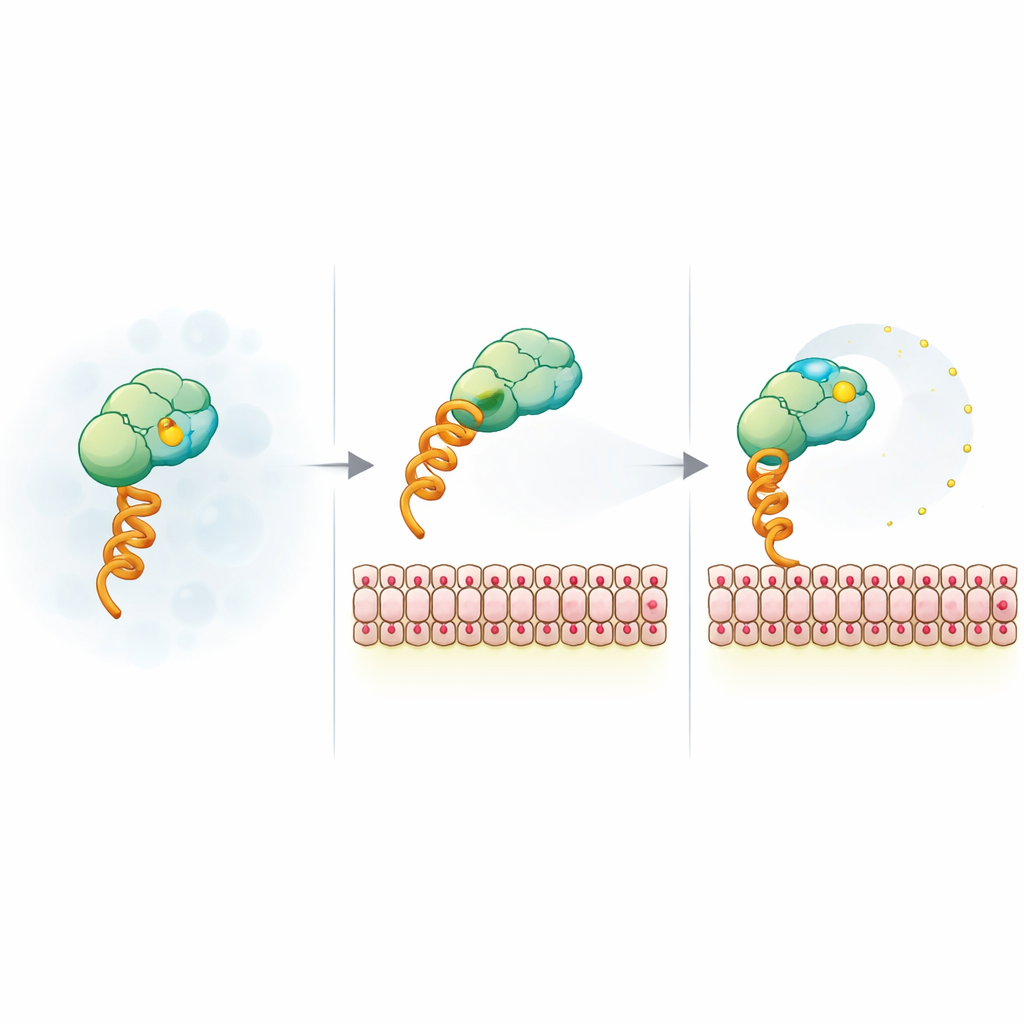
膜电荷如何释放荧光报告器
为了解释这一意外信号,团队将系统简化为一个模型构建体,该构建体通过通用的组氨酸标签和与镍螯合的脂质结合膜。他们随后改变了囊泡尺寸、表面电荷、盐浓度和染料类型。各向异性下降对囊泡尺寸和荧光团身份不敏感,但对负膜电荷和盐的屏蔽高度敏感,指向电荷起源。时间分辨荧光测量显示,当结合到带电膜时,尽管整个复合体旋转变慢,染料获得了额外的局部移动性。核磁共振和FRET实验进一步提示,SUMO表面的正电斑块可作为带负电染料的临时系带;与带电膜结合或对这些斑块进行突变都会放松该系带,使染料更自由地摆动,从而降低各向异性。
规模化绘制膜偏好图谱
由于各向异性下降是稳健且可重复的,它可以被用作方便的结合报告器,而不是视为有问题的伪像。不同脂质类型和曲率的囊泡阵列可以被快速探测,使研究者能够确定哪些脂质与形状组合最能吸引某一螺旋。该平台对带负电的膜尤为有效,这类膜在参与运输和能量生产的细胞器中很常见。通过工程化改变载体蛋白电荷的变体,作者将可用条件的范围扩展到更生理的盐度和轻微带电的膜,进一步拓宽了该方法的适用性。
这对理解细胞靶向意味着什么
通俗地说,这项工作提供了一个新的高通量“读取器”,用于识别引导蛋白到正确细胞地址的分子邮编。科学家们现在可以不必依赖笨重且缓慢的实验,而是在并行条件下筛选许多螺旋和膜配方,使用一个简单的光学特征——虽反向但已被充分理解——来指示结合。随着时间推移,这应当使解码哪类氨基酸模式对应哪类脂质环境成为可能,从而阐明细胞如何利用这些小而灵活的螺旋对蛋白进行分拣、重塑膜以及控制关键的信号和运输通路。
引用: Margaritakis, A., Qian, M., Johnson, D.H. et al. Recombinant protein platform for high-throughput investigation of peptide-liposome interactions via fluorescence anisotropy depolarization. Commun Chem 9, 165 (2026). https://doi.org/10.1038/s42004-026-01994-9
关键词: 膜结合肽, 荧光各向异性, 两亲性螺旋, 脂质囊泡, 蛋白质–膜相互作用