Clear Sky Science · ja
蛍光異方性脱偏光を用いたペプチド–リポソーム相互作用のハイスループット解析のための組換えタンパク質プラットフォーム
形を変えるタンパク質断片が正しい膜を見つける仕組み
細胞内では、多数の輸送、シグナル伝達、リサイクルが、タンパク質が適切なタイミングで適切な膜に結合することに依存しています。多くのタンパク質は、適合する膜に触れると初めてきちんとしたヘリックス構造をとる短く柔らかい配列を利用します。本論文は、そんな形を変える断片が特定の膜をどのように認識するかを、意外な光学信号を内蔵レポーターとして用いることで、より速く調べる新しい方法を紹介します。
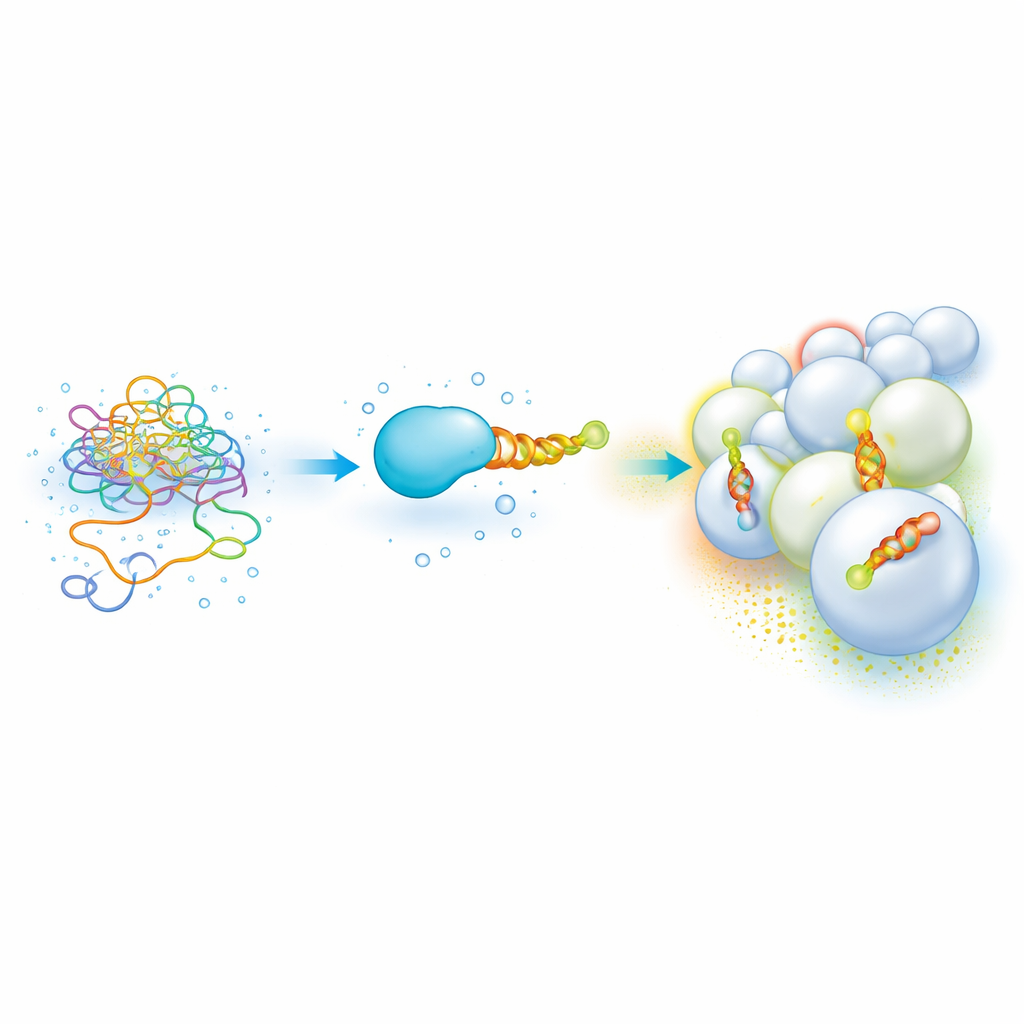
膜の「郵便番号」を読み取る柔軟なタンパク質末端
多くの重要な細胞内タンパク質は、膜にドッキングすると両親媒性ヘリックス—片面が疎水性、片面が親水性を持つ螺旋構造—に折りたたまれる短い非構造領域を持ちます。これらのヘリックスは脂質組成や曲率を感知してエンドソームやミトコンドリアなどの特定の小器官を識別することで、タンパク質の局在を導きます。しかし、単体のままではこれらの粘着性で部分的に疎水的な断片は扱いにくく、凝集や沈殿を起こし、異なる膜への結合の強さを測るには遅くサンプルを大量に消費する手法が必要でした。そのため、ヘリックス配列と膜選好性を結びつける明確な「コード」を構築することは困難でした。
結合で発光するモジュール型タンパク質プラットフォーム
著者らは、扱いにくいヘリックスを安定化させ、その膜選択を並列に測定しやすくする組換えプラットフォームを構築しました。各テスト用ヘリックスは可溶性と発現性を高めるキャリアタンパク質SUMOに融合され、先端には蛍光色素が結合されています。構築体を人工脂質小胞と混合して一般的なマイクロプレートリーダーで読み出すと、蛍光異方性—色素の発光がどれだけ偏光を“記憶”するかの尺度で、色素の回転の自由度に依存します—を追跡します。小容量で多数の脂質混合物と小胞サイズを滴定することで、さまざまなヘリックスについて幅広い膜組成と曲率の景観にわたる結合曲線を迅速に構築できます。
直感に反するが結合を報告するシグナル
直感的には、小さなタンパク質–色素構築体がはるかに大きな小胞に結合すると回転が遅くなり異方性は上昇すると期待されます。ところが著者らは逆に、結合が増えると異方性が低下することを観察しました。この奇妙な挙動が実際の膜結合を反映しているかを調べるために、彼らはトリプトファン蛍光に基づく古典的手法(ヘリックスが膜の疎水コアにどれだけ深く埋まるかを報告する)と比較しました。Amphiphysin、CHMP4B、Endophilin-B1、Huntingtinのような生物学的に重要なヘリックスについて、新しいプラットフォームと従来の指標は結合曲線や脂質選好性がよく一致し、コレステロールリッチな膜に対するAmphiphysinヘリックスの結合が強いといった新たな傾向も明らかになりました。
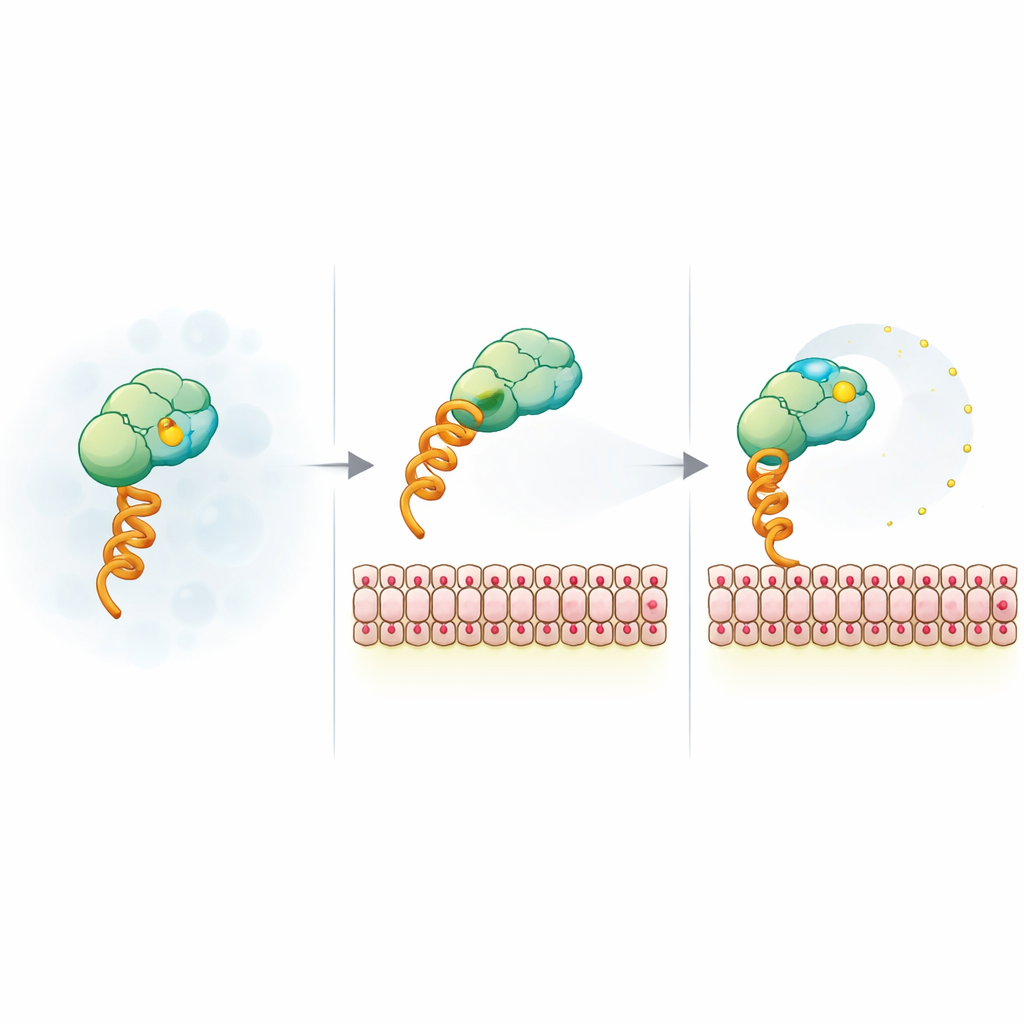
膜の電荷が蛍光レポーターを解き放つ仕組み
予期せぬ信号を説明するために、チームは系を一般的なヒスチジンタグとニッケル配位脂質を介して膜に結合するモデル構築体まで単純化しました。次に小胞のサイズ、表面電荷、塩濃度、色素の種類を変化させました。異方性の低下は小胞サイズや蛍光団の種類には鈍感でしたが、負の膜電荷と塩による遮蔽には非常に敏感であり、電気的起源を示唆しました。時間分解蛍光測定は、荷電膜に結合したときに色素が全体の回転は遅くなっても局所的には追加の可動性を得ることを示しました。核磁気共鳴やFRET実験はさらに、SUMO表面の正電荷パッチが負に帯電した色素の一時的な係留点として働く可能性を示唆しました。荷電膜への結合やこれらのパッチの変異はその係留を緩め、色素がより自由に揺らぐようになり異方性が低下すると考えられます。
大規模に膜選好性をマッピングする
異方性の低下が堅牢かつ再現性が高いため、これは問題となるアーティファクトとして扱うのではなく結合の便利なレポーターとして利用できます。脂質の種類や曲率が異なる小胞のアレイを迅速にプローブすることで、どの脂質と形状の組み合わせが特定のヘリックスを最も強く引き付けるかを特定できます。このプラットフォームは、輸送やエネルギー生産に関わる小器官で一般的な負に帯電した膜に対して特に有効です。キャリアタンパク質の電荷を改変した変異体を設計することで、生理的な塩濃度や微妙に帯電した膜への有用範囲を拡張し、手法の適用範囲をさらに広げています。
細胞内ターゲティングの理解に与える意義
平たく言えば、この研究はタンパク質を正しい細胞内アドレスへ導く分子郵便番号を読むための新しいハイスループットな“リーダー”を提供します。かさばり遅い実験に頼る代わりに、研究者は多くのヘリックスと膜の組み合わせを並列にスクリーニングでき、予期せぬが十分に理解された方向に反転する単純な光学的指標を利用できます。時間をかけて、どのアミノ酸パターンがどの脂質環境に対応するかを解読できるようになり、細胞がこれらの小さく柔軟なヘリックスを使ってタンパク質を仕分け、膜を再構築し、重要なシグナル伝達や輸送経路を制御する仕組みの解明が進むことが期待されます。
引用: Margaritakis, A., Qian, M., Johnson, D.H. et al. Recombinant protein platform for high-throughput investigation of peptide-liposome interactions via fluorescence anisotropy depolarization. Commun Chem 9, 165 (2026). https://doi.org/10.1038/s42004-026-01994-9
キーワード: 膜結合ペプチド, 蛍光異方性, 両親媒性ヘリックス, 脂質小胞, タンパク質–膜相互作用