Clear Sky Science · fr
Plateforme de protéines recombinantes pour l’étude à haut débit des interactions peptide-liposome par dépolarisation d’anisotropie de fluorescence
Comment des fragments protéiques polymorphes trouvent les membranes appropriées
À l’intérieur de chaque cellule, d’innombrables livraisons, signaux et événements de recyclage dépendent du fait que les protéines atteignent la membrane adéquate au bon moment. Beaucoup de ces protéines utilisent de courts segments flexibles qui ne se replient en hélices ordonnées que lorsqu’ils touchent une membrane appropriée. Cet article présente une nouvelle méthode, plus rapide, pour étudier comment ces segments métamorphes reconnaissent des membranes spécifiques, en utilisant un signal optique surprenant comme témoin intégré.
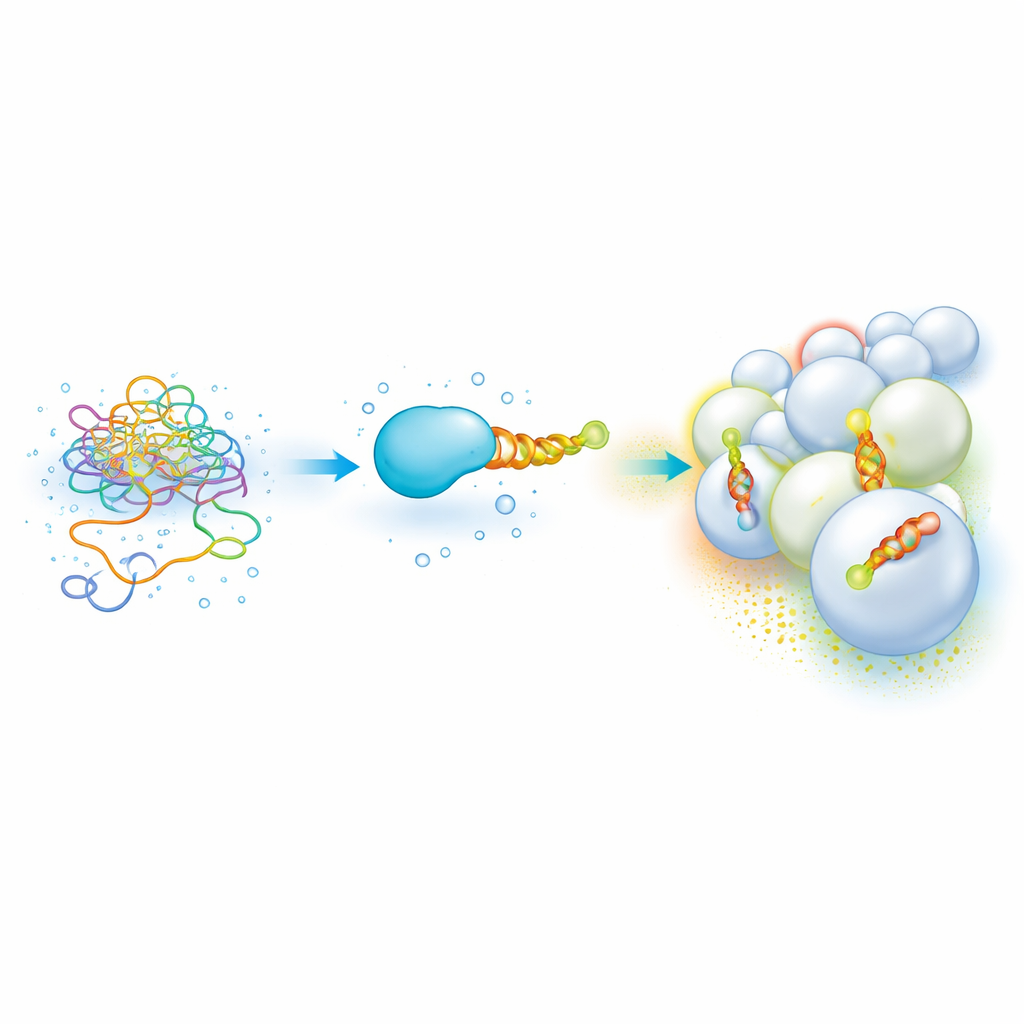
Extrémités protéiques flexibles qui lisent les « codes postaux » membranaires
De nombreuses protéines cellulaires importantes portent un court segment non structuré qui devient une hélice amphipathique — une spirale à une face hydrophobe et une face hydrophile — dès qu’il se fixe à une membrane. Ces hélices aident les protéines à distinguer un organite d’un autre en détectant la composition lipidique et la courbure, ce qui leur permet de cibler des lieux comme les endosomes ou les mitochondries. Mais prises isolément, ces portions adhésives et partiellement hydrophobes sont difficiles à manipuler : elles s’agrègent, précipitent et nécessitent des méthodes lentes et gourmandes en échantillons pour mesurer leur affinité pour différentes membranes. Il en résulte qu’il a été difficile d’élaborer un « code » clair reliant la séquence des hélices à leur préférence membranaire.
Une plateforme protéique modulaire qui éclaire la liaison
Les auteurs ont conçu une plateforme recombinante qui dompte ces hélices récalcitrantes et facilite la mesure simultanée de leurs préférences membranaires. Chaque hélice testée est fusionnée à une protéine porteuse bien tolérée nommée SUMO, qui améliore la solubilité et l’expression, et est marquée à l’extrémité libre par un colorant fluorescent. Lorsque le construit est mélangé à des vésicules lipidiques artificielles et mesuré dans un lecteur de microplaques courant, les chercheurs suivent l’anisotropie de fluorescence — une mesure de la capacité de la fluorescence à « conserver » sa polarisation, dépendant de la liberté de rotation du colorant. En titrant de nombreuses compositions lipidiques et tailles de vésicules en petits volumes, ils établissent rapidement des courbes de liaison pour différentes hélices à travers un large éventail de compositions et de courbures membranaires.
Un signal contre-intuitif qui reflète néanmoins la liaison
Intuitivement, on s’attendrait à ce que lorsqu’un petit construit protéine‑colorant se lie à une vésicule beaucoup plus grande, sa rotation ralentisse et que l’anisotropie augmente. À l’inverse, les auteurs observent que l’anisotropie diminue lorsque la liaison augmente. Ils ont vérifié si ce comportement étrange reflétait malgré tout une association membranaire réelle en le comparant à une méthode classique basée sur la fluorescence du tryptophane, qui renseigne sur la profondeur d’enfouissement d’une hélice dans le cœur lipophile de la membrane. Pour plusieurs hélices d’intérêt biologique — issues de protéines telles qu’Amphiphysin, CHMP4B, Endophilin‑B1 et Huntingtin — la nouvelle plateforme et la méthode traditionnelle produisent des courbes de liaison et des préférences lipidiques très proches, révélant même de nouvelles tendances comme une affinité renforcée de l’hélice d’Amphiphysin pour les membranes riches en cholestérol.
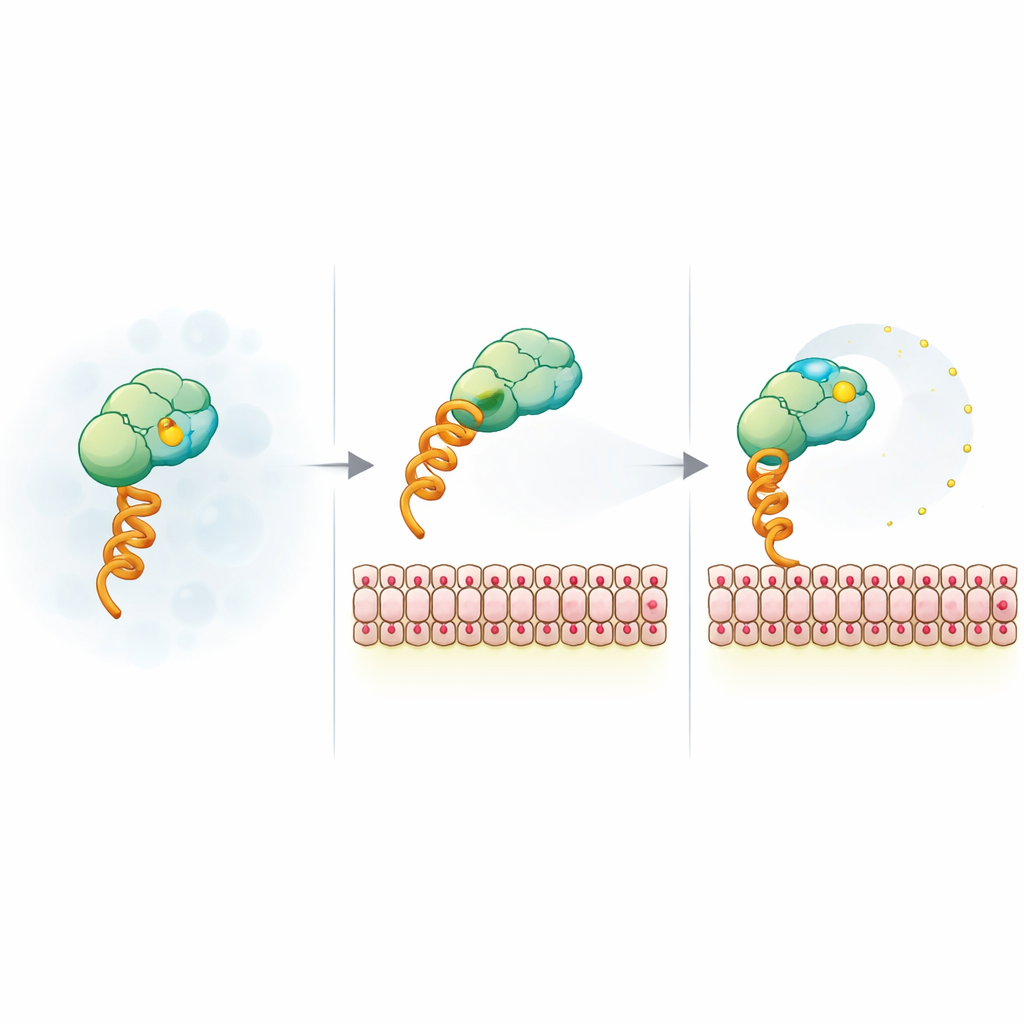
Comment la charge membranaire libère le témoin fluorescent
Pour expliquer ce signal inattendu, l’équipe a réduit le système à un construit modèle qui se lie aux membranes via une étiquette histidine générique et un lipide chélatant le nickel. Ils ont ensuite modifié la taille des vésicules, la charge de surface, le niveau de sel et le type de colorant. La chute d’anisotropie s’est révélée insensible à la taille des vésicules et à l’identité du fluorophore mais fortement dépendante de la charge négative de la membrane et du criblage par le sel, ce qui indique une origine électrostatique. Des mesures de fluorescence résolues en temps ont montré que, lorsqu’il est lié à des membranes chargées, le colorant gagne en mobilité locale même si l’ensemble du complexe tourne plus lentement. Des expériences de résonance magnétique nucléaire et de FRET ont en outre suggéré que des zones positives à la surface de SUMO peuvent agir comme des attaches temporaires pour le colorant chargé négativement ; la liaison à une membrane chargée et la mutation de ces zones desserrent cette attache, laissant le colorant osciller plus librement et diminuant l’anisotropie.
Cartographier à grande échelle les préférences membranaires
Parce que la diminution d’anisotropie est robuste et reproductible, elle peut être utilisée comme un témoin pratique de la liaison plutôt que d’être considérée comme un artefact problématique. Des bancs de vésicules differents par le type de lipide et la courbure peuvent être sondés rapidement, permettant aux chercheurs d’identifier quelles combinaisons de lipides et de formes attirent le mieux une hélice donnée. La plateforme fonctionne particulièrement bien pour les membranes chargées négativement, fréquentes dans les organites impliqués dans le trafic et la production d’énergie. En concevant des variantes de la protéine porteuse modifiées au niveau de la charge, les auteurs étendent la plage d’application utile vers des niveaux de sel plus physiologiques et des membranes faiblement chargées, élargissant encore le champ d’utilisation de la méthode.
Ce que cela implique pour la compréhension du ciblage cellulaire
Concrètement, ce travail fournit un nouveau « lecteur » à haut débit pour les codes moléculaires qui guident les protéines vers la bonne adresse cellulaire. Plutôt que de dépendre d’expériences volumineuses et lentes, les scientifiques peuvent désormais cribler en parallèle de nombreuses hélices et recettes de membranes, en s’appuyant sur une signature optique simple qui s’inverse de façon inattendue mais dont le mécanisme est bien compris. Avec le temps, cela devrait permettre de décoder quelles combinaisons d’acides aminés correspondent à quels environnements lipidiques, clarifiant comment les cellules utilisent ces petites hélices flexibles pour trier les protéines, remodeler les membranes et contrôler des voies essentielles de signalisation et de trafic.
Citation: Margaritakis, A., Qian, M., Johnson, D.H. et al. Recombinant protein platform for high-throughput investigation of peptide-liposome interactions via fluorescence anisotropy depolarization. Commun Chem 9, 165 (2026). https://doi.org/10.1038/s42004-026-01994-9
Mots-clés: peptides de liaison membranaire, anisotropie de fluorescence, hélices amphipathiques, vésicules lipidiques, interactions protéine–membrane