Clear Sky Science · it
Piattaforma di proteine ricombinanti per l’indagine ad alto rendimento delle interazioni peptide-liposoma tramite depolarizzazione dell’anisotropia di fluorescenza
Come pezzi proteici che cambiano forma trovano le membrane giuste
All’interno di ogni cellula, innumerevoli consegne, segnali ed eventi di riciclaggio dipendono dal fatto che le proteine atterrino sulla membrana corretta al momento giusto. Molte di queste proteine usano tratti corti e flessibili che si ripiegano in eleganti eliche solo quando incontrano una membrana adatta. Questo articolo presenta un modo nuovo e più rapido per studiare come questi frammenti muta-forma riconoscano membrane specifiche, sfruttando un segnale ottico sorprendente come reporter integrato.
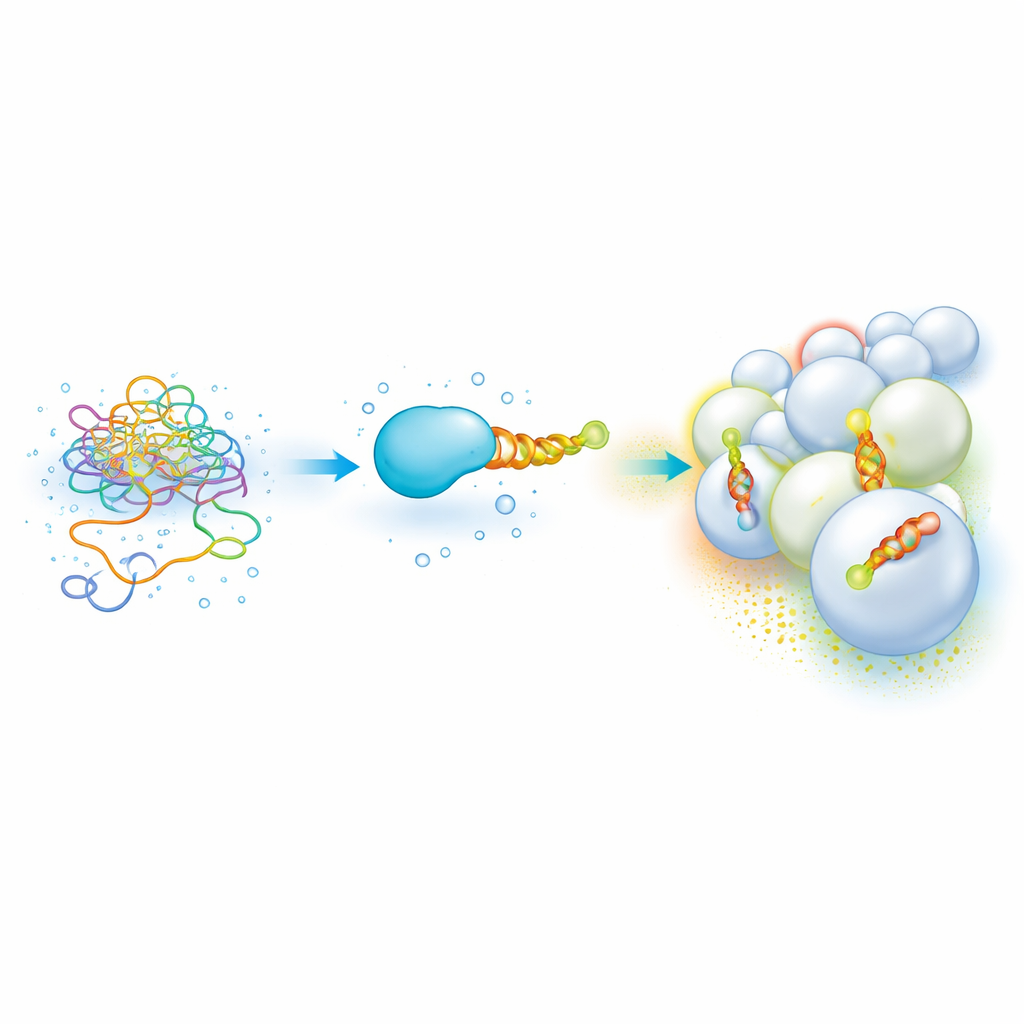
Estremità proteiche flessibili che leggono i “codici postali” delle membrane
Molte proteine cellulari importanti portano un segmento breve e non strutturato che diventa un’elica anfipatica — una spirale con un lato idrocarburico e un lato idrofilo — quando si ancora a una membrana. Queste eliche aiutano le proteine a distinguere un organello dall’altro rilevando la composizione lipidica e la curvatura, permettendo loro di localizzarsi in posti come endosomi o mitocondri. Ma prese da sole, queste porzioni appiccicose e parzialmente idrofobiche sono difficili da manipolare: tendono a aggregare, precipitare e richiedono metodi lenti e dispendiosi in campione per misurare l’affinità verso membrane diverse. Di conseguenza, costruire un “codice” chiaro che colleghi la sequenza dell’elica alla preferenza per una membrana è stato finora complicato.
Una piattaforma proteica modulare che illumina il legame
Gli autori hanno costruito una piattaforma ricombinante che doma queste eliche indisciplinate e rende le loro scelte di membrana facili da misurare in parallelo. Ogni elica in prova è fusa a una proteina veicolatrice ben comportata chiamata SUMO, che migliora solubilità ed espressione, e marcata all’estremità opposta con un colorante fluorescente. Quando il costrutto viene miscelato con vescicole lipidiche artificiali e letto in un comune microplate reader, i ricercatori tracciano l’anisotropia di fluorescenza — una misura di quanto l’emissione luminosa del colorante “ricordi” la sua polarizzazione, che dipende da quanto liberamente il colorante può ruotare. Titolando molte miscele lipidiche e dimensioni di vescicole in piccoli volumi, costruiscono rapidamente curve di legame per diverse eliche su un ampio panorama di composizioni e curvature di membrana.
Un segnale controintuitivo che comunque segnala il legame
Intuitivamente ci si aspetterebbe che quando un piccolo costrutto proteina-colorante si lega a una vescicola molto più grande la sua rotazione rallenti e l’anisotropia aumenti. Invece, gli autori osservano l’opposto: l’anisotropia diminuisce con l’aumentare del legame. Hanno verificato se questo comportamento insolito corrispondesse comunque alla reale associazione con la membrana confrontandolo con un metodo classico basato sulla fluorescenza del triptofano, che segnala quanto profondamente un’elica si inserisce nel nucleo idrofobico della membrana. Per diverse eliche biologicamente rilevanti — provenienti da proteine come Amphiphysin, CHMP4B, Endophilin-B1 e Huntingtin — la nuova piattaforma e la lettura tradizionale forniscono curve di legame e preferenze lipidiche molto simili, rivelando persino nuove tendenze come un legame più forte dell’elica di Amphiphysin a membrane ricche di colesterolo.
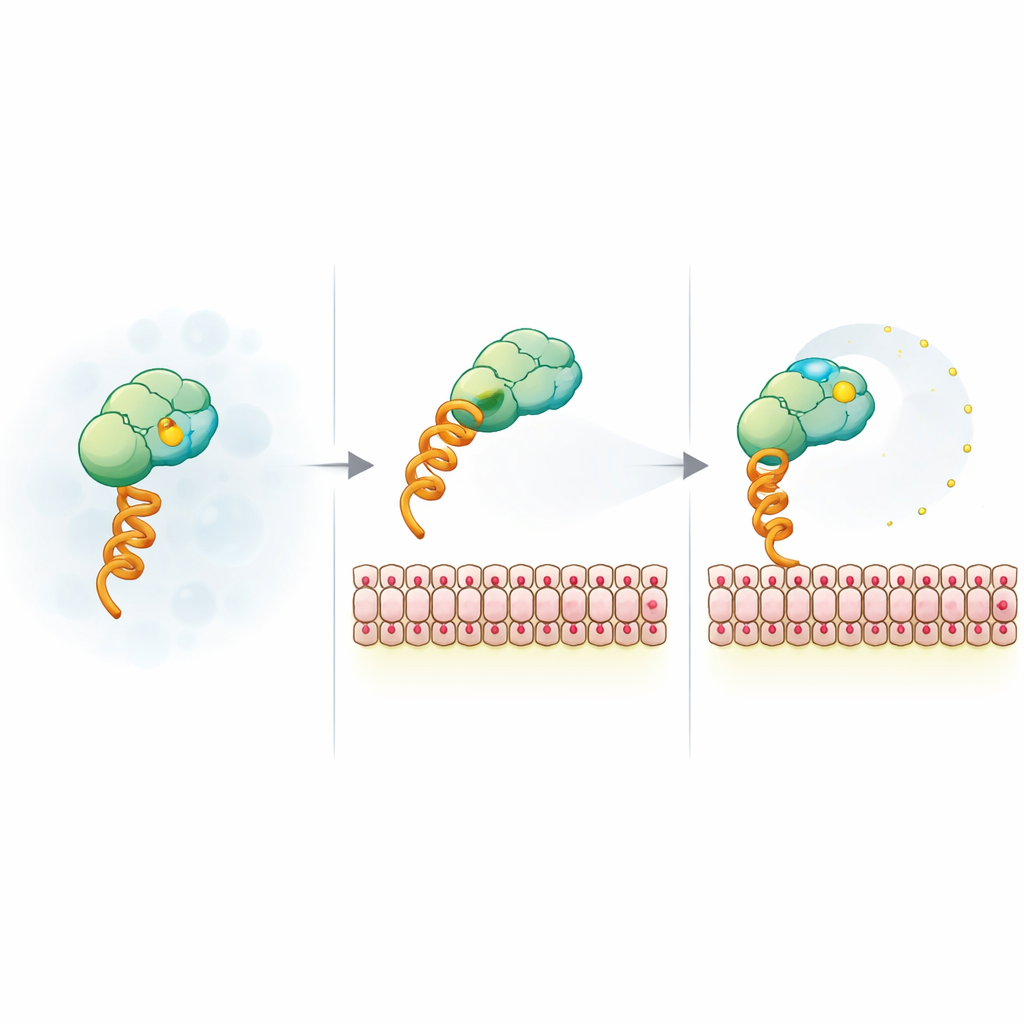
Come la carica della membrana libera il reporter fluorescente
Per spiegare il segnale inaspettato, il gruppo ha ridotto il sistema a un costrutto modello che si lega alle membrane tramite un generico tag di istidina e un lipide che chela il nichel. Hanno quindi variato la dimensione delle vescicole, la carica superficiale, il livello di sale e il tipo di colorante. La diminuzione dell’anisotropia si è dimostrata insensibile alla dimensione delle vescicole e all’identità del fluoroforo, ma altamente sensibile alla carica negativa della membrana e allo screening salino, indicando un’origine elettrostatica. Misure di fluorescenza risolta nel tempo hanno mostrato che, quando il costrutto è legato a membrane cariche, il colorante acquista mobilità locale aggiuntiva nonostante l’intero complesso ruoti più lentamente. Esperimenti di risonanza magnetica nucleare e FRET hanno inoltre suggerito che patch cariche positivamente sulla superficie di SUMO possono agire da tenaglie temporanee per il colorante carico negativamente; il legame a una membrana carica e la mutazione di queste patch allentano questo vincolo, permettendo al colorante di oscillare più liberamente e abbassando l’anisotropia.
Mappare le preferenze di membrana su larga scala
Poiché la diminuzione dell’anisotropia è robusta e riproducibile, può essere usata come reporter comodo del legame anziché considerata un artefatto problematico. Array di vescicole che differiscono per tipo di lipide e curvatura possono essere sondati rapidamente, permettendo ai ricercatori di individuare quali combinazioni di lipidi e forme attraggono meglio una data elica. La piattaforma funziona particolarmente bene per membrane cariche negativamente, comuni negli organelli coinvolti nel traffico e nella produzione energetica. Ingegnerizzando varianti della proteina veicolatrice con carica modificata, gli autori estendono l’intervallo utile di condizioni verso livelli salini più fisiologici e membrane con cariche più sottili, ampliando ulteriormente l’applicabilità del metodo.
Cosa significa per la comprensione dell’indirizzamento cellulare
In termini pratici, questo lavoro fornisce un nuovo «lettore» ad alto rendimento per i codici postali molecolari che guidano le proteine all’indirizzo cellulare corretto. Invece di affidarsi a esperimenti ingombranti e lenti, gli scienziati possono ora schermare molte eliche e ricette di membrane in parallelo, usando una semplice firma ottica che si inverte in modo inatteso ma ben compreso. Nel tempo, questo dovrebbe rendere possibile decodificare quali pattern di amminoacidi corrispondono a quali ambienti lipidici, chiarendo come le cellule usino queste piccole eliche flessibili per smistare proteine, rimodellare membrane e controllare segnali e percorsi di traffico vitali.
Citazione: Margaritakis, A., Qian, M., Johnson, D.H. et al. Recombinant protein platform for high-throughput investigation of peptide-liposome interactions via fluorescence anisotropy depolarization. Commun Chem 9, 165 (2026). https://doi.org/10.1038/s42004-026-01994-9
Parole chiave: peptidi leganti le membrane, anisotropia di fluorescenza, eliche anfipatiche, vescicole lipidiche, interazioni proteina–membrana