Clear Sky Science · es
Plataforma de proteína recombinante para la investigación de alto rendimiento de interacciones péptido-lipósoma mediante despolarización por anisotropía de fluorescencia
Cómo las piezas proteicas cambiantes encuentran las membranas adecuadas
Dentro de cada célula, innumerables envíos, señales y procesos de reciclaje dependen de que las proteínas aterricen en la membrana correcta en el momento oportuno. Muchas de estas proteínas usan tramos cortos y flexibles que solo se pliegan en hélices ordenadas cuando entran en contacto con una membrana apropiada. Este artículo presenta una forma nueva y más rápida de estudiar cómo esas piezas que cambian de forma reconocen membranas específicas, usando una señal óptica sorprendente como un reportero incorporado.
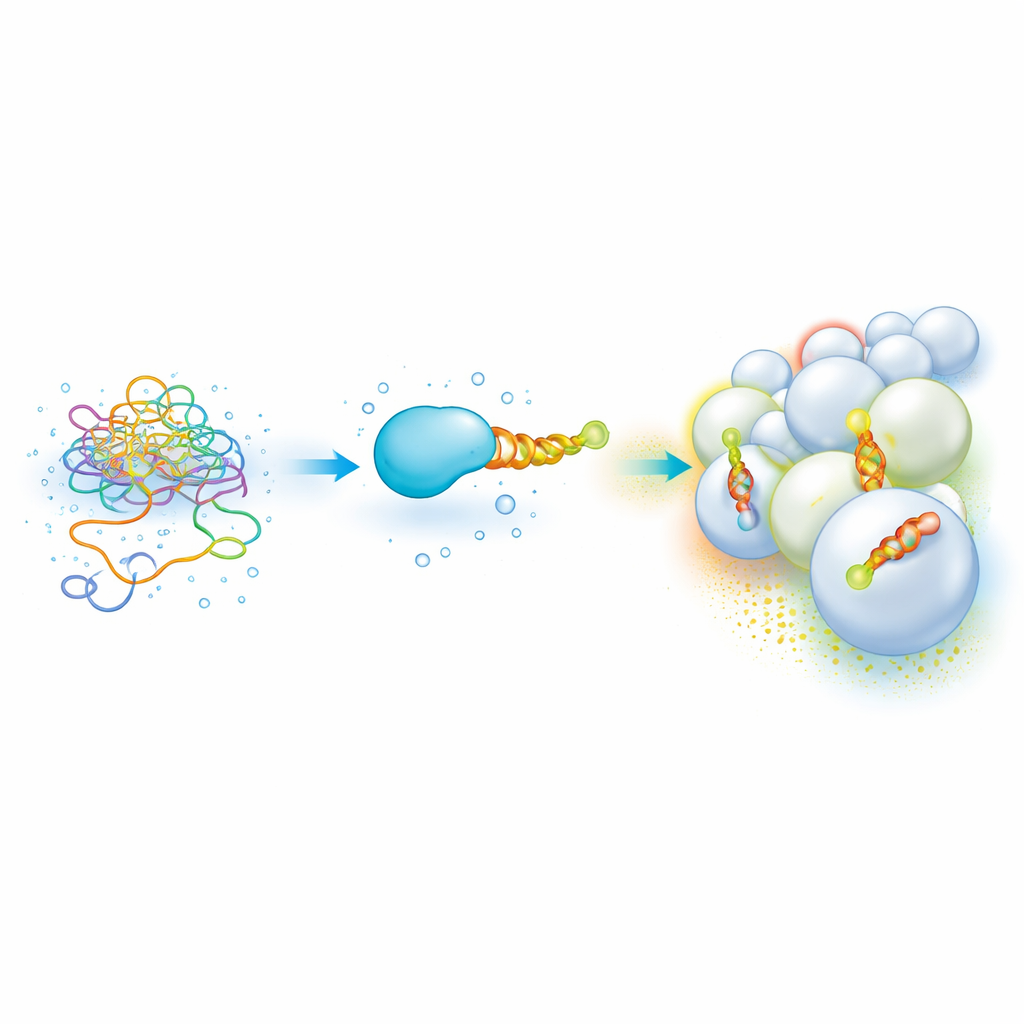
Extremos proteicos flexibles que leen los “códigos postales” de la membrana
Muchas proteínas celulares importantes llevan un segmento corto y no estructurado que se convierte en una hélice anfipática —una espiral con un lado apolar y otro polar— cuando se ancla a una membrana. Estas hélices ayudan a las proteínas a distinguir un orgánulo de otro al detectar la composición lipídica y la curvatura, permitiéndoles localizarse en sitios como endosomas o mitocondrias. Pero aisladas, estas piezas pegajosas y parcialmente apolares son difíciles de manejar: tienden a agregarse, precipitar y requieren métodos lentos y consumidores de muestra para medir cuán fuertemente se unen a distintas membranas. En consecuencia, ha sido difícil construir un “código” claro que vincule la secuencia de la hélice con su preferencia por membranas.
Una plataforma proteica modular que ilumina la unión
Los autores diseñaron una plataforma recombinante que doma estas hélices indómitas y facilita medir sus preferencias de membrana en paralelo. Cada hélice prueba se fusiona a una proteína portadora bien comportada llamada SUMO, que mejora la solubilidad y la expresión, y se etiqueta en el extremo con un colorante fluorescente. Cuando el constructo se mezcla con vesículas lipídicas artificiales y se lee en un lector de microplacas común, los investigadores siguen la anisotropía de fluorescencia —una medida de cuánto la emisión del tinte “recuerda” su polarización, que depende de la libertad de rotación del tinte. Mediante la titulación de muchas mezclas lipídicas y tamaños de vesículas en volúmenes pequeños, construyen rápidamente curvas de unión para distintas hélices a lo largo de un amplio paisaje de composiciones y curvaturas de membrana.
Una señal contraintuitiva que aun así informa sobre la unión
Intuitivamente, uno esperaría que cuando un pequeño constructo proteína-tinte se une a una vesícula mucho mayor, su rotación se ralentice y la anisotropía aumente. En cambio, los autores observan lo contrario: la anisotropía disminuye a medida que aumenta la unión. Comprobaron si este comportamiento extraño seguía reflejando la asociación real a la membrana comparándolo con un método clásico basado en la fluorescencia de triptófano, que informa cuán profundamente una hélice se entierra en el núcleo apolar de la membrana. Para varias hélices de relevancia biológica —provenientes de proteínas como Amphiphysin, CHMP4B, Endophilin-B1 y Huntingtina—, la nueva plataforma y la lectura tradicional producen curvas de unión y preferencias lipídicas muy similares, llegando incluso a revelar tendencias nuevas, como una unión más fuerte de la hélice de Amphiphysin a membranas ricas en colesterol.
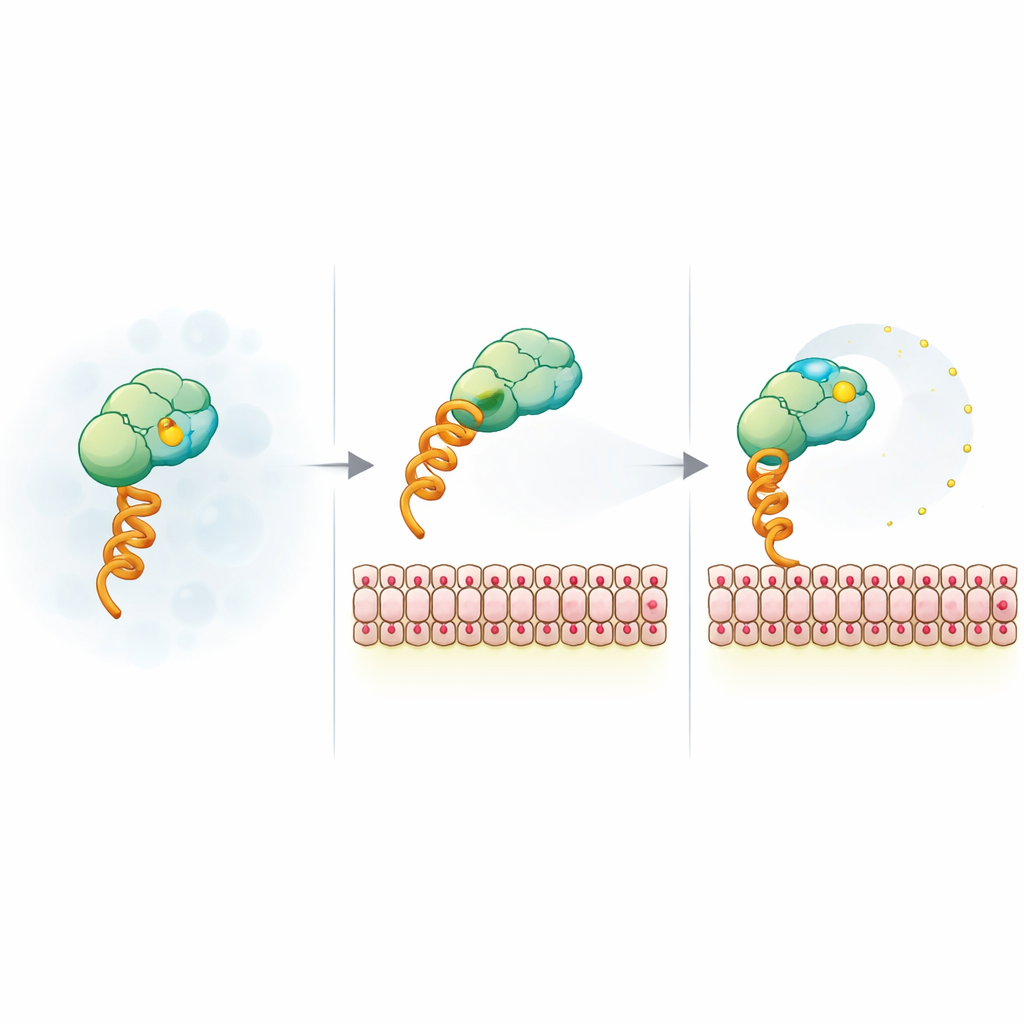
Cómo la carga de la membrana libera al reportero fluorescente
Para explicar la señal inesperada, el equipo redujo el sistema a un constructo modelo que se une a membranas mediante una etiqueta genérica de histidina y un lípido quelante de níquel. Luego variaron el tamaño de las vesículas, la carga superficial, el nivel de sal y el tipo de tinte. La caída de anisotropía resultó insensible al tamaño de las vesículas y a la identidad del fluoróforo, pero muy sensible a la carga negativa de la membrana y al apantallamiento por sal, lo que apunta a un origen electrostático. Mediciones de fluorescencia resueltas en el tiempo mostraron que, cuando está unido a membranas cargadas, el tinte gana movilidad local extra aunque el conjunto completo rote más despacio. Experimentos de resonancia magnética nuclear y FRET sugirieron además que parches positivos en la superficie del SUMO pueden actuar como ataduras temporales para el tinte cargado negativamente; la unión a una membrana cargada y la mutación de estos parches aflojan esta atadura, permitiendo que el tinte oscile con más libertad y reduciendo la anisotropía.
Cartografiar preferencias de membrana a gran escala
Debido a que la disminución de anisotropía es robusta y reproducible, puede usarse como un reportero conveniente de unión en lugar de considerarse un artefacto problemático. Matrices de vesículas que difieren en tipo lipídico y curvatura pueden sondearse rápidamente, permitiendo a los investigadores identificar qué combinaciones de lípidos y formas atraen mejor a una hélice dada. La plataforma funciona especialmente bien para membranas con carga negativa, comunes en orgánulos implicados en el tráfico y la producción de energía. Mediante la ingeniería de variantes de la proteína portadora con cargas alteradas, los autores extienden el rango útil de condiciones hacia niveles de sal más fisiológicos y membranas con cargas sutiles, ampliando aún más el alcance del método.
Qué implica esto para entender el direccionamiento celular
En términos cotidianos, este trabajo proporciona un nuevo “lector” de alto rendimiento para los códigos postales moleculares que guían a las proteínas hacia la dirección celular correcta. En lugar de depender de experimentos voluminosos y lentos, los científicos pueden ahora cribar muchas hélices y recetas de membrana en paralelo, usando una firma óptica simple que se invierte en una dirección inesperada pero bien comprendida. Con el tiempo, esto debería permitir decodificar qué patrones de aminoácidos corresponden a qué entornos lipídicos, aclarando cómo las células usan estas hélices pequeñas y flexibles para clasificar proteínas, remodelar membranas y controlar vías vitales de señalización y tráfico.
Cita: Margaritakis, A., Qian, M., Johnson, D.H. et al. Recombinant protein platform for high-throughput investigation of peptide-liposome interactions via fluorescence anisotropy depolarization. Commun Chem 9, 165 (2026). https://doi.org/10.1038/s42004-026-01994-9
Palabras clave: péptidos de unión a membrana, anisotropía de fluorescencia, hélices anfipáticas, vesículas lipídicas, interacciones proteína–membrana