Clear Sky Science · tr
Fleoresan anizotropi depolarizasyonu ile peptit-lipozom etkileşimlerinin yüksek verimli araştırılması için rekombinant protein platformu
Şekil Değiştiren Protein Parçacıkları Doğru Zarları Nasıl Bulur
Her hücrenin içinde sayısız teslimat, sinyal ve geri dönüşüm olayı, proteinlerin doğru zamanda doğru zar üzerinde konumlanmasına bağlıdır. Bu proteinlerin birçoğu, uygun bir zara dokunduklarında ancak o zaman düz bir heliks haline gelen kısa, gevşek bölgeler kullanır. Bu makale, bu şekil değiştiren parçaların belirli zarları nasıl tanıdığını incelemek için şaşırtıcı bir optik sinyali yerleşik bir raporlayıcı olarak kullanan yeni ve daha hızlı bir yöntem sunuyor.
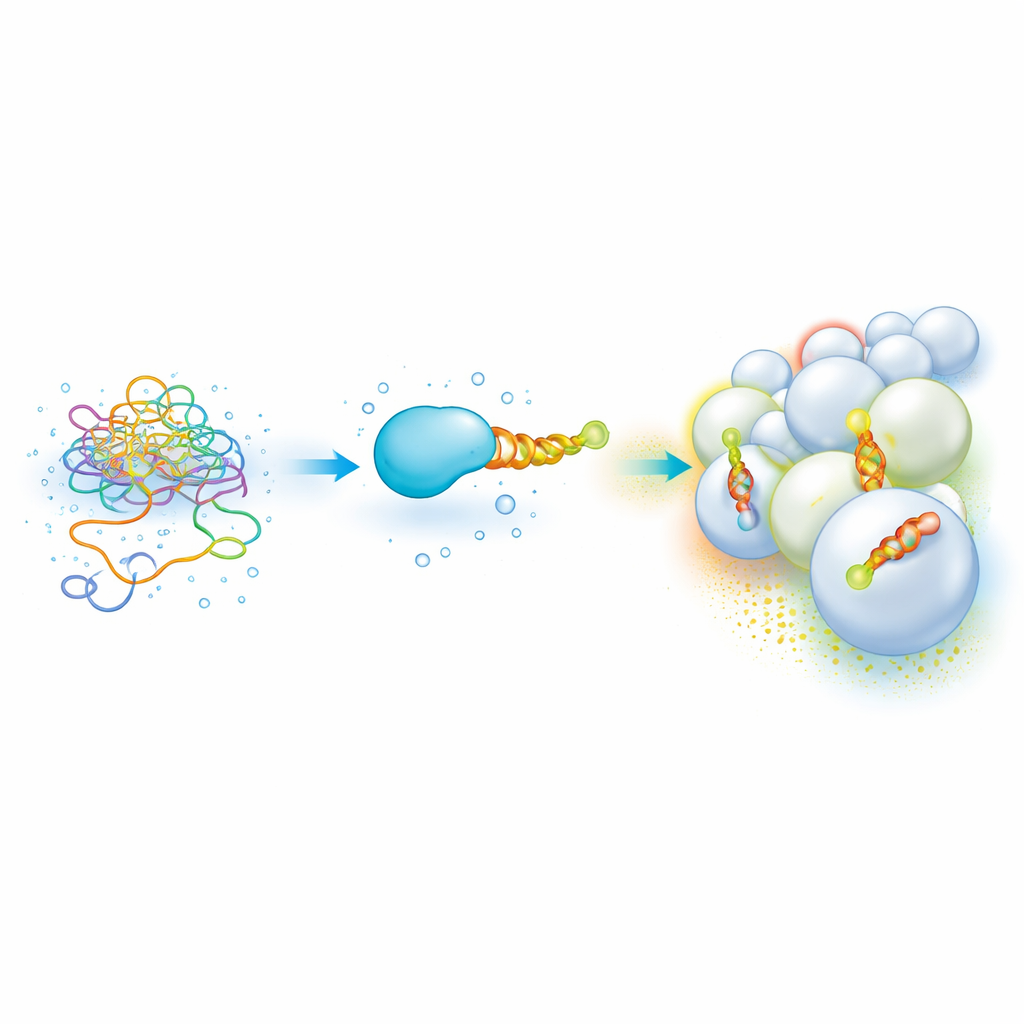
Zar "Posta Kodlarını" Okuyan Esnek Protein Uçları
Pek çok önemli hücresel protein, zara bağlandığında amfipatik bir heliks—bir tarafı yağlı, diğer tarafı sulu olan bir spiral—haline gelen kısa, yapısız bir segmente sahiptir. Bu heliksler, lipid bileşimi ve eğriliği algılayarak proteinlerin endozom veya mitokondri gibi belirli organellere yönelmesine yardımcı olur. Ancak tek başlarına alındıklarında bu yapışkan, kısmen yağlı parçalar çalışması zor olabilir: kümeleşir, çözünürlük sorunları çıkarır ve farklı zarlarla ne kadar sıkı bağlandıklarını ölçmek için yavaş ve çok örnek gerektiren yöntemler gerektirirler. Sonuç olarak, heliks dizisini zar tercihiyle bağlayan açık bir “kod” oluşturmak zordu.
Bağlanmayı Aydınlatan Modüler Bir Protein Platformu
Yazarlar, bu uyumsuz heliksleri kontrol altına alan ve onların zar tercihlerini paralel olarak ölçmeyi kolaylaştıran bir rekombinant platform geliştirdiler. Her test heliksi, çözünürlüğü ve ekspresyonu artıran SUMO adlı iyi davranışlı bir taşıyıcı proteine füzyonlanır ve uçta bir floresan boya ile etiketlenir. Yapay lipid vezikülleri ile karıştırıldığında ve sıradan bir mikroplak okuyucuda ölçüldüğünde, araştırmacılar floresans anizotropisini izler—bunun anlamı, boyanın ışık yayılımının polarizasyonunu ne kadar “hatırladığıdır”; bu, boyanın ne kadar serbest dönebileceğine bağlıdır. Küçük hacimlerde çok sayıda lipid karışımı ve vezikül boyutu titrasyonu yaparak, farklı heliksler için geniş bir zar bileşimi ve eğriliği yelpazesinde hızla bağlanma eğrileri oluştururlar.
Hâlâ Bağlanmayı Bildiren Tersine Mantıklı Bir Sinyal
Sezgisel olarak, küçük bir protein-boya yapısı çok daha büyük bir veziküle bağlandığında dönmesinin yavaşlayacağını ve anizotropinin artacağını bekleriz. Bunun yerine yazarlar, bağlanma arttıkça anizotropinin azaldığını gözlüyorlar. Bu garip davranışın gerçek zar birleşmesini hâlâ izleyip izlemediğini test etmek için, bir heliksin yağlı zarın çekirdeğine ne kadar derin gömüldüğünü bildiren klasik bir yöntem olan triptofan floresansına dayanan yöntemle karşılaştırdılar. Amphiphysin, CHMP4B, Endophilin-B1 ve Huntingtin gibi proteinlerden birkaç biyolojik olarak ilginç heliks için yeni platform ve geleneksel okuma yakından eşleşen bağlanma eğrileri ve lipid tercihleri verdi; hatta Amphiphysin heliksinin kolesterolce zengin zarlara daha güçlü bağlanması gibi yeni eğilimleri ortaya koydu.
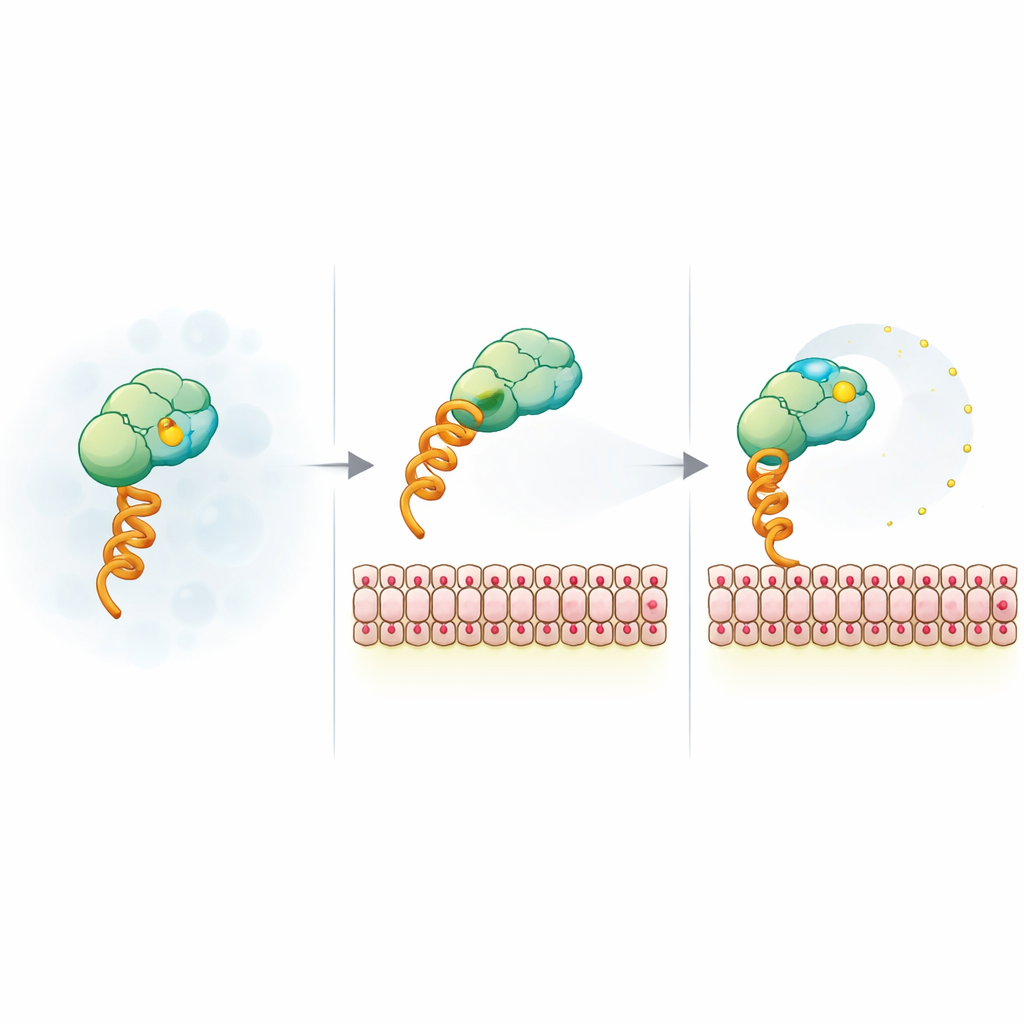
Zar Yükünün Floresan Raporlayıcıyı Nasıl Serbest Bıraktığı
Beklenmeyen sinyali açıklamak için ekip sistemi, bir histidin etiketi ve nikel şelatlayıcı bir lipid aracılığıyla zar bağlanan basit bir model yapıya indirgedi. Ardından vezikül boyutu, yüzey yükü, tuz seviyesi ve boya türünü değiştirdiler. Anizotropi düşüşünün vezikül boyutuna ve fluorofor kimliğine duyarsız, fakat negatif zar yüküne ve tuzla taramaya karşı çok duyarlı olduğu ortaya çıktı; bu da elektrostatik bir kökeni işaret etti. Zaman çözünürlüklü floresans ölçümleri, yüklü zarlarla bağlandığında boyanın, tüm kompleks daha yavaş dönerken bile ekstra yerel hareketliliğe kavuştuğunu gösterdi. Nükleer manyetik rezonans ve FRET deneyleri, SUMO yüzeyindeki pozitif yamaların negatif yüklü boya için geçici bir tutturucu gibi davranabileceğini öne sürdü; yüklü bir zara bağlanma ve bu yamaların mutasyona uğratılması, bu tutturucuyu gevşeterek boyanın daha serbest sallanmasına izin veriyor ve anizotropiyi düşürüyor.
Ölçekli Zar Tercihlerini Haritalama
Anizotropi azalması sağlam ve tekrarlanabilir olduğu için, bunun sorunlu bir artefakt olarak ele alınmasından ziyade bağlanmanın kullanışlı bir raporlayıcısı olarak kullanılması mümkündür. Lipid türü ve eğriliği farklı dizilmiş vezikül dizileri hızla denenebilir ve araştırmacıların belirli bir heliksi en çok çeken lipid ve şekil kombinasyonlarını belirlemesine olanak tanır. Platform özellikle trafik ve enerji üretimiyle ilişkili organellerde yaygın olan negatif yüklü zarlar için iyi çalışır. Taşıyıcı proteinin yükü değiştirilmiş varyantlarını tasarlayarak yazarlar, yöntemin kullanılabilir koşullarını daha fizyolojik tuz seviyelerine ve hafifçe yüklü zarlarına doğru genişleterek yöntemin erişimini daha da artırırlar.
Hücresel Hedeflemenin Anlaşılması Açısından Ne Anlama Gelir
Günlük terimlerle, bu çalışma proteinleri doğru hücresel adrese yönlendiren moleküler posta kodları için yeni, yüksek verimli bir “okuyucu” sağlar. Hantal, yavaş deneylere dayanmak yerine, bilim insanları artık birçok heliksi ve zar tarifini paralel olarak tarayabilir; bu, beklenmedik ama iyi anlaşılan bir yönde tersine dönen basit bir optik imza kullanılarak yapılır. Zaman içinde, bu yaklaşım hangi amino asit desenlerinin hangi lipid ortamlarına karşılık geldiğini çözmeyi mümkün kılmalı; hücrelerin bu küçük, esnek heliksleri proteinleri sıralamak, zarları yeniden şekillendirmek ve hayati sinyal ve trafi̇k yollarını kontrol etmek için nasıl kullandığını açıklığa kavuşturacaktır.
Atıf: Margaritakis, A., Qian, M., Johnson, D.H. et al. Recombinant protein platform for high-throughput investigation of peptide-liposome interactions via fluorescence anisotropy depolarization. Commun Chem 9, 165 (2026). https://doi.org/10.1038/s42004-026-01994-9
Anahtar kelimeler: zar-bağlayıcı peptitler, fluoresans anizotropisi, amfipatik heliksler, lipid veziküller, protein–zar etkileşimleri