Clear Sky Science · sv
Rekombinant proteinplattform för storskalig studie av peptid-liposome-interaktioner via depolarisation av fluorescensanisotropi
Hur formförändrande proteinbitar hittar rätt membran
Inuti varje cell är otaliga leveranser, signaler och återvinningsprocesser beroende av att proteiner landar på rätt membran vid rätt tidpunkt. Många av dessa proteiner använder korta, rörliga segment som endast veckas till ordnade helixar när de rör vid ett lämpligt membran. Denna artikel introducerar ett nytt, snabbare sätt att studera hur dessa formförändrande delar känner igen specifika membran, med hjälp av en överraskande optisk signal som inbyggd rapportör.
Flexibla proteindelar som läser membranets "postnummer"
Många viktiga cellulära proteiner bär på ett kort, ostrukturerat segment som blir en amfipatisk helix — en spiral med en oljig sida och en vattnig sida — när det fäster vid ett membran. Dessa helixar hjälper proteiner att skilja ett organell från ett annat genom att känna av lipidernas sammansättning och kurvatur, vilket gör att de kan rikta in sig på platser som endosomer eller mitokondrier. Men på egen hand är dessa klibbiga, delvis oljiga bitar svåra att hantera: de klumpar ihop sig, fälls ut och kräver långsamma, provkrävande metoder för att mäta hur tätt de binder till olika membran. Som en följd har det varit svårt att bygga en tydlig "kod" som kopplar helixsekvens till membranpreferens.
En modulär proteinplattform som lyser upp bindning
Författarna byggde en rekombinant plattform som tämjer dessa svårhanterliga helixar och gör deras membranval enkla att mäta parallellt. Varje testhelix är fuserad med ett välbeteende bärarprotein kallat SUMO, vilket ökar lösligheten och uttrycket, och är märkt i den fjärran änden med en fluorescerande färg. När konstrukten blandas med artificiella lipidvesiklar och avläses i en vanlig mikrotiterplatta följer forskarna fluorescensanisotropi — ett mått på hur mycket färgens ljusemission "kommer ihåg" sin polarisering, vilket beror på hur fritt färgen kan rotera. Genom att titrera många lipidblandningar och vesikelstorlekar i små volymer bygger de snabbt bindningskurvor för olika helixar över ett brett landskap av membransammansättningar och kurvaturer.
En kontraintuitiv signal som ändå rapporterar bindning
Intuitivt skulle man förvänta sig att när en liten protein-färg-konstruktion binder till en mycket större vesikel, så bromsas dess rotation och anisotropin ökar. Istället observerar författarna det motsatta: anisotropin minskar när bindningen ökar. De testade om detta ovanliga beteende ändå följer verklig membranassociering genom att jämföra det med en klassisk metod baserad på tryptofanflorescens, som rapporterar hur djupt en helix begraver sig i membranets oljiga kärna. För flera biologiskt relevanta helixar — från proteiner som Amphiphysin, CHMP4B, Endophilin-B1 och Huntingtin — ger den nya plattformen och den traditionella avläsningen tätt matchande bindningskurvor och lipidpreferenser, och avslöjar även nya trender såsom starkare Amphiphysin-helixbindning till kolesterolrika membran.
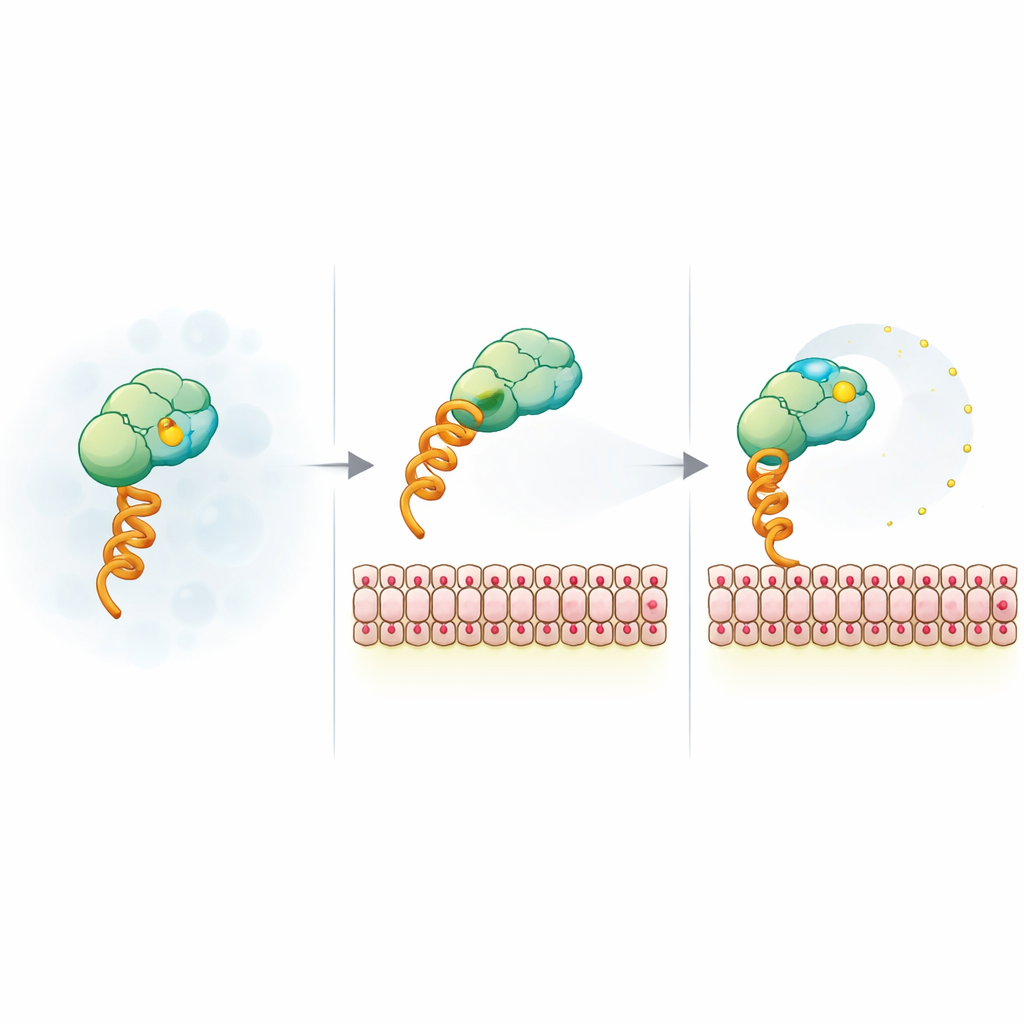
Hur membranets laddning frigör den fluorescerande rapportören
För att förklara den oväntade signalen förenklade teamet systemet till en modellkonstruktion som binder membran via en generisk histidin-tag och en nickelkelaterande lipid. De varierade sedan vesikelstorlek, ytladdning, salthalt och färgtyp. Anisotropifallet visade sig vara okänsligt för vesikelstorlek och fluoroforidentitet men mycket känsligt för negativ membranladdning och skärmning av salt, vilket pekar på ett elektrostatisk ursprung. Tidsupplösta fluorescensmätningar visade att när konstrukten är bunden till laddade membran får färgen ökad lokal rörlighet trots att hela komplexet roterar långsammare. Kärnmagnetisk resonans och FRET-experiment föreslog vidare att positiva yttäckor på SUMO-ytan kan fungera som tillfälliga fästen för den negativt laddade färgen; bindning till ett laddat membran och mutation av dessa yttäckor båda lossar detta fäste, vilket låter färgen vicka friare och sänker anisotropin.
Kartläggning av membranpreferenser i stor skala
Eftersom anisotropiminskningen är robust och reproducerbar kan den användas som en bekväm rapportör för bindning snarare än betraktas som ett problematiskt artefakt. Arrayer av vesiklar som skiljer sig i lipidtyp och kurvatur kan undersökas snabbt, vilket gör att forskare kan peka ut vilka kombinationer av lipider och former som bäst attraherar en given helix. Plattformen fungerar särskilt väl för negativt laddade membran, som är vanliga i organeller involverade i transport och energiproduktion. Genom att konstruera bärare med förändrad laddning utvidgar författarna det användbara spannet av förhållanden mot mer fysiologiska saltnivåer och subtilt laddade membran, vilket ytterligare breddar metodens räckvidd.
Vad detta betyder för förståelsen av cellulär riktning
I vardagliga termer ger detta arbete en ny, höggenomströmning "läsare" för de molekylära postnummer som styr proteiner till rätt cellulära adress. Istället för att förlita sig på otympliga, långsamma experiment kan forskare nu skärma många helixar och membranrecept i parallell, med hjälp av en enkel optisk signatur som vänder i en oväntad men väl förstådd riktning. Med tiden bör detta göra det möjligt att avkoda vilka aminosyremönster som motsvarar vilka lipidmiljöer, och klargöra hur celler använder dessa små, flexibla helixar för att sortera proteiner, omforma membran och kontrollera viktiga signal- och transportvägar.
Citering: Margaritakis, A., Qian, M., Johnson, D.H. et al. Recombinant protein platform for high-throughput investigation of peptide-liposome interactions via fluorescence anisotropy depolarization. Commun Chem 9, 165 (2026). https://doi.org/10.1038/s42004-026-01994-9
Nyckelord: membranbindande peptider, fluorescensanisotropi, amfipatiska helixar, lipidvesiklar, protein–membran-interaktioner