Clear Sky Science · pt
Plataforma de proteína recombinante para investigação de alto rendimento de interações peptídeo-lipossoma via despolarização de anisotropia de fluorescência
Como pedaços proteicos que mudam de forma encontram as membranas certas
Dentro de cada célula, inúmeras entregas, sinais e eventos de reciclagem dependem de proteínas que aterrissam na membrana correta no momento certo. Muitas dessas proteínas utilizam trechos curtos e flexíveis que só se dobram em hélices ordenadas quando tocam uma membrana adequada. Este artigo apresenta uma nova maneira, mais rápida, de estudar como esses pedaços que mudam de forma reconhecem membranas específicas, usando um sinal óptico surpreendente como um repórter embutido.
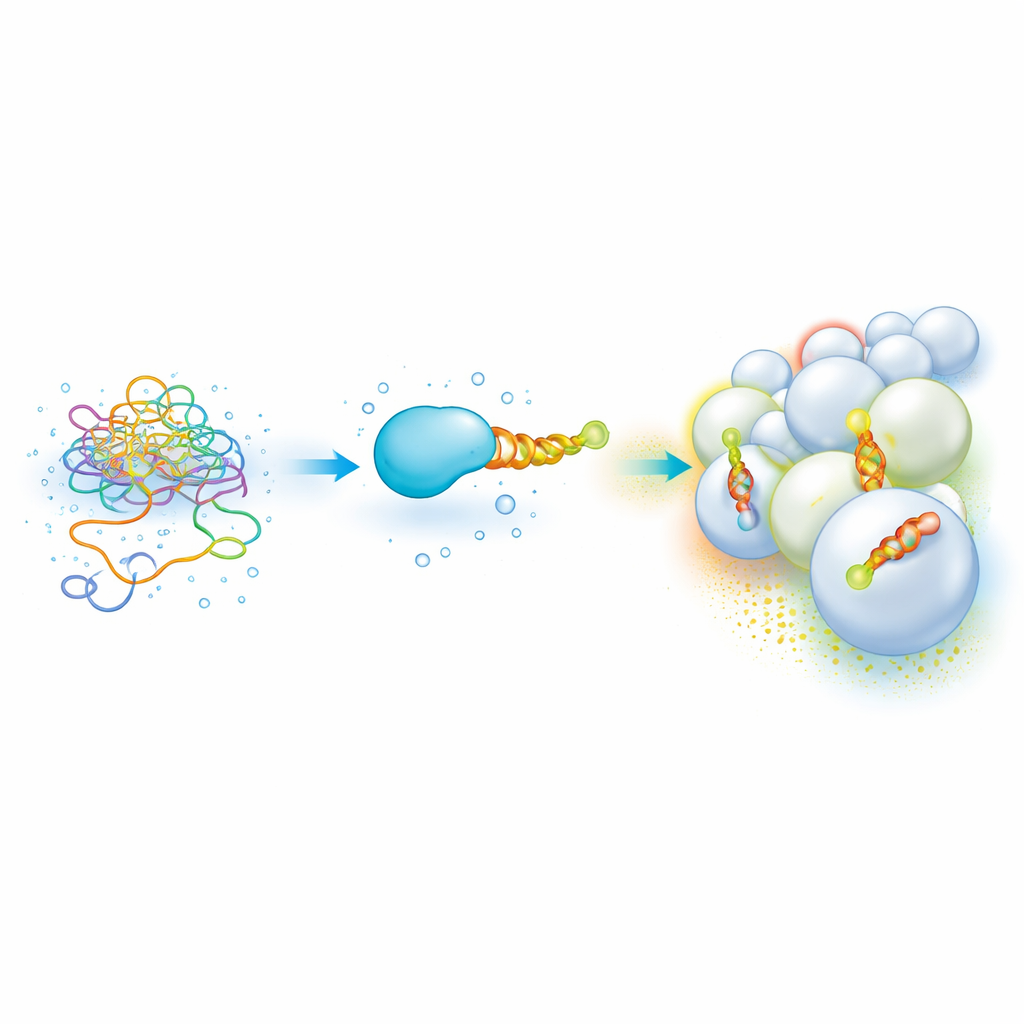
Extremidades proteicas flexíveis que leem os “códigos postais” das membranas
Muitas proteínas celulares importantes carregam um segmento curto e não estruturado que se torna uma hélice anfipática — uma espiral com um lado oleoso e um lado aquoso — assim que se ancora em uma membrana. Essas hélices ajudam as proteínas a distinguir um organelo de outro ao sentir a composição lipídica e a curvatura, permitindo que elas se dirijam a locais como endossomos ou mitocôndrias. Mas isoladas, essas partes pegajosas e parcialmente oleosas são difíceis de manusear: aglomeram-se, precipitam e exigem métodos lentos e que consomem muitas amostras para medir quão fortemente se ligam a diferentes membranas. Como resultado, construir um “código” claro que vincule sequência de hélice à preferência por membrana tem sido difícil.
Uma plataforma proteica modular que acende ao ligar
Os autores construíram uma plataforma recombinante que doma essas hélices indomáveis e torna suas escolhas de membrana fáceis de medir em paralelo. Cada hélice teste é fundida a uma proteína carreadora bem comportada chamada SUMO, que aumenta a solubilidade e a expressão, e é rotulada na extremidade oposta com um corante fluorescente. Quando o construto é misturado com vesículas lipídicas artificiais e lido em um leitor de microplacas comum, os pesquisadores acompanham a anisotropia de fluorescência — uma medida de quanto a emissão de luz do corante “lembra” sua polarização, que depende de quão livremente o corante pode girar. Ao titular muitas misturas de lipídios e tamanhos de vesículas em pequenos volumes, eles constroem rapidamente curvas de ligação para diferentes hélices através de um amplo panorama de composições e curvaturas de membrana.
Um sinal contraintuitivo que ainda relata ligação
Intuitivamente, esperaria-se que, quando um pequeno construto proteína-corante se liga a uma vesícula muito maior, sua rotação diminuísse e a anisotropia aumentasse. Em vez disso, os autores observam o oposto: a anisotropia diminui conforme a ligação aumenta. Eles testaram se esse comportamento estranho ainda acompanha a associação real com a membrana comparando-o com um método clássico baseado na fluorescência de triptofano, que informa o quão profundamente uma hélice se enterra no núcleo oleoso da membrana. Para várias hélices biologicamente relevantes — de proteínas como Amfifisina, CHMP4B, Endophilin-B1 e Huntingtin — a nova plataforma e a leitura tradicional fornecem curvas de ligação e preferências lipídicas muito semelhantes, revelando até novas tendências, como a ligação mais forte da hélice de Amfifisina a membranas ricas em colesterol.
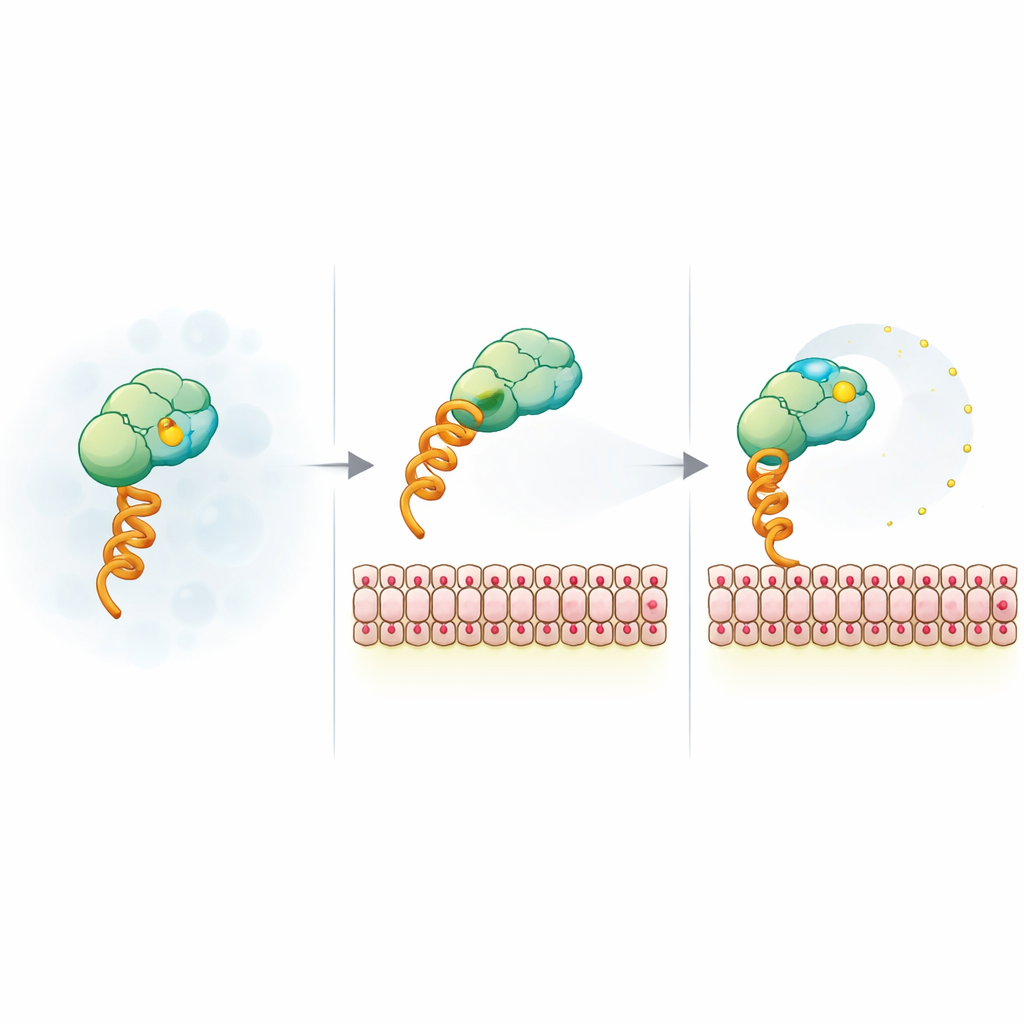
Como a carga da membrana libera o repórter fluorescente
Para explicar o sinal inesperado, a equipe reduziu o sistema a um construto modelo que se liga a membranas via uma etiqueta genérica de histidina e um lipídio quelante de níquel. Eles então variaram o tamanho das vesículas, a carga superficial, o nível de sal e o tipo de corante. A queda de anisotropia mostrou-se insensível ao tamanho da vesícula e à identidade do fluoróforo, mas altamente sensível à carga negativa da membrana e ao efeito de blindagem pelo sal, apontando para uma origem eletrostática. Medições de fluorescência em tempo-resolvido mostraram que, quando ligado a membranas carregadas, o corante ganha mobilidade local extra apesar de todo o complexo girar mais lentamente. Experimentos de ressonância magnética nuclear e FRET sugeriram ainda que manchas positivas na superfície do SUMO podem agir como amarras temporárias para o corante carregado negativamente; a ligação a uma membrana carregada e a mutação dessas manchas afrouxam essa amarra, permitindo que o corante oscile com mais liberdade e reduzindo a anisotropia.
Mapeando preferências de membrana em larga escala
Porque a diminuição da anisotropia é robusta e reprodutível, ela pode ser usada como um repórter conveniente de ligação em vez de tratada como um artefato problemático. Matrizes de vesículas que diferem em tipo de lipídio e curvatura podem ser sondadas rapidamente, permitindo que os pesquisadores identifiquem quais combinações de lipídios e formas atraem melhor uma dada hélice. A plataforma funciona especialmente bem para membranas carregadas negativamente, que são comuns em organelos envolvidos no tráfego e na produção de energia. Ao projetar variantes da proteína carreadora com cargas alteradas, os autores estendem a faixa útil de condições em direção a níveis de sal mais fisiológicos e membranas sutilmente carregadas, ampliando ainda mais o alcance do método.
O que isso significa para entender o direcionamento celular
Em termos práticos, este trabalho fornece um novo “leitor” de alto rendimento para os códigos postais moleculares que guiam proteínas ao endereço celular correto. Em vez de depender de experimentos volumosos e lentos, os cientistas agora podem triagemar muitas hélices e receitas de membrana em paralelo, usando uma assinatura óptica simples que se inverte de maneira inesperada, porém bem compreendida. Com o tempo, isso deve viabilizar decodificar quais padrões de aminoácidos correspondem a quais ambientes lipídicos, esclarecendo como as células usam essas hélices pequenas e flexíveis para classificar proteínas, remodelar membranas e controlar vias vitais de sinalização e tráfego.
Citação: Margaritakis, A., Qian, M., Johnson, D.H. et al. Recombinant protein platform for high-throughput investigation of peptide-liposome interactions via fluorescence anisotropy depolarization. Commun Chem 9, 165 (2026). https://doi.org/10.1038/s42004-026-01994-9
Palavras-chave: peptídeos de ligação à membrana, anisotropia de fluorescência, hélices anfipáticas, vesículas lipídicas, interações proteína–membrana