Clear Sky Science · ru
Рекомбинантная платформа белков для высокопроизводительного изучения взаимодействий пептид–липосома методом деполяризации флуоресцентной анизотропии
Как меняющиеся по форме фрагменты белков находят нужные мембраны
Внутри каждой клетки бесчисленные доставки, сигналы и процессы утилизации зависят от того, что белки попадают на нужную мембрану в нужный момент. Многие из этих белков используют короткие, гибкие участки, которые сворачиваются в аккуратные спирали только при контакте с подходящей мембраной. В этой статье представлена новая, более быстрая методика изучения того, как такие «меняющиеся» фрагменты распознают специфические мембраны, с использованием неожиданного оптического сигнала в роли встроенного репортера.
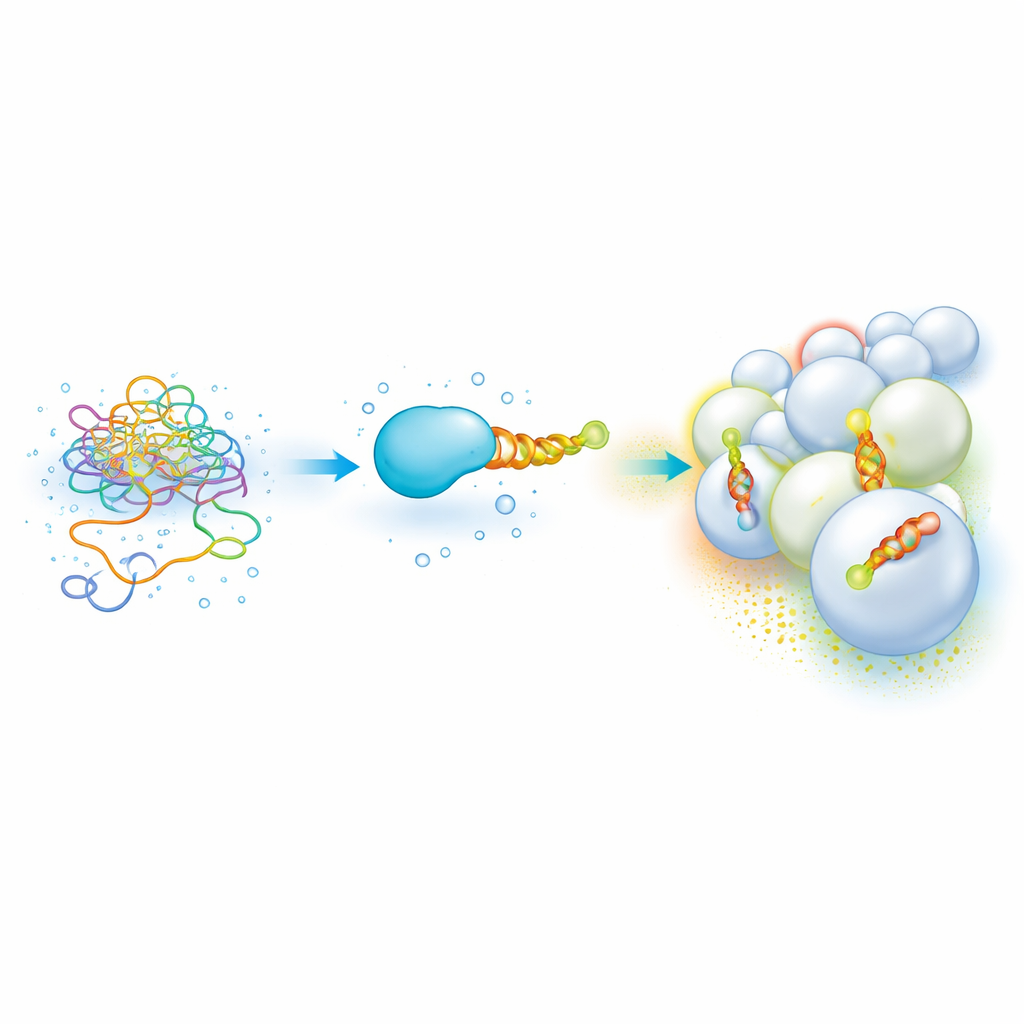
Гибкие концы белков, читающие «почтовые индексы» мембран
Многие важные клеточные белки несут короткий неструктурированный участок, который превращается в амфипатическую спираль — виток с одной жировой и одной водной стороной — когда он прикрепляется к мембране. Эти спирали помогают белкам различать органеллы по составу липидов и кривизне, позволяя им «домашиться» в таких местах, как эндосомы или митохондрии. Но сами по себе эти липкие, частично гидрофобные фрагменты трудно изучать: они склонны к агрегации и осаждению и требуют медленных, объёмных методов для измерения силы связывания с разными мембранами. В результате построение чёткого «кода», связывающего последовательность спирали с предпочтением мембраны, было затруднено.
Модульная белковая платформа, которая «зажигается» при связывании
Авторы создали рекомбинантную платформу, которая укрощает эти неуправляемые спирали и делает выбор мембраны простым для параллельного измерения. Каждый тестовый фрагмент спирали сливается с хорошо выражаемым носителем — белком SUMO, который повышает растворимость и экспрессию, а на дальнем конце конструкции установлен флуоресцентный краситель. При смешивании конструкции с искусственными липидными везикулами и измерении в обычном микропланшетном считывателе исследователи отслеживают флуоресцентную анизотропию — меру того, насколько испускание красителя «помнит» поляризацию света, что зависит от свободы вращения красителя. Титруя множество липидных смесей и размеров везикул в небольших объёмах, они быстро получают кривые связывания для разных спиралей по широкой палитре составов мембран и кривизн.
Парадоксальный сигнал, который всё же отражает связывание
Интуитивно ожидаешь, что при связывании маленькой конструкции белок–краситель с гораздо большей везикулой её вращение замедлится и анизотропия повысится. Вместо этого авторы наблюдают обратное: анизотропия уменьшается по мере усиления связывания. Они проверили, действительно ли это странное поведение отражает ассоциацию с мембраной, сравнив его с классическим методом на основе флуоресценции триптофана, который показывает, насколько глубоко спираль погружается в гидрофобное ядро мембраны. Для нескольких биологически значимых спиралей — из белков, таких как амфифизин, CHMP4B, Endophilin-B1 и гантингтин — новая платформа и традиционный метод дают похожие кривые связывания и предпочтения по липидам, даже выявляя новые тенденции, например более сильное связывание спирали амфифизина с мембранами, богатыми холестерином.
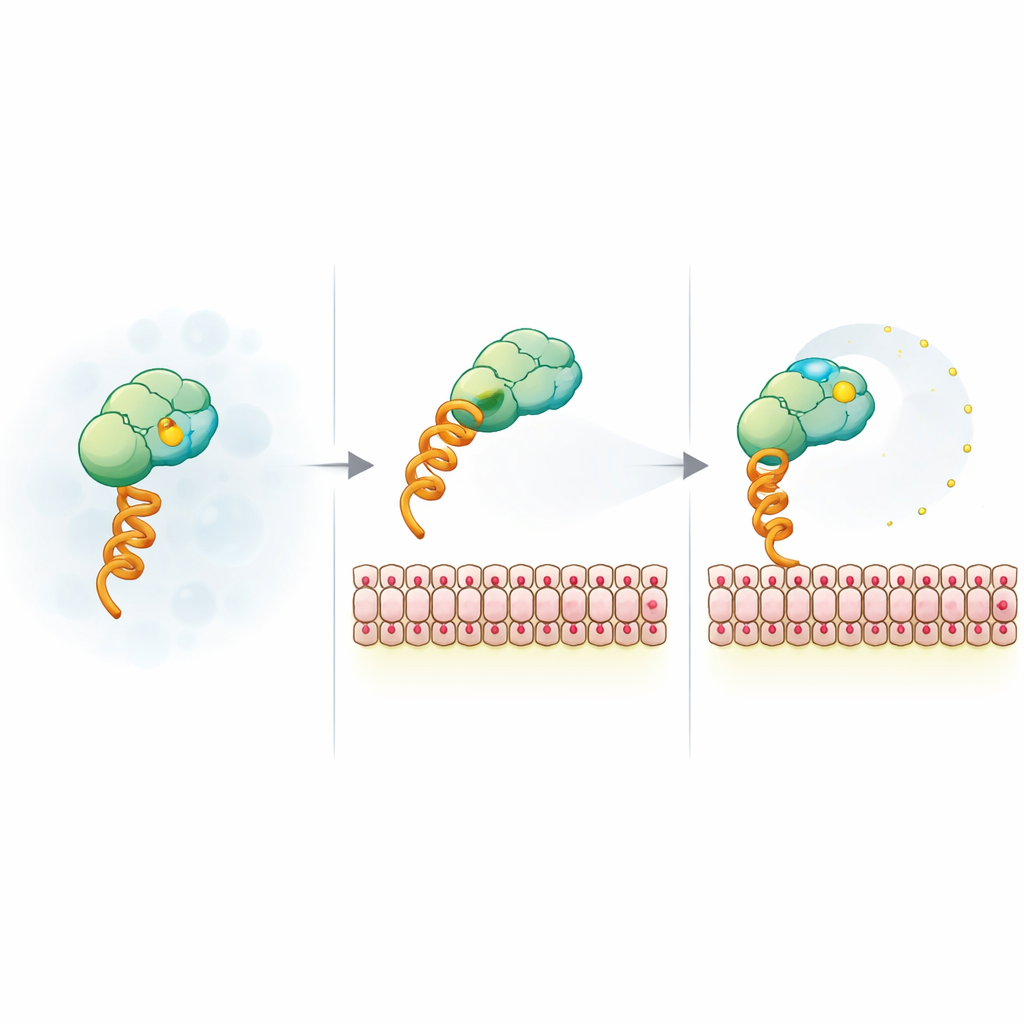
Как заряд мембраны освобождает флуоресцентный репортер
Чтобы объяснить неожиданный сигнал, команда упростила систему до модельной конструкции, которая связывается с мембраной через универсальную гистидиновую метку и липид, хелатирующий никель. Затем они варьировали размер везикул, поверхностный заряд, концентрацию соли и тип красителя. Снижение анизотропии оказалось нечувствительным к размеру везикул и типу флюорофора, но очень чувствительным к отрицательному заряду мембраны и экранированию ионами соли, что указывает на электростатическое происхождение. Времяразрешённые флуоресцентные измерения показали, что при связывании с заряженными мембранами краситель приобретает дополнительную локальную подвижность, несмотря на то, что весь комплекс вращается медленнее. ЯМР и эксперименты FRET дополнительно показали, что положительные участки на поверхности SUMO могут действовать как временные привязи для отрицательно заряженного красителя; связывание с заряженной мембраной и мутации этих участков ослабляют эту привязь, позволяя красителю свободнее «шаркаться» и снижая анизотропию.
Картирование предпочтений мембран в большом масштабе
Поскольку уменьшение анизотропии устойчиво и воспроизводимо, его можно использовать как удобный индикатор связывания, а не рассматривать как проблемный артефакт. Массивы везикул с разными типами липидов и кривизной можно быстро исследовать, позволяя точно определить, какие сочетания липидов и форм лучше притягивают данную спираль. Платформа особенно хорошо работает для отрицательно заряженных мембран, которые распространены в органеллах, участвующих в траффикинге и энергетическом обмене. За счёт конструирования вариантов носителя с изменённым зарядом авторы расширяют полезный диапазон условий в сторону более физиологических уровней соли и слабо заряженных мембран, ещё больше увеличивая охват метода.
Что это означает для понимания клеточной таргетности
Проще говоря, эта работа предоставляет новый высокопроизводительный «сканер» молекулярных почтовых индексов, которые направляют белки к правильному клеточному адресу. Вместо громоздких, медленных экспериментов учёные теперь могут скринировать многие спирали и рецепты мембран параллельно, используя простой оптический признак, который меняет знак неожиданно, но в понятном ключе. Со временем это позволит расшифровать, какие аминокислотные шаблоны соответствуют каким липидным средам, прояснив, как клетки используют эти небольшие гибкие спирали для сортировки белков, изменения формы мембран и управления важными сигнальными и транспортными путями.
Цитирование: Margaritakis, A., Qian, M., Johnson, D.H. et al. Recombinant protein platform for high-throughput investigation of peptide-liposome interactions via fluorescence anisotropy depolarization. Commun Chem 9, 165 (2026). https://doi.org/10.1038/s42004-026-01994-9
Ключевые слова: пептиды, связывающиеся с мембраной, флуоресцентная анизотропия, амфипатические спирали, липидные везикулы, взаимодействия белок–мембрана