Clear Sky Science · pl
Rekombinacyjna platforma białkowa do badań wysokoprzepustowych interakcji peptyd–liposom za pomocą depolaryzacji anizotropii fluorescencji
Jak kształtujące się fragmenty białek znajdują właściwe błony
Wewnątrz każdej komórki liczne dostawy, sygnały i procesy recyklingu zależą od tego, by białka trafiały na odpowiednią błonę we właściwym czasie. Wiele z tych białek wykorzystuje krótkie, luźne odcinki, które dopiero po zetknięciu z odpowiednią błoną układają się w porządne helisy. W artykule przedstawiono nową, szybszą metodę badania, jak te „kształtujące się” fragmenty rozpoznają konkretne błony, wykorzystując zaskakujący sygnał optyczny jako wbudowany reporter.
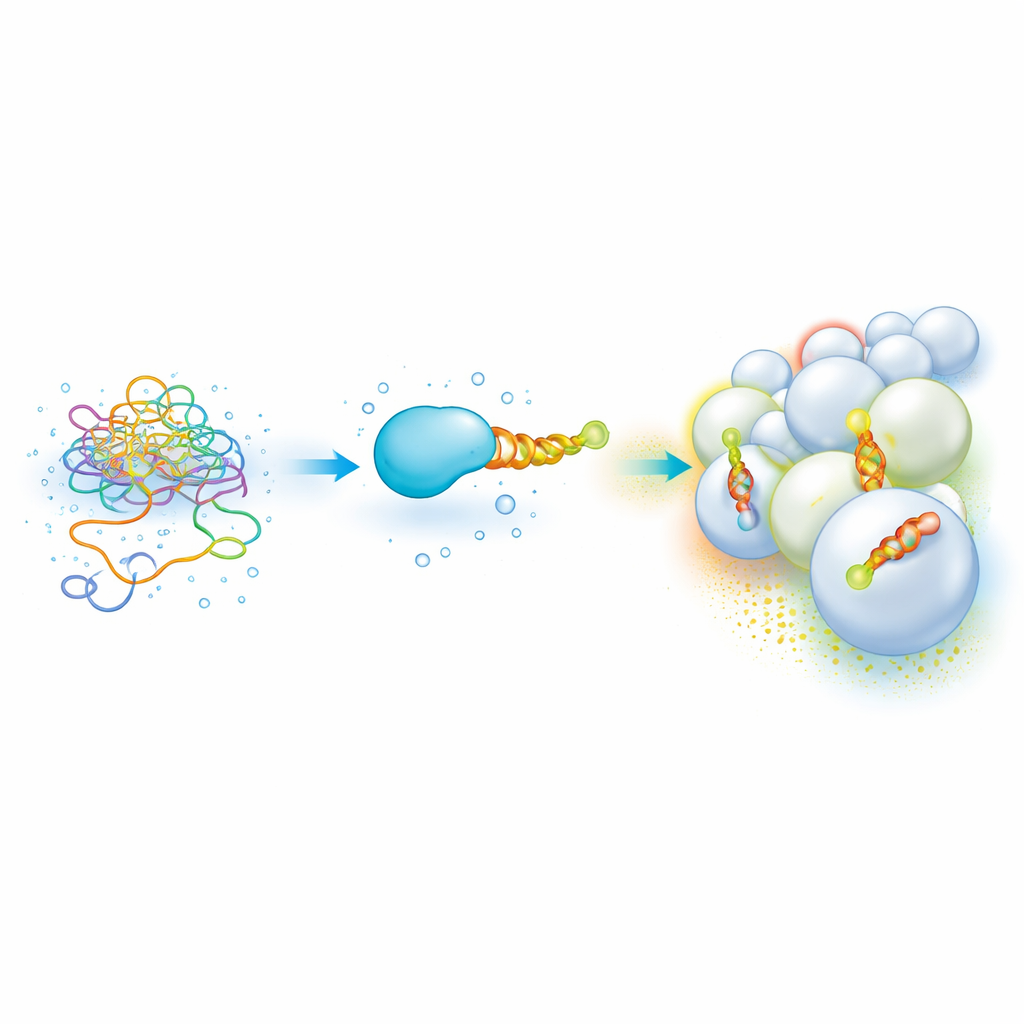
Elastyczne końce białek czytające „kody pocztowe” błon
Wiele ważnych białek komórkowych ma krótki, nieuporządkowany fragment, który po przyłączeniu do błony staje się helisą amfipatyczną — spiralą z jedną tłustą i jedną wodną stroną. Te helisy pomagają białkom rozróżniać organelle, wyczuwając skład lipidowy i krzywiznę błony, dzięki czemu mogą lokalizować się w miejscach takich jak endosomy czy mitochondria. Jednak same w sobie te lepkie, częściowo hydrofobowe fragmenty trudno jest badać: zbrylają się, wytrącają i wymagają powolnych, dużych objętościowo metod, by zmierzyć ich powinowactwo do różnych błon. W efekcie trudne było zbudowanie przejrzystego „kodu” łączącego sekwencję helisy z preferencją błonową.
Modularna platforma białkowa, która świeci przy wiązaniu
Autorzy skonstruowali rekombinacyjną platformę, która okiełznaje te niepokorne helisy i umożliwia łatwe, równoległe pomiary ich wyborów błonowych. Każda testowa helisa jest złączona z dobrze zachowującym się nośnikiem białkowym SUMO, co zwiększa rozpuszczalność i ekspresję, a na drugim końcu posiada znacznik fluorescencyjny. Po zmieszaniu konstruktu z sztucznymi pęcherzykami lipidowymi i odczycie na standardowym czytniku mikropłytkowym badacze śledzą anizotropię fluorescencji — miarę tego, na ile emisja światła barwnika „pamięta” swoją polaryzację, co zależy od swobody obrotu barwnika. Poprzez miareczkowanie wielu mieszanin lipidowych i rozmiarów pęcherzyków w małych objętościach szybko budują krzywe wiązania dla różnych helis w szerokim spektrum składu i krzywizny błon.
Przeciwintuicyjny sygnał, który jednak raportuje wiązanie
Intuicyjnie oczekiwalibyśmy, że gdy mały konstruk białko–barwnik przyłącza się do dużo większego pęcherzyka, jego rotacja spowolni i anizotropia wzrośnie. Zamiast tego autorzy obserwują przeciwne zjawisko: anizotropia zmniejsza się wraz ze wzrostem wiązania. Sprawdzili, czy to dziwne zachowanie nadal odzwierciedla rzeczywiste kojarzenie z błoną, porównując je z klasyczną metodą opartą na fluorescencji tryptofanu, która sygnalizuje, jak głęboko helisa zanurza się w hydrofobowym wnętrzu błony. Dla kilku biologicznie istotnych helis — pochodzących z białek takich jak Amphiphysin, CHMP4B, Endophilin-B1 i Huntingtin — nowa platforma i tradycyjny odczyt dają zbliżone krzywe wiązania i preferencje lipidowe, ujawniając nawet nowe trendy, np. silniejsze wiązanie helisy Amphiphysin z błonami bogatymi w cholesterol.
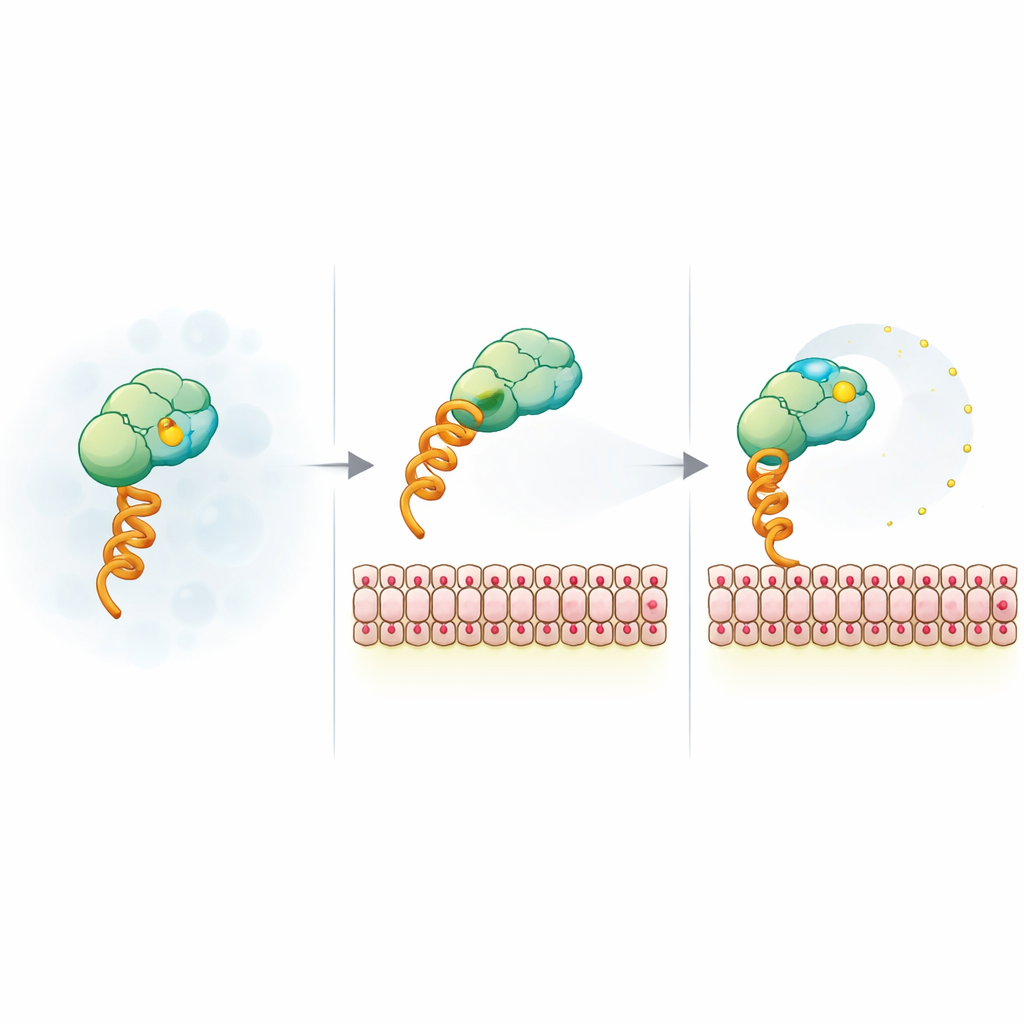
Jak ładunek błony uwalnia fluorescencyjny reporter
Aby wyjaśnić nieoczekiwany sygnał, zespół uprościł układ do modelowego konstruktu, który wiąże błony przez ogólny znacznik histydynowy i lipid chelatujący nikiel. Następnie zmieniali rozmiar pęcherzyków, ładunek powierzchniowy, poziom soli i typ barwnika. Spadek anizotropii okazał się niewrażliwy na rozmiar pęcherzyków i tożsamość fluoroforu, ale silnie zależny od ujemnego ładunku błony i ekranowania przez sól, co wskazuje na pochodzenie elektrostatyczne. Pomiary fluorescencji czasowo-rozdzielczej wykazały, że po związaniu z naładowanymi błonami barwnik zyskuje dodatkową lokalną ruchomość, mimo że cały kompleks obraca się wolniej. Badania metodami rezonansu magnetycznego jądrowego (NMR) i FRET sugerowały ponadto, że dodatnie „plamy” na powierzchni SUMO mogą pełnić rolę tymczasowych kotwic dla ujemnie naładowanego barwnika; przyłączenie do naładowanej błony i mutacje tych miejsc polarnych osłabiają tę kotwicę, pozwalając barwnikowi na większe kołysanie i obniżając anizotropię.
Mapowanie preferencji błonowych na dużą skalę
Ponieważ spadek anizotropii jest trwały i powtarzalny, można go wykorzystać jako wygodny reporter wiązania, zamiast traktować jako problematyczny artefakt. Tablice pęcherzyków różniące się rodzajem lipidów i krzywizną można szybko przebadać, co pozwala badaczom precyzyjnie określić, które kombinacje lipidów i kształtów najbardziej przyciągają daną helisę. Platforma działa szczególnie dobrze dla błon o ładunku ujemnym, które są powszechne w organellach zaangażowanych w transport i produkcję energii. Poprzez inżynierię wariantów nośnika o zmienionym ładunku autorzy poszerzają użyteczny zakres warunków w kierunku bardziej fizjologicznych poziomów soli i subtelnie naładowanych błon, dodatkowo rozszerzając zakres zastosowań metody.
Co to oznacza dla zrozumienia celowania w komórce
Mówiąc obrazowo, ta praca dostarcza nowego, wysokoprzepustowego „czytnika” molekularnych kodów pocztowych, które kierują białka do właściwego adresu komórkowego. Zamiast polegać na ciężkich, wolnych eksperymentach, naukowcy mogą teraz równolegle przesiewać wiele helis i receptur błon, korzystając z prostego sygnału optycznego, który zmienia się w zaskakującym, ale dobrze zrozumiałym kierunku. Z czasem powinno to umożliwić odczytanie, jakie wzorce aminokwasowe odpowiadają którym środowiskom lipidowym, wyjaśniając, jak komórki wykorzystują te małe, elastyczne helisy do segregowania białek, przekształcania błon i kontrolowania kluczowych szlaków sygnalizacyjnych oraz transportowych.
Cytowanie: Margaritakis, A., Qian, M., Johnson, D.H. et al. Recombinant protein platform for high-throughput investigation of peptide-liposome interactions via fluorescence anisotropy depolarization. Commun Chem 9, 165 (2026). https://doi.org/10.1038/s42004-026-01994-9
Słowa kluczowe: peptydy wiążące błony, anizotropia fluorescencji, helisy amfipatyczne, pęcherzyki lipidowe, interakcje białko–błona