Clear Sky Science · de
Rekombinante Proteinplattform zur Hochdurchsatz-Untersuchung von Peptid-Liposom-Wechselwirkungen mittels Fluoreszenzanisotropie-Depolarisation
Wie gestaltwandelnde Proteinfragmente die richtigen Membranen finden
In jeder Zelle hängen zahllose Transporte, Signalübertragungen und Recyclingvorgänge davon ab, dass Proteine zur richtigen Zeit an der richtigen Membran anlanden. Viele dieser Proteine nutzen kurze, flexible Abschnitte, die erst beim Kontakt mit einer passenden Membran zu wohlgeordneten Helices ausfalten. Diese Arbeit stellt eine neue, schnellere Methode vor, um zu untersuchen, wie diese gestaltwandelnden Stücke spezifische Membranen erkennen — und nutzt dafür ein überraschendes optisches Signal als integrierten Reporter.
Flexible Proteinenden, die Membran-„Postleitzahlen“ lesen
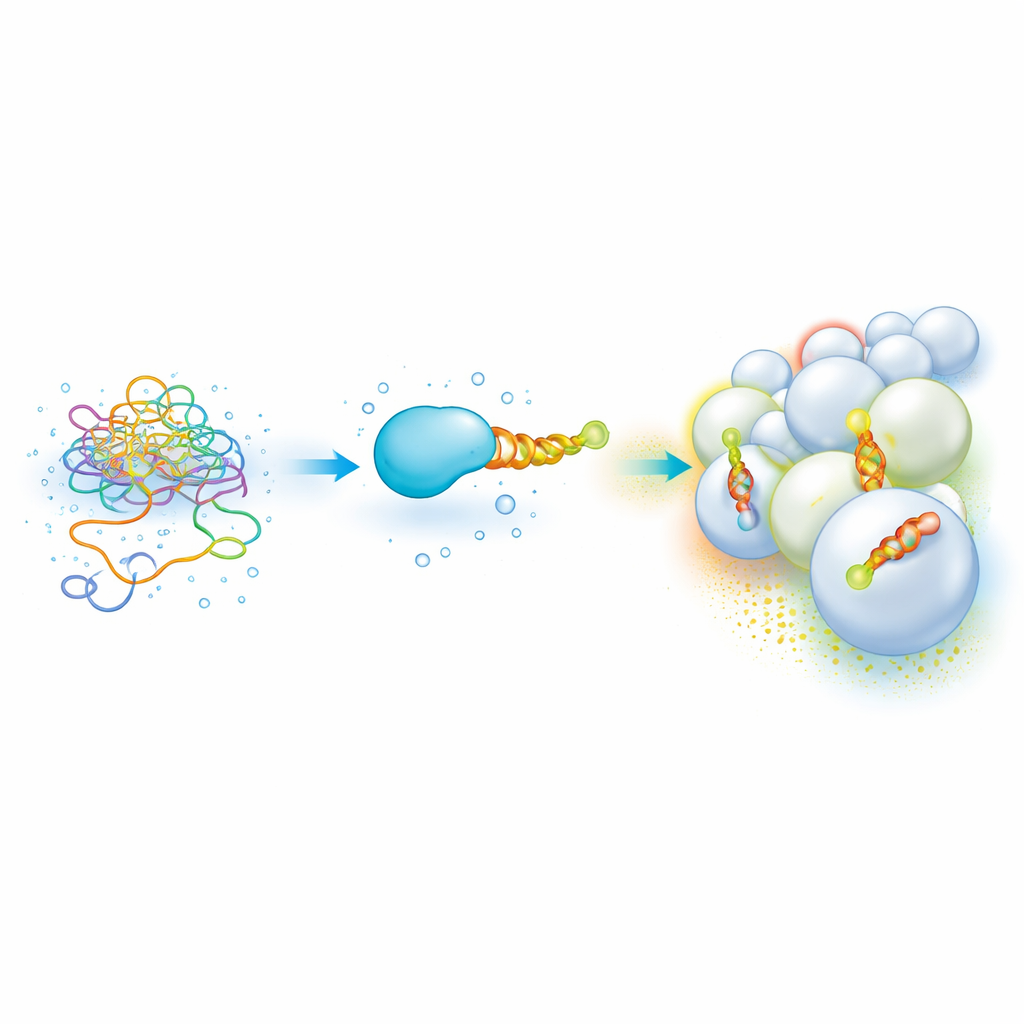
Viele wichtige zelluläre Proteine tragen ein kurzes, ungeordnetes Segment, das beim Andocken an eine Membran zu einer amphipathischen Helix wird — einer Spirale mit einer öligen und einer wässrigen Seite. Diese Helices helfen Proteinen, ein Organell vom anderen zu unterscheiden, indem sie die Lipidzusammensetzung und Krümmung wahrnehmen und so Orte wie Endosomen oder Mitochondrien ansteuern. Allein genommen sind diese klebrigen, teilöligen Abschnitte jedoch schwer zu handhaben: Sie neigen zur Aggregation, Fällung und erfordern langsame, materialintensive Methoden, um ihre Bindungsstärke an verschiedene Membranen zu messen. Daher war es schwierig, einen klaren „Code“ zu entwickeln, der Helixsequenz und Membranpräferenz verknüpft.
Eine modulare Proteinplattform, die Bindung sichtbar macht
Die Autoren entwickelten eine rekombinante Plattform, die diese widerspenstigen Helices zähmt und ihre Membranzuordnungen parallel messbar macht. Jede Testhelix wird an ein gut handhabbares Trägerprotein namens SUMO fusioniert, das Löslichkeit und Expression verbessert, und am entfernten Ende mit einem Fluoreszenzfarbstoff markiert. Mischt man den Konstrukt mit künstlichen Lipidvesikeln und liest ihn in einem gängigen Mikroplattenleser aus, verfolgt man die Fluoreszenzanisotropie — ein Maß dafür, wie sehr die Lichtexcitation des Farbstoffs ihre Polarisation „beibehält“, was davon abhängt, wie frei sich der Farbstoff drehen kann. Durch Titration vieler Lipidmischungen und Vesikelgrößen in kleinen Volumina lassen sich schnell Bindungskurven für verschiedene Helices über ein breites Spektrum von Membranzusammensetzungen und Krümmungen erstellen.
Ein kontraintuitives Signal, das dennoch Bindung meldet
Intuitiv würde man erwarten, dass ein kleiner Protein-Farbstoff-Konstrukt beim Binden an ein viel größeres Vesikel langsamer rotiert und die Anisotropie steigt. Stattdessen beobachten die Autoren das Gegenteil: Die Anisotropie nimmt ab, wenn die Bindung zunimmt. Sie prüften, ob dieses ungewöhnliche Verhalten trotzdem echte Membranassoziation abbildet, indem sie es mit einer klassischen Methode auf Basis von Tryptophan-Fluoreszenz verglichen, die meldet, wie tief eine Helix in den öligen Membrankern eintaucht. Für mehrere biologisch relevante Helices — aus Proteinen wie Amphiphysin, CHMP4B, Endophilin-B1 und Huntingtin — liefern die neue Plattform und der traditionelle Messwert eng übereinstimmende Bindungskurven und Lipidpräferenzen und zeigen sogar neue Trends, etwa eine stärkere Bindung der Amphiphysin-Helix an cholesterinreiche Membranen.
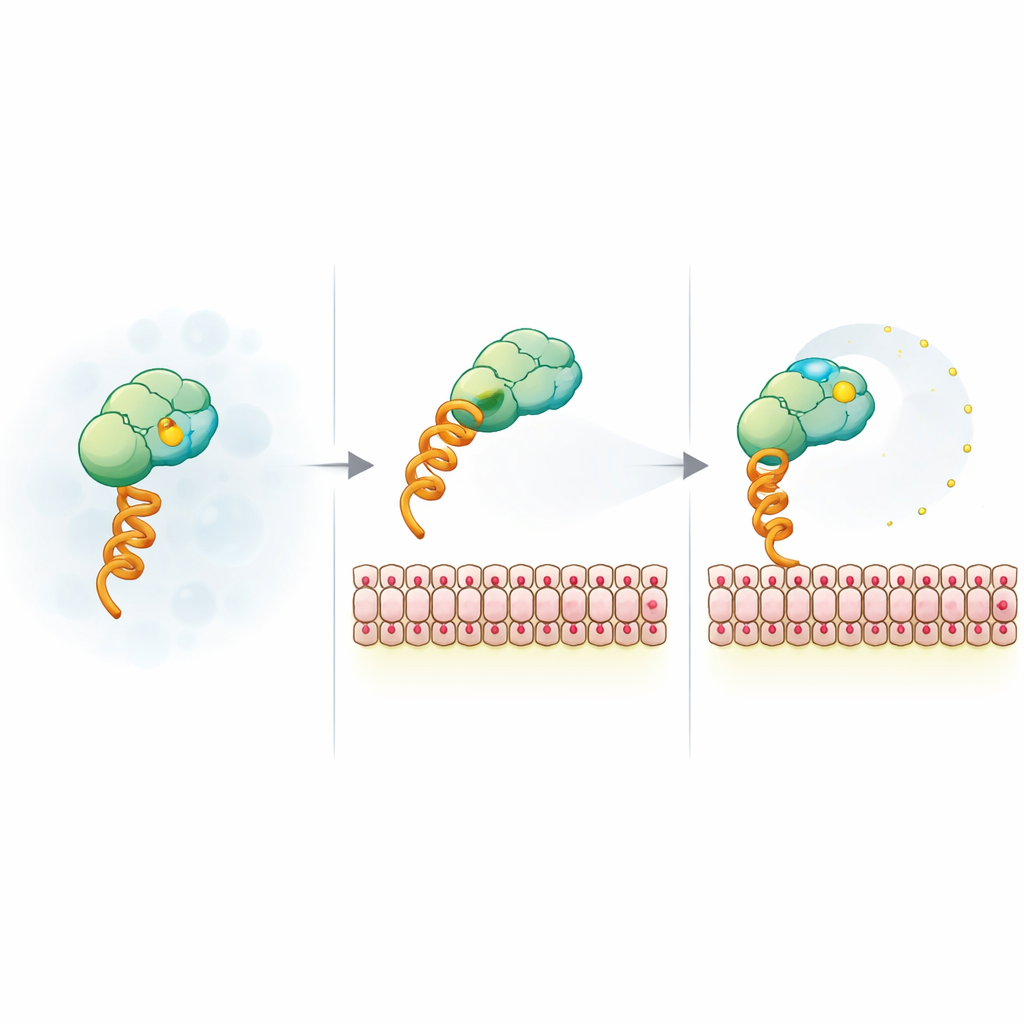
Wie Membranladung den fluoreszenten Reporter befreit
Um das unerwartete Signal zu erklären, reduzierten die Forscher das System auf einen Modellkonstrukt, das über einen generischen His-Tag und ein nickel-chelatierendes Lipid an Membranen bindet. Sie variierten Vesikelgröße, Oberflächenladung, Salzkonzentration und Farbstofftyp. Der Abfall der Anisotropie erwies sich als unabhängig von Vesikelgröße und Fluorophoridentität, war jedoch sehr sensibel gegenüber negativer Membranladung und Abschirmung durch Salz, was auf eine elektrostatische Ursache hinweist. Zeitaufgelöste Fluoreszenzmessungen zeigten, dass der Farbstoff, wenn er an geladene Membranen gebunden ist, eine erhöhte lokale Beweglichkeit gewinnt, obwohl sich der gesamte Komplex langsamer dreht. Kernspinresonanz- und FRET-Experimente deuteten weiter darauf hin, dass positive Bereiche auf der SUMO-Oberfläche als vorübergehende Anker für den negativ geladenen Farbstoff wirken können; die Bindung an eine geladene Membran und Mutationen in diesen Bereichen lockern dieses Ankerverhalten, sodass der Farbstoff freier wackeln kann und die Anisotropie sinkt.
Membranpräferenzen im Maßstab abbilden
Weil der Anisotropierückgang robust und reproduzierbar ist, kann er als praktischer Bindungsreporter genutzt werden, statt als störender Artefakt behandelt zu werden. Arrays von Vesikeln mit unterschiedlichen Lipidtypen und Krümmungen lassen sich schnell untersuchen, wodurch Forscher schnell bestimmen können, welche Kombinationen aus Lipiden und Formen eine bestimmte Helix am stärksten anziehen. Die Plattform funktioniert besonders gut für negativ geladene Membranen, die in Organellen vorkommen, die am Transport und der Energieerzeugung beteiligt sind. Durch das Engineering von ladungsveränderten Varianten des Trägerproteins erweitern die Autoren den nützlichen Bereich der Bedingungen hin zu physiologischeren Salzkonzentrationen und subtil geladenen Membranen und vergrößern damit die Anwendbarkeit der Methode.
Was das für das Verständnis zellulärer Zielsteuerung bedeutet
Alltagssprachlich bietet diese Arbeit einen neuen Hochdurchsatz-„Leser“ für die molekularen Postleitzahlen, die Proteine zur richtigen zellulären Adresse führen. Anstatt sich auf sperrige, langsame Experimente zu verlassen, können Wissenschaftler nun viele Helices und Membranrezepte parallel screenen und dabei eine einfache optische Signatur verwenden, die sich in eine unerwartete, aber gut verstandene Richtung umkehrt. Im Laufe der Zeit sollte dies ermöglichen, welche Aminosäuremuster welchen Lipidumgebungen entsprechen, zu entschlüsseln und so klarer zu machen, wie Zellen diese kleinen, flexiblen Helices nutzen, um Proteine zu sortieren, Membranen umzubauen und wichtige Signal- und Transportwege zu steuern.
Zitation: Margaritakis, A., Qian, M., Johnson, D.H. et al. Recombinant protein platform for high-throughput investigation of peptide-liposome interactions via fluorescence anisotropy depolarization. Commun Chem 9, 165 (2026). https://doi.org/10.1038/s42004-026-01994-9
Schlüsselwörter: membranbindende Peptide, Fluoreszenzanisotropie, amphipatische Helices, Lipidvesikel, Protein–Membran-Interaktionen