Clear Sky Science · nl
Recombinant-eiwitplatform voor grootschalig onderzoek van peptide-liposoominteracties via depolarisatie van fluorescentie-anisotropie
Hoe vormveranderende eiwitstukjes de juiste membranen vinden
In elke cel hangen talloze transporten, signalen en recyclingprocessen ervan af dat eiwitten op het juiste membraan op het juiste moment terechtkomen. Veel van deze eiwitten gebruiken korte, slappe reeksen die pas in nette helices vouwen wanneer ze een geschikt membraan aanraken. Dit artikel introduceert een nieuwe, snellere manier om te bestuderen hoe die vormveranderende stukjes specifieke membranen herkennen, waarbij een verrassend optisch signaal als ingebouwde reporter wordt gebruikt.
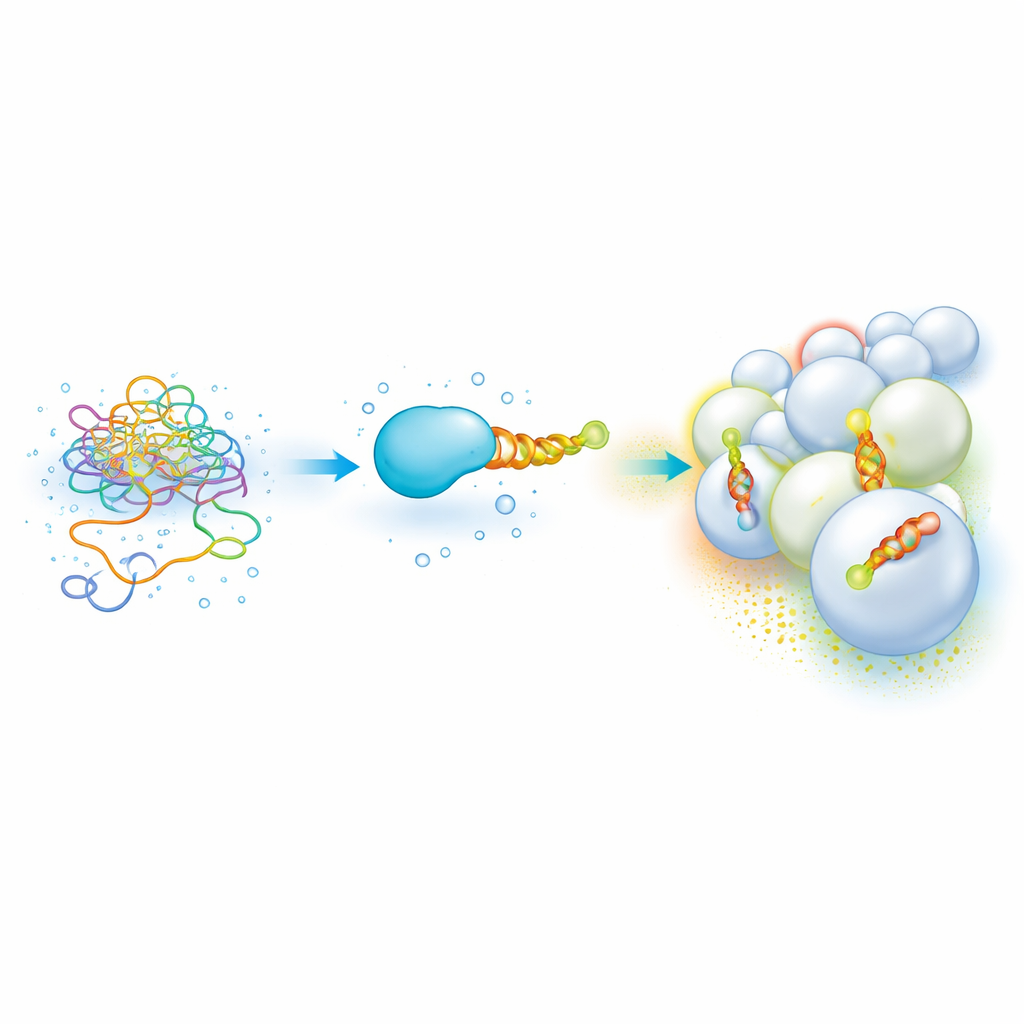
Flexibele eiwituiteinden die membrane "postcode" lezen
Veel belangrijke cellulaire eiwitten dragen een korte, ongestructureerde segment dat een amfifatische helix wordt — een spiraal met een vette kant en een waterige kant — zodra het aan een membraan dockt. Deze helices helpen eiwitten om het ene organel van het andere te onderscheiden door de lipide-samenstelling en kromming te voelen, waardoor ze terechtkomen op plaatsen zoals endosomen of mitochondriën. Maar losgemaakt zijn deze plakkerige, deels vette stukjes moeilijk hanteerbaar: ze klonteren, neerslaan en vereisen trage, monsteretende methoden om te meten hoe sterk ze aan verschillende membranen binden. Daardoor is het lastig geweest om een duidelijke “code” te bouwen die helicesekwestie koppelt aan membraangevoeligheid.
Een modulair eiwitplatform dat binden doet oplichten
De auteurs bouwden een recombinant platform dat deze ontembare helices temt en hun membraankeuzes gemakkelijk parallel meetbaar maakt. Elke testhelix is gefuseerd met een goed gedraagde drager‑eiwit genaamd SUMO, wat de oplosbaarheid en expressie verhoogt, en is aan het verre eind gemarkeerd met een fluorescent kleurstof. Wanneer het construct wordt gemengd met kunstmatige lipideblaasjes en uitgelezen in een gangbare microplatenlezer, volgen de onderzoekers fluorescentie-anisotropie — een maat voor hoezeer de emissie van de kleurstof haar polarisatie "onthoudt", wat afhangt van hoe vrij de kleurstof kan roteren. Door veel lipidemengsels en blaasjesgroottes in kleine volumes te titreren, bouwen ze snel bindingscurven voor verschillende helices over een breed landschap van membraansamenstellingen en krommingen.
Een tegenintuïtief signaal dat toch binding rapporteert
Intuïtief zou je verwachten dat wanneer een klein eiwit‑kleurstofconstruct aan een veel groter blaasje bindt, de rotatie vertraagt en de anisotropie stijgt. In plaats daarvan zien de auteurs het tegengestelde: anisotropie daalt naarmate binding toeneemt. Ze onderzochten of dit vreemde gedrag nog steeds echte membraanassociatie weergeeft door het te vergelijken met een klassieke methode op basis van tryptofaanfluorescentie, die rapporteert hoe diep een helix zich in de vette kern van het membraan begraaft. Voor meerdere biologisch relevante helices — afkomstig van eiwitten zoals Amphiphysin, CHMP4B, Endophilin-B1 en Huntingtin — geven het nieuwe platform en de traditionele uitlezing sterk overeenkomende bindingscurven en lipidevoorkeuren, en onthullen ze zelfs nieuwe trends zoals sterkere binding van de Amphiphysin-helix aan cholesterolrijke membranen.
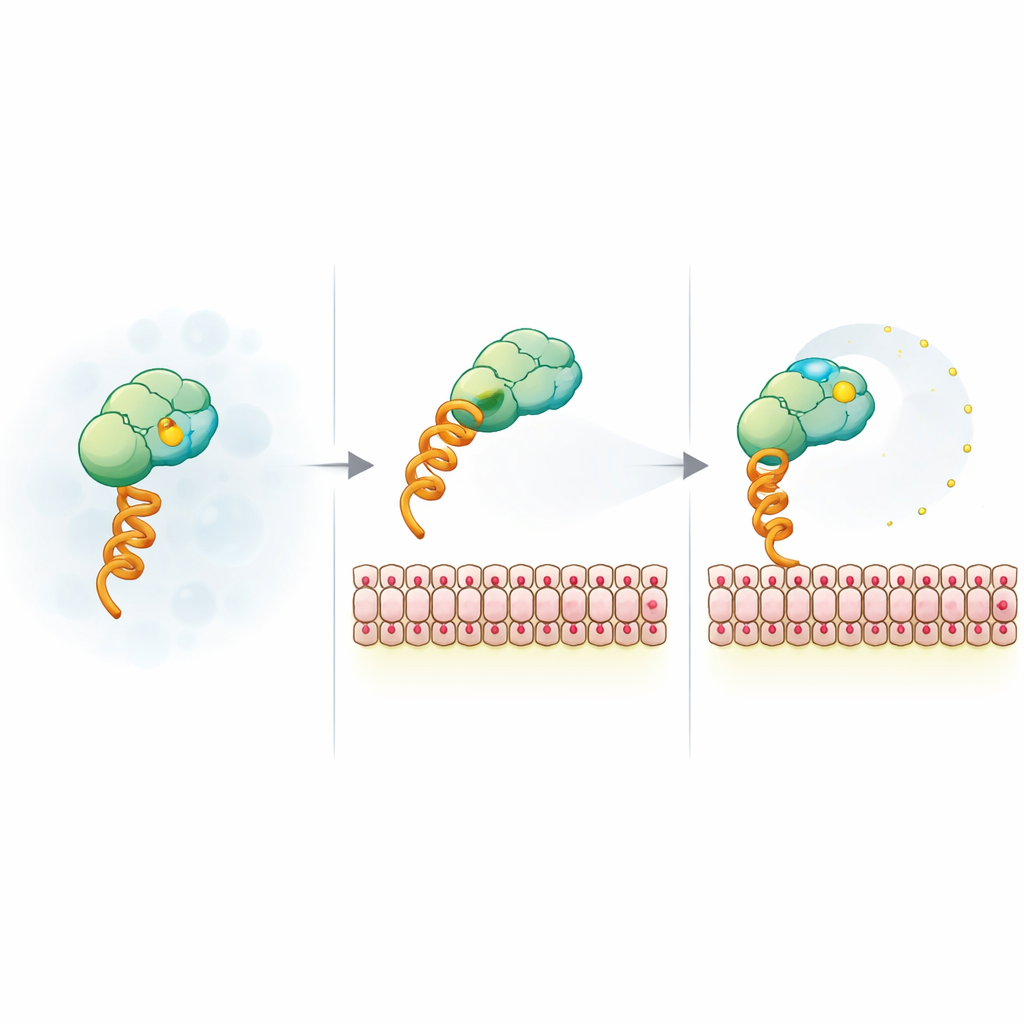
Hoe membraanspanning de fluorescente reporter vrijmaakt
Om het onverwachte signaal te verklaren, brachten het team het systeem terug tot een modelconstruct dat membranen bindt via een generieke histidine-tag en een nikkel-chelerende lipide. Ze varieerden vervolgens blaasjesgrootte, oppervlakte‑lading, zoutniveau en kleurstoftype. De daling in anisotropie bleek ongevoelig voor blaasjesgrootte en fluoroforenidentiteit, maar sterk gevoelig voor negatieve membraanlading en scherming door zout, wat wijst op een elektrostatische oorsprong. Tijdsgedragen fluorescentiemetingen toonden aan dat wanneer gebonden aan geladen membranen, de kleurstof meer lokale mobiliteit verkrijgt hoewel het gehele complex trager roteert. Nucleaire magnetische resonantie en FRET-experimenten suggereerden verder dat positieve patchen op het SUMO‑oppervlak als tijdelijke ankers voor de negatief geladen kleurstof kunnen fungeren; binden aan een geladen membraan en het muteren van deze patchen versoepelen beide dit anker, waardoor de kleurstof vrijer kan wiebelen en de anisotropie daalt.
Op grote schaal membraangevoorkeuren in kaart brengen
Aangezien de afname van anisotropie robuust en reproduceerbaar is, kan ze als handige reporter van binding worden gebruikt in plaats van als een problematisch artefact. Arrays van blaasjes die verschillen in lipide‑type en kromming kunnen snel worden onderzocht, waardoor onderzoekers kunnen bepalen welke combinaties van lipiden en vormen het beste een bepaalde helix aantrekken. Het platform werkt vooral goed voor negatief geladen membranen, die veel voorkomen in organellen die betrokken zijn bij transport en energieproductie. Door drager‑eiwitten met veranderde lading te ontwerpen, breiden de auteurs het nuttige bereik van condities uit naar meer fysiologische zoutniveaus en subtiel geladen membranen, waardoor de toepasbaarheid van de methode verder toeneemt.
Wat dit betekent voor het begrijpen van cellulaire targeting
In gewone bewoordingen biedt dit werk een nieuwe, grootschalige "lezer" voor de moleculaire postcodes die eiwitten naar het juiste cellulaire adres leiden. In plaats van te vertrouwen op omvangrijke, trage experimenten, kunnen wetenschappers nu veel helices en membraanrecepten parallel screenen met een eenvoudig optisch signaal dat onverwacht omklapt maar goed begrepen is. Naarmate dit zich ontwikkelt, zal het mogelijk worden te ontcijferen welke aminozuurpatronen corresponderen met welke lipideomgevingen, en zo verduidelijken hoe cellen deze kleine, flexibele helices gebruiken om eiwitten te sorteren, membranen te vervormen en vitale signaal‑ en transportroutes te reguleren.
Bronvermelding: Margaritakis, A., Qian, M., Johnson, D.H. et al. Recombinant protein platform for high-throughput investigation of peptide-liposome interactions via fluorescence anisotropy depolarization. Commun Chem 9, 165 (2026). https://doi.org/10.1038/s42004-026-01994-9
Trefwoorden: membraan-bindende peptiden, fluorescentie-anisotropie, amfifatische helices, lipideblaasjes, eiwit–membraaninteracties