Clear Sky Science · zh
果糖-2,6-二磷酸恢复由TDP-43病理驱动的运动神经疾病中基因组修复缺陷
为什么断裂的DNA对神经细胞很重要
肌萎缩侧索硬化(ALS)与额颞叶痴呆(FTD)是夺走人们运动、语言和记忆能力的毁灭性脑病。多年来,科学家们已知一种名为TDP-43的蛋白在这些疾病中会在神经细胞内错误聚集,但这种现象如何导致神经元死亡仍不清楚。这项研究揭示了能量代谢与细胞修复断裂DNA能力之间的一个意外联系,并显示一种小型糖类相关分子可以在疾病模型中部分逆转DNA损伤和运动功能障碍。
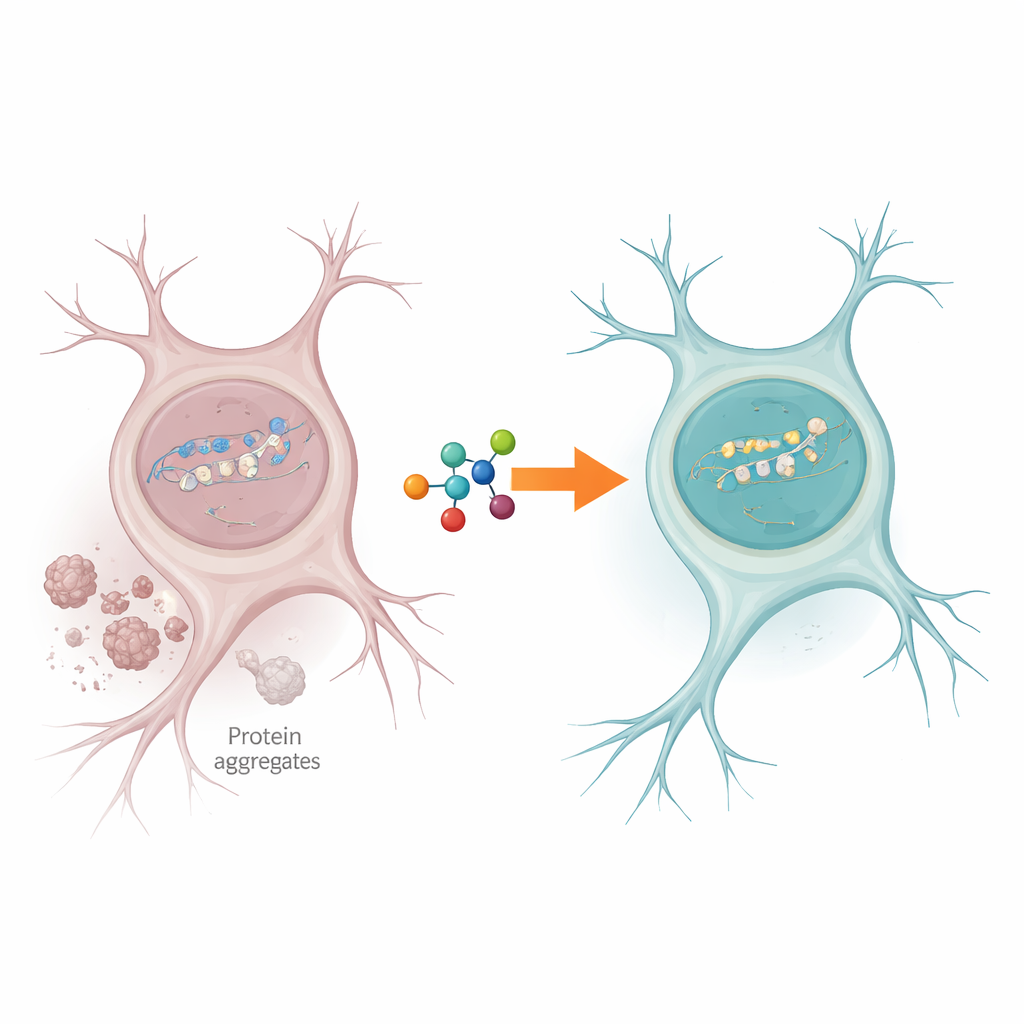
细胞“修复车间”中的交通堵塞
神经细胞不断遭受DNA断裂,尤其发生在那些被积极转录以维持细胞功能的基因中。通常,一种叫PNKP的酶能清理断裂DNA的游离末端,从而使修复得以完成。作者发现,在ALS和FTD患者的大脑组织中,PNKP的活性明显下降,尽管该酶本身仍存在。与此同时,在活跃基因中存在持续的DNA损伤迹象,表明修复机器正停滞在最需要维持神经元功能的位置。
一种错位的蛋白如何扰乱DNA修复
TDP-43通常位于储存DNA的细胞核内,帮助协调危险的双链断裂的修复。然而在ALS和FTD中,TDP-43泄漏到细胞外围并形成黏性的聚集体。通过在培养细胞中降低TDP-43水平,研究者们证明,仅仅失去核内TDP-43就足以削弱PNKP处理断裂DNA的能力,尽管PNKP的数量并未改变。他们还观察到,一个较大的修复复合体——其中通常包括TDP-43、PNKP及其它在活跃基因中封闭DNA断裂的因子——在TDP-43错位时解体。结果是在高使用率基因中特异性地积累DNA损伤,使本已脆弱的运动神经元更加易受损害。
糖代谢利用与基因组保护之间的缺失关联
研究进一步将这种修复失败追溯到代谢开关。PNKP依赖一种称为果糖-2,6-二磷酸(F2,6BP)的微小分子以高效工作,该分子由酶PFKFB3产生。在ALS和FTD的大脑样本中,PFKFB3蛋白和F2,6BP水平明显降低,而PFKFB3的基因指令基本完好。这指向PFKFB3蛋白被增强降解而非产生问题。在来自患者的神经前体细胞和多个模拟TDP-43病理的动物模型中,出现了相同模式:TDP-43错位、PFKFB3下降、PNKP活性减弱,以及活跃基因中更多的DNA损伤。
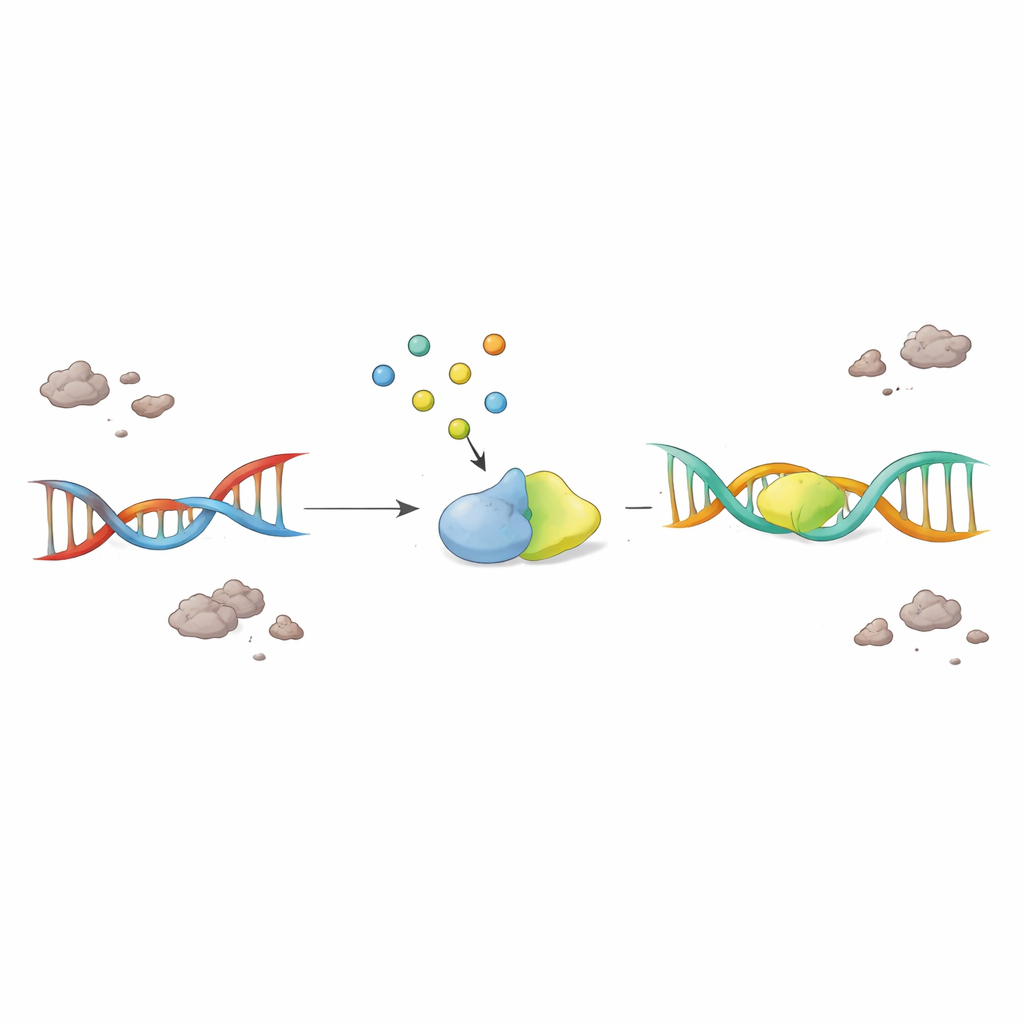
增强一种小分子以拯救病变神经元
关键是,科学家们测试了仅仅补充F2,6BP是否能重新激活停滞的修复系统。当向来自ALS和FTD大脑的核提取物中加入F2,6BP时,PNKP活性以剂量依赖性方式恢复,而与之相近的其他糖类分子则无效。在携带疾病相关TDP-43突变的患者来源细胞中,F2,6BP既恢复了PNKP活性,又减少了细胞质中异常聚集的TDP-43。在具有TDP-43病理的小鼠模型中,F2,6BP同样使PNKP功能复苏。最显著的是,在一种在人类突变TDP-43表达的水果蝇运动神经元模型中,经口给予F2,6BP改善了昆虫的爬行能力,并减少了在那些易断裂的大型高活性基因中的DNA损伤。
这对未来治疗可能意味着什么
总的来说,这些发现描绘了这样一条路径:TDP-43病理扰乱了将能量代谢与DNA修复连接起来的关键轴线——PFKFB3产生F2,6BP,F2,6BP支持PNKP,PNKP保护活跃基因免于积累断裂。当该轴线失效时,神经元逐步失去基因组稳定性和功能。通过补充F2,6BP,作者得以恢复PNKP活性、更高效地修复DNA,并在活体生物中缓解运动障碍。尽管要将此转化为人类疗法并精细调控代谢影响仍需大量工作,但该研究表明,精确针对这一代谢—修复通路可能为治疗ALS、FTD以及其他由TDP-43蛋白堆积标志的疾病开辟一种基于机制的新途径。
引用: Chakraborty, A., Mitra, J., Malojirao, V.H. et al. Fructose-2,6-bisphosphate restores TDP-43 pathology-driven genome repair deficiency in motor neuron diseases. Commun Biol 9, 563 (2026). https://doi.org/10.1038/s42003-026-09787-5
关键词: ALS, TDP-43, DNA修复, 神经退行性疾病, 细胞代谢