Clear Sky Science · pt
Frutose-2,6-bisfosfato restaura a deficiência de reparo genômico causada pela patologia de TDP-43 em doenças do neurônio motor
Por que o DNA Quebrado Importa nas Células Nervosas
A esclerose lateral amiotrófica (ELA) e a demência frontotemporal (DFT) são doenças cerebrais devastadoras que roubam das pessoas a capacidade de se mover, falar e lembrar. Há anos os cientistas sabem que uma proteína chamada TDP-43 se agrega no local errado dentro das células nervosas nessas condições, mas como isso leva à morte neuronal permaneceu obscuro. Este estudo revela uma ligação surpreendente entre o metabolismo energético e a habilidade da célula de reparar DNA quebrado, e mostra que uma pequena molécula relacionada a açúcares pode reverter parcialmente tanto o dano ao DNA quanto os problemas de movimento em modelos da doença.
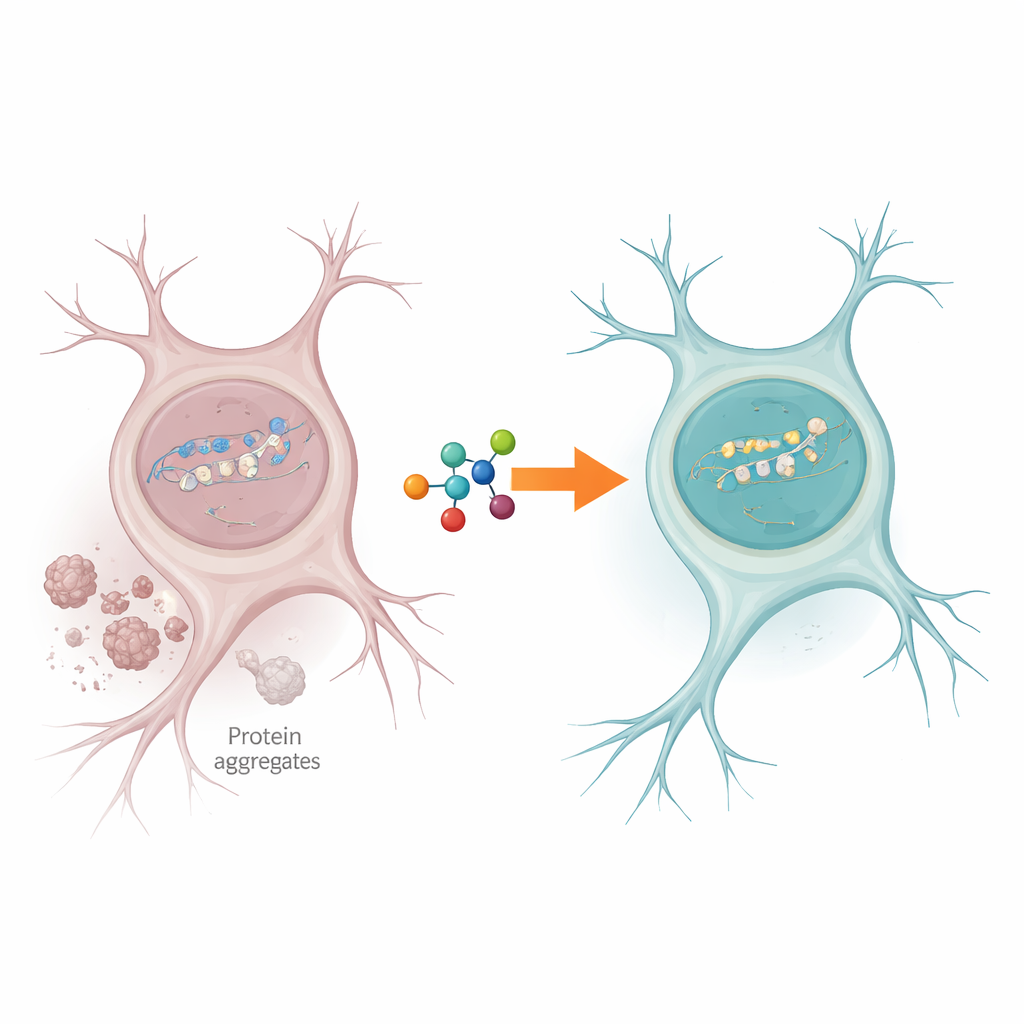
Um Engarrafamento na Oficina de Reparo da Célula
As células nervosas experimentam constantemente quebras de DNA, especialmente em genes que são ativamente lidos para manter a célula funcionando. Normalmente, uma enzima chamada PNKP ajuda a aparar as extremidades soltas do DNA quebrado para que o reparo possa ser completado. Os autores descobriram que, em tecido cerebral de pessoas com ELA e DFT, a atividade da PNKP estava fortemente reduzida, embora a própria enzima ainda estivesse presente. Ao mesmo tempo, havia evidências claras de dano persistente ao DNA em genes ativos, sugerindo que a maquinaria de reparo estava travada justamente onde é mais necessário para preservar a função neuronal.
Como uma Proteína Fora do Lugar Desregula o Reparo do DNA
Normalmente TDP-43 reside no núcleo, onde o DNA é armazenado, e ajuda a coordenar o reparo de quebras de dupla fita perigosas. Na ELA e na DFT, no entanto, TDP-43 vaza para a região externa da célula e forma agregados pegajosos. Ao reduzir os níveis de TDP-43 em células cultivadas, os pesquisadores demonstraram que essa perda de TDP-43 nuclear é suficiente para prejudicar a capacidade da PNKP de processar DNA quebrado, mesmo que a quantidade de PNKP não mude. Eles também observaram que uma equipe maior de reparo, que normalmente inclui TDP-43, PNKP e outros fatores que selam quebras em genes ativos, se desfaz quando TDP-43 está mal localizado. O resultado é um acúmulo de dano ao DNA especificamente em genes muito usados, tornando os neurônios motores já vulneráveis ainda mais frágeis.
Um Elo Ausente Entre o Uso de Açúcar e a Proteção do Genoma
O estudo então rastreia essa falha de reparo até uma mudança metabólica. A PNKP depende de uma pequena molécula chamada frutose-2,6-bisfosfato (F2,6BP), produzida pela enzima PFKFB3, para funcionar eficientemente. Em amostras cerebrais de ELA e DFT, as proteínas PFKFB3 e os níveis de F2,6BP estavam marcadamente reduzidos, enquanto as instruções genéticas para PFKFB3 estavam em grande parte intactas. Isso aponta para um aumento na degradação da proteína PFKFB3 em vez de um problema em sua produção. Em células precursoras nervosas derivadas de pacientes e em vários modelos animais diferentes que imitam a patologia de TDP-43, emergiu o mesmo padrão: TDP-43 mal localizado, PFKFB3 reduzido, atividade da PNKP enfraquecida e mais dano ao DNA em genes ativos.
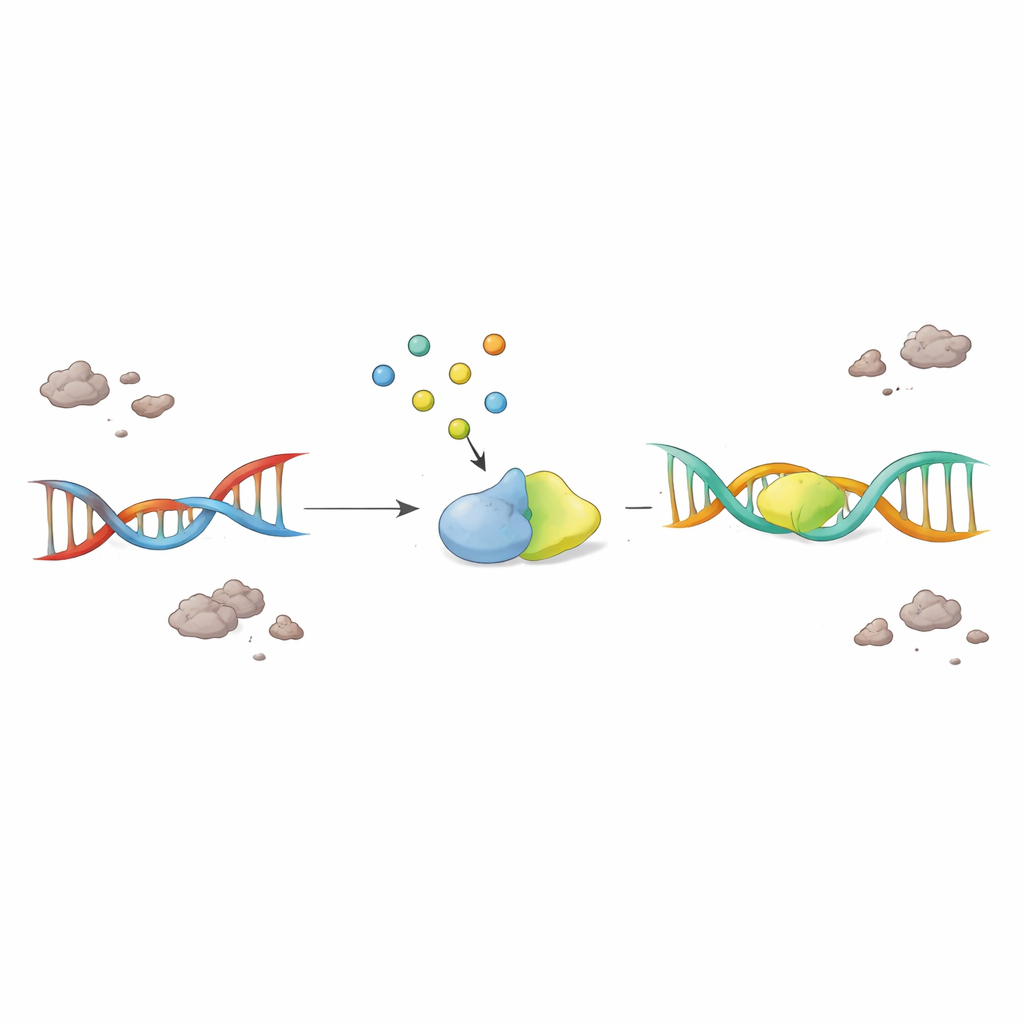
Potencializando uma Pequena Molécula para Resgatar Neurônios Doentes
De modo crucial, os cientistas testaram se simplesmente repor F2,6BP poderia reativar o sistema de reparo travado. Quando F2,6BP foi fornecido a extratos nucleares de cérebros com ELA e DFT, a atividade da PNKP se recuperou de forma dependente da dose, enquanto moléculas de açúcar estreitamente relacionadas não tiveram efeito. Em células de pacientes portadoras de mutações de TDP-43 associadas à doença, F2,6BP tanto restaurou a atividade da PNKP quanto reduziu a quantidade de TDP-43 anormal e agregada no citosol. Em um modelo de camundongo com patologia de TDP-43, F2,6BP novamente reativou a função da PNKP. Mais notavelmente, em um modelo de mosca-da-fruta expressando TDP-43 humano mutante em neurônios motores, o tratamento oral com F2,6BP melhorou a capacidade de escalada das moscas e reduziu o dano ao DNA em genes grandes e de alta atividade que são sensíveis à quebra.
O Que Isso Pode Significar para Tratamentos Futuros
Em conjunto, essas descobertas retratam um quadro no qual a patologia de TDP-43 descarrila um eixo crítico que liga metabolismo energético ao reparo do DNA: PFKFB3 produz F2,6BP, F2,6BP alimenta a PNKP, e PNKP protege genes ativos de acumular quebras. Quando esse eixo falha, os neurônios gradualmente perdem estabilidade genômica e função. Ao reabastecer F2,6BP, os autores foram capazes de reviver a atividade da PNKP, reparar o DNA de forma mais eficiente e aliviar problemas de movimento em um organismo vivo. Embora ainda haja muito trabalho para traduzir isso em terapias humanas e ajustar os efeitos metabólicos, o estudo sugere que direcionar cuidadosamente essa via metabólica–reparo pode abrir uma nova rota baseada em mecanismos para tratar ELA, DFT e possivelmente outros distúrbios marcados pelo acúmulo da proteína TDP-43.
Citação: Chakraborty, A., Mitra, J., Malojirao, V.H. et al. Fructose-2,6-bisphosphate restores TDP-43 pathology-driven genome repair deficiency in motor neuron diseases. Commun Biol 9, 563 (2026). https://doi.org/10.1038/s42003-026-09787-5
Palavras-chave: ALS, TDP-43, Reparo de DNA, Neurodegeneração, Metabolismo celular