Clear Sky Science · ar
الفركتوز-2,6-بيسفوسفات يستعيد عجز إصلاح الجينوم الناجم عن باثولوجيا TDP-43 في أمراض الخلايا العصبية الحركية
لماذا تهم الكسور في الحمض النووي خلايا الأعصاب
التصلب الجانبي الضموري (ALS) وخرف الفص الجبهي الصدغي (FTD) هما مرضان دمّرا قدرة الأشخاص على الحركة والكلام والذاكرة. لسنوات، عرف العلماء أن بروتينًا يسمى TDP-43 يتجمع في مكان خاطئ داخل خلايا الأعصاب في هذه الحالات، لكن كيف يؤدي ذلك إلى موت الخلايا العصبية ظل غامضًا. تكشف هذه الدراسة عن صلة مفاجئة بين استقلاب الطاقة وقدرة الخلية على إصلاح الحمض النووي المكسور، وتُظهر أن جزيئًا سكريًا صغيرًا يمكنه أن يعكس جزئيًا كلًّا من تلف الحمض النووي ومشكلات الحركة في نماذج المرض.
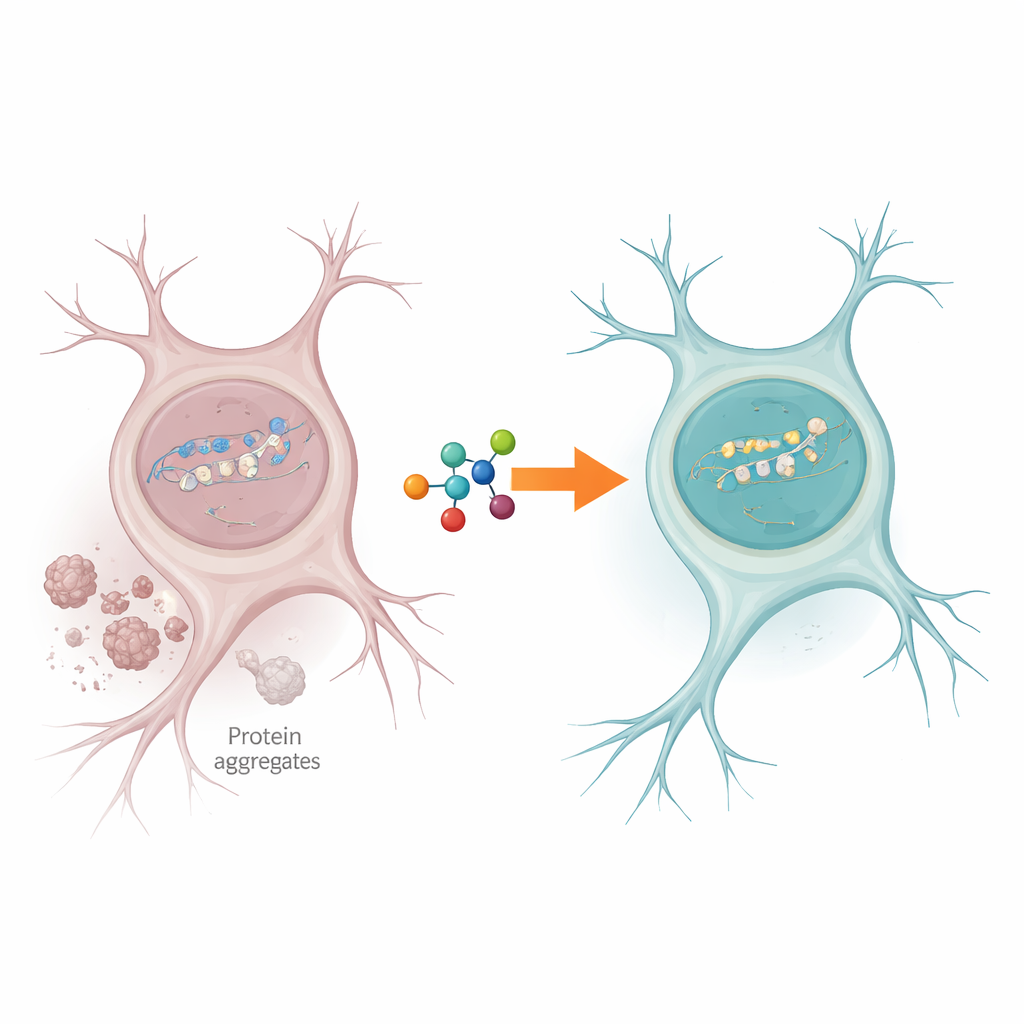
ازدحام مروري في ورشة إصلاح الخلية
تعاني خلايا الأعصاب باستمرار كسورًا في الحمض النووي، لا سيما في الجينات التي تُقرأ بنشاط للحفاظ على عمل الخلية. عادةً ما يساعد إنزيم يسمى PNKP في ترتيب النهايات الحرة للحمض النووي المكسور بحيث يمكن إتمام الإصلاح. وجد المؤلفون أنه في أنسجة المخ لأشخاص مصابين بـ ALS وFTD، انخفض نشاط PNKP بشكل حاد، رغم أن الإنزيم نفسه لا يزال موجودًا. وفي الوقت نفسه، وُجدت أدلة واضحة على بقاء تلف الحمض النووي في الجينات النشيطة، ما يشير إلى أن آلية الإصلاح توقفت تمامًا حيث تُعدّ الأكثر حاجة للحفاظ على وظيفة العصبون.
كيف يعطل بروتين في المكان الخطأ إصلاح الحمض النووي
عادةً ما يقيم TDP-43 في النواة حيث يُخزن الحمض النووي، ويساهم في تنسيق إصلاح الكسور ذات الشريحتين الخطير. في حالات ALS وFTD، يتسرّب TDP-43 إلى المنطقة الخارجية للخلية ويتجمع فيها بشكل لزج. بخفض مستويات TDP-43 في خلايا مزروعة، أظهر الباحثون أن هذا الفقدان لـ TDP-43 النووي يكفي لتعطيل قدرة PNKP على معالجة الحمض النووي المكسور، رغم عدم تغيّر كمية PNKP. كما لاحظوا أن فريق إصلاح أوسع، والذي يشمل عادةً TDP-43 وPNKP وعوامل أخرى تغلق كسور الحمض النووي في الجينات النشيطة، يتفكك عندما يُزال TDP-43 عن موضعه. النتيجة هي تراكم تلف الحمض النووي تحديدًا في الجينات ذات الاستخدام الكثيف، مما يجعل الخلايا العصبية الحركية المعرضة للخطر أكثر هشاشة.
حلقة مفقودة بين استخدام السكر وحماية الجينوم
تتبع البحث هذا الفشل في الإصلاح إلى مفتاح أيضي. يعتمد PNKP على جزيء صغير يُدعى فركتوز-2،6-بيسفوسفات (F2,6BP)، والذي تنتجه الإنزيم PFKFB3، ليعمل بكفاءة. في عينات أدمغة مرضى ALS وFTD، لوحظ انخفاض واضح في بروتين PFKFB3 ومستويات F2,6BP، بينما كانت التعليمات الجينية الخاصة بـ PFKFB3 سليمة إلى حد كبير. يشير ذلك إلى زيادة تحطيم بروتين PFKFB3 بدلًا من مشكلة في تصنيعه. في خلايا مُنفَدة من مرضى ومختلف نماذج حيوانية تُحاكي باثولوجيا TDP-43، ظهر نفس النمط: وجود TDP-43 في المكان الخاطئ، انخفاض PFKFB3، ضعف نشاط PNKP، ومزيد من تلف الحمض النووي في الجينات النشيطة.
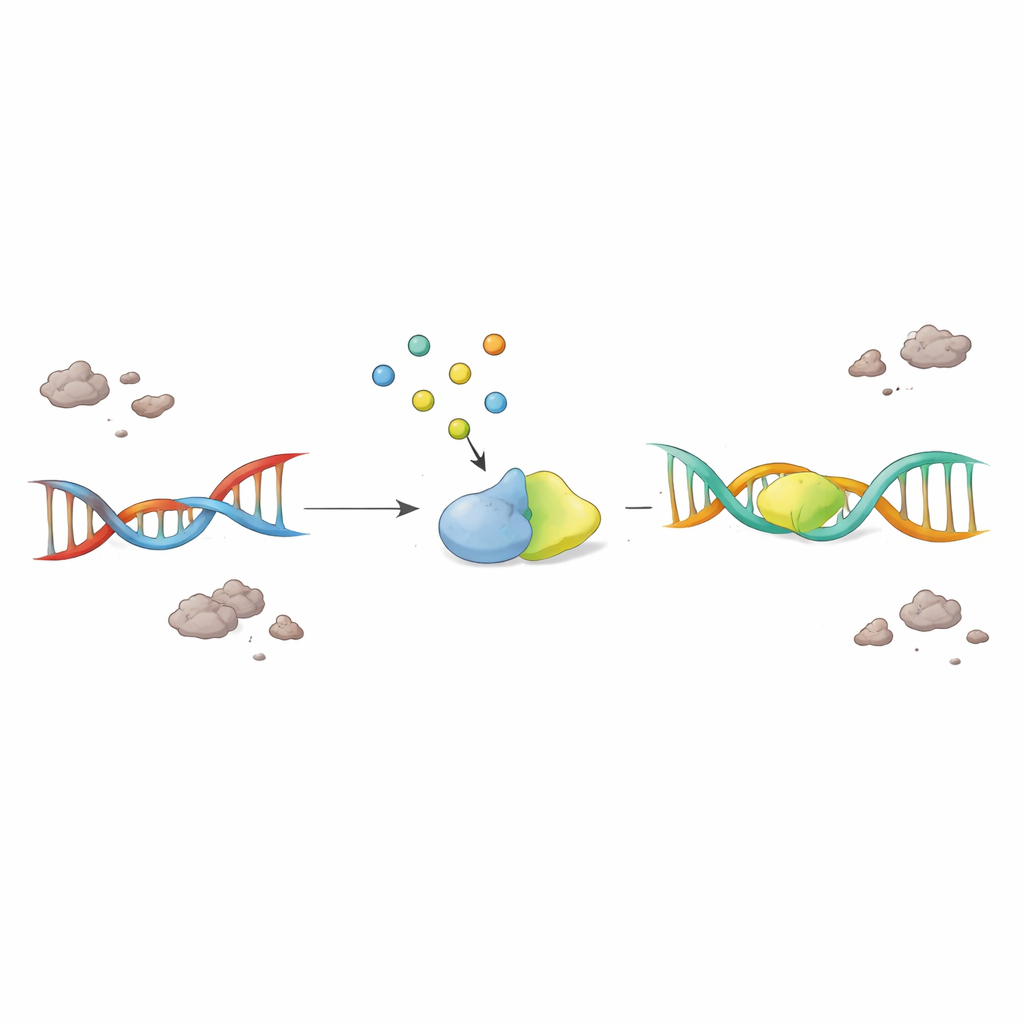
تعزيز جزيء صغير لإنقاذ الخلايا العصبية المريضة
الأهم أن العلماء اختبروا ما إذا كان ببساطة إعادة F2,6BP كافٍ لإيقاظ نظام الإصلاح المتعطّل. عندما مُنح F2,6BP إلى مستخلصات نوية من أدمغة ALS وFTD، عاد نشاط PNKP تدريجيًا وباعتماد الجرعة، بينما لم تُظهر جزيئات سكرية قريبة أي تأثير. في خلايا من المرضى تحمل طفرات مرتبطة بالمرض في TDP-43، أعاد F2,6BP نشاط PNKP وخفض أيضاً كمية TDP-43 الشاذ والمتجمع في السيتوبلازم. في نموذج فأري ذو باثولوجيا TDP-43، أعاد F2,6BP مرة أخرى وظيفة PNKP. والأكثر لفتًا للانتباه، في نموذج ذبابة الفاكهة المعبر عن TDP-43 البشري الطافر في الخلايا العصبية الحركية، حسَّنت المعالجة الفموية بـ F2,6BP قدرة الذباب على التسلق وقلَّلت تلف الحمض النووي في الجينات الكبيرة والنشيطة المعرضة للكسر.
ماذا قد يعني هذا للعلاجات المستقبلية
معًا ترسم هذه النتائج صورة تفيد بأن باثولوجيا TDP-43 تعطل محورًا حاسمًا يربط استقلاب الطاقة بإصلاح الحمض النووي: ينتج PFKFB3 الفركتوز-2،6-بيسفوسفات، يغذي F2,6BP نشاط PNKP، ويحمي PNKP الجينات النشيطة من تراكم الكسور. عندما يفشل هذا المحور، تفقد الخلايا العصبية استقرارها الجينومي ووظيفتها تدريجيًا. من خلال تجديد F2,6BP، استطاع المؤلفون إحياء نشاط PNKP، وإصلاح الحمض النووي بكفاءة أكبر، وتخفيف مشكلات الحركة في كائن حي. بينما يبقى الكثير من العمل لنقل هذا إلى علاجات بشرية ولضبط التأثيرات الأيضية بعناية، تقترح الدراسة أن استهداف هذا المسار الأيضي—الإصلاح بشكل دقيق قد يفتح مسارًا علاجيًا جديدًا يقوم على الآلية لعلاج ALS وFTD وربما اضطرابات أخرى تتميز بتراكم بروتين TDP-43.
الاستشهاد: Chakraborty, A., Mitra, J., Malojirao, V.H. et al. Fructose-2,6-bisphosphate restores TDP-43 pathology-driven genome repair deficiency in motor neuron diseases. Commun Biol 9, 563 (2026). https://doi.org/10.1038/s42003-026-09787-5
الكلمات المفتاحية: التصلب الجانبي الضموري, TDP-43, إصلاح الحمض النووي, الضمور العصبي, استقلاب الخلايا