Clear Sky Science · pl
Fruktozo-2,6-bisfosforan przywraca deficyt naprawy genomu wywołany patologią TDP-43 w chorobach neuronu ruchowego
Dlaczego uszkodzone DNA ma znaczenie w komórkach nerwowych
Stwardnienie zanikowe boczne (ALS) i otępienie czołowo-skroniowe (FTD) to niszczycielskie choroby mózgu, które pozbawiają ludzi ruchu, mowy i pamięci. Od lat wiadomo, że białko zwane TDP-43 zbija się w nieodpowiednim miejscu w komórkach nerwowych w tych schorzeniach, jednak mechanizm prowadzący do śmierci neuronów pozostawał niejasny. Badanie to ujawnia zaskakujące powiązanie między metabolizmem energetycznym a zdolnością komórki do naprawy złamanego DNA i pokazuje, że mała cząsteczka związana z cukrem może częściowo odwrócić zarówno uszkodzenia DNA, jak i problemy z ruchem w modelach choroby.
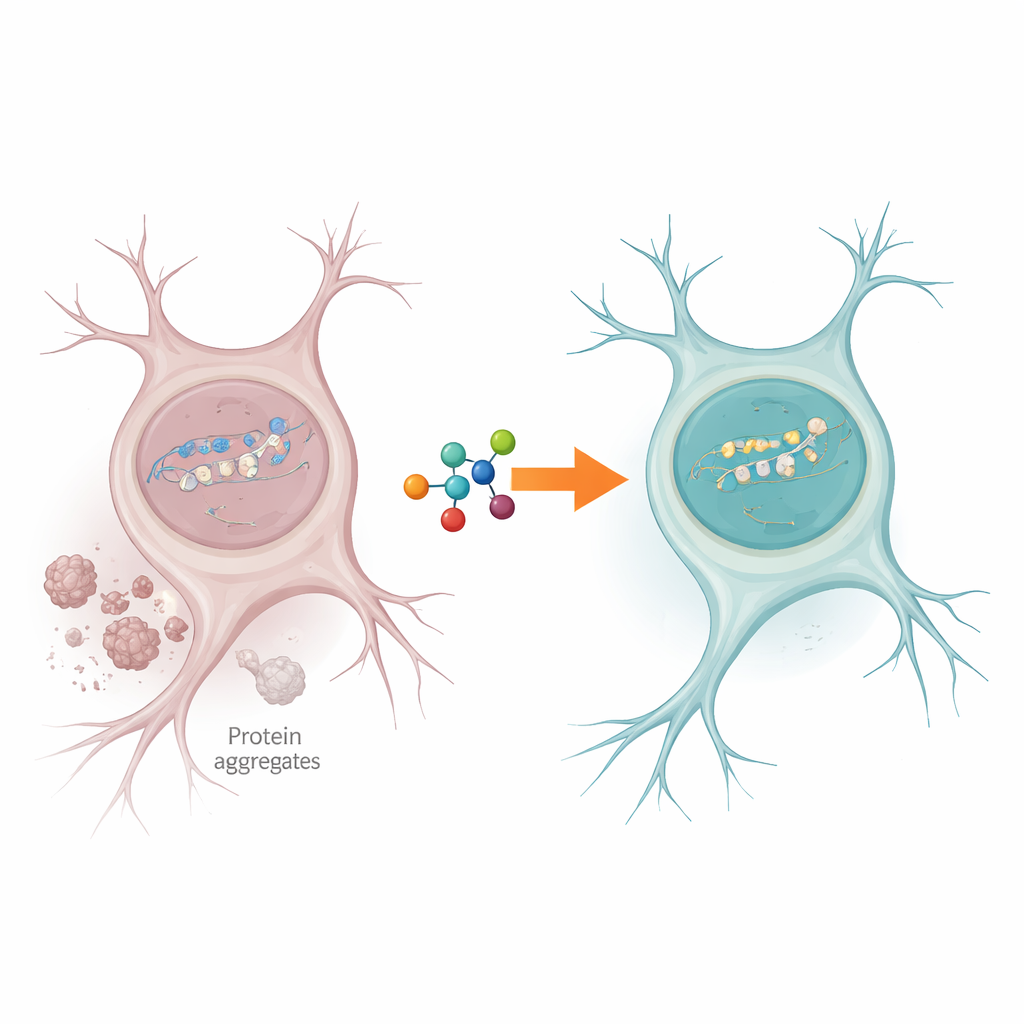
Korek w „warsztacie” naprawczym komórki
Komórki nerwowe stale doznają pęknięć DNA, zwłaszcza w genach, które są aktywnie odczytywane, by utrzymać funkcje komórki. Zwykle enzym zwany PNKP porządkuje wolne końce złamanego DNA, aby naprawa mogła zostać dokończona. Autorzy wykazali, że w tkankach mózgowych osób z ALS i FTD aktywność PNKP była wyraźnie osłabiona, choć sam enzym nadal był obecny. Równocześnie zaobserwowano trwałe ślady uszkodzeń DNA w aktywnych genach, co sugeruje, że aparat naprawczy zablokował się dokładnie tam, gdzie jest najbardziej potrzebny do zachowania funkcji neuronów.
Jak przesunięte białko zaburza naprawę DNA
TDP-43 zwykle znajduje się w jądrze komórkowym, gdzie przechowywane jest DNA, i pomaga koordynować naprawę groźnych pęknięć dwuniciowych. W ALS i FTD jednak TDP-43 przemieszcza się do obszaru zewnętrznego komórki i tworzy lepkie agregaty. Obniżając poziom TDP-43 w hodowlach komórkowych, badacze pokazali, że utrata jądrowego TDP-43 wystarcza, aby sparaliżować zdolność PNKP do przetwarzania złamanego DNA, mimo że ilość PNKP nie ulega zmianie. Zaobserwowali też, że większy zespół naprawczy, który normalnie obejmuje TDP-43, PNKP i inne czynniki uszczelniające przerwy w aktywnych genach, rozpada się, gdy TDP-43 jest błędnie zlokalizowane. W rezultacie w aktywnie używanych genach gromadzi się uszkodzenie DNA, przez co już i tak wrażliwe neurony ruchowe stają się jeszcze bardziej podatne na utratę funkcji.
Brakujące ogniwo między wykorzystaniem cukrów a ochroną genomu
Badanie śledzi tę awarię naprawczą aż do przełączenia metabolicznego. PNKP zależy od małej cząsteczki zwanej fruktozo-2,6-bisfosforanem (F2,6BP), produkowanej przez enzym PFKFB3, aby działać wydajnie. W próbkach mózgowych od osób z ALS i FTD poziomy białka PFKFB3 i F2,6BP były wyraźnie zredukowane, podczas gdy instrukcje genetyczne dla PFKFB3 były w dużej mierze nienaruszone. Wskazuje to na zwiększony rozkład białka PFKFB3, a nie na problem z jego syntezą. W komórkach prekursorowych pochodzących od pacjentów oraz w kilku różnych modelach zwierzęcych odzwierciedlających patologię TDP-43 pojawiał się ten sam wzorzec: przesunięte TDP-43, obniżone PFKFB3, słabsza aktywność PNKP i więcej uszkodzeń DNA w aktywnych genach.
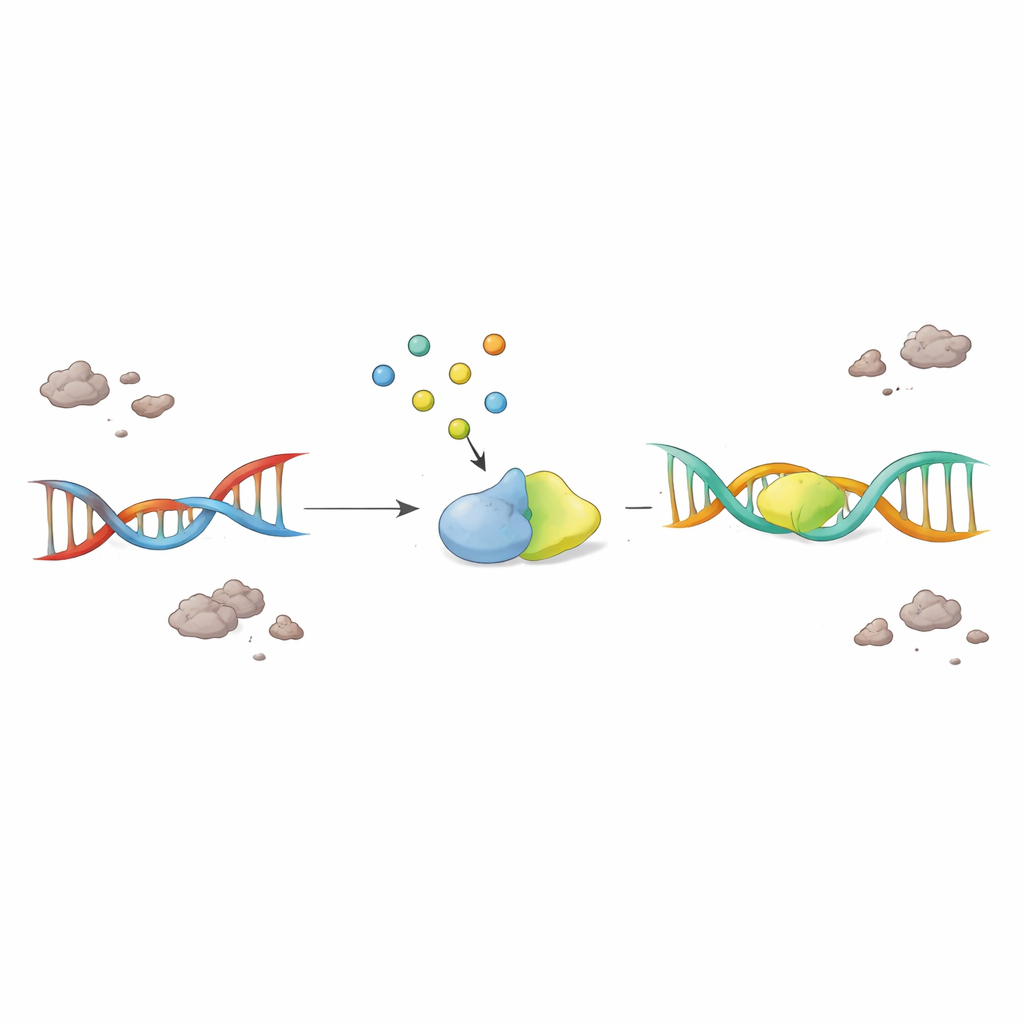
Zwiększenie poziomu małej cząsteczki ratuje chore neurony
Co istotne, naukowcy sprawdzili, czy samo uzupełnienie F2,6BP może wznowić zatrzymany system naprawy. Gdy F2,6BP dodano do ekstraktów jądrowych z mózgów chorych na ALS i FTD, aktywność PNKP odżywała w sposób zależny od dawki, podczas gdy blisko spokrewnione cząsteczki cukrowe nie wywołały takiego efektu. W komórkach pacjentów z mutacjami TDP-43 związanymi z chorobą, F2,6BP zarówno przywracało aktywność PNKP, jak i zmniejszało ilość nieprawidłowego, zdegenerowanego TDP-43 w cytosolu. W modelu myszy z patologią TDP-43 F2,6BP ponownie ożywiło funkcję PNKP. Co najbardziej uderzające, w modelu muszki owocowej wyrażającej zmutowane ludzkie TDP-43 w neuronach ruchowych doustne podanie F2,6BP poprawiło zdolność wspinaczkową muszek i zmniejszyło uszkodzenia DNA w dużych, intensywnie używanych genach podatnych na pęknięcia.
Co to może znaczyć dla przyszłych terapii
W sumie wyniki tworzą obraz, w którym patologia TDP-43 wytrąca z równowagi kluczową oś łączącą metabolizm energetyczny z naprawą DNA: PFKFB3 produkuje F2,6BP, F2,6BP zasila PNKP, a PNKP chroni aktywne geny przed gromadzeniem się pęknięć. Gdy ta oś zawodzi, neurony stopniowo tracą stabilność genomu i funkcję. Poprzez uzupełnienie F2,6BP autorzy byli w stanie przywrócić aktywność PNKP, skuteczniej naprawiać DNA i złagodzić problemy z ruchem u żywego organizmu. Choć wciąż potrzebne są liczne prace, by przekształcić to w terapie dla ludzi i dopracować efekty metaboliczne, badanie sugeruje, że celowanie w tę ścieżkę metabolizm–naprawa może otworzyć nową, opartą na mechanizmach drogę leczenia ALS, FTD i prawdopodobnie innych zaburzeń związanych z nagromadzeniem białka TDP-43.
Cytowanie: Chakraborty, A., Mitra, J., Malojirao, V.H. et al. Fructose-2,6-bisphosphate restores TDP-43 pathology-driven genome repair deficiency in motor neuron diseases. Commun Biol 9, 563 (2026). https://doi.org/10.1038/s42003-026-09787-5
Słowa kluczowe: ALS, TDP-43, naprawa DNA, neurodegeneracja, metabolizm komórkowy