Clear Sky Science · zh
冷冻电镜解析的联苯唑类杀菌剂(bixafen)结合的酿酒酵母复合体 II 结构揭示了 SDHI 对病原真菌的特异性
为何阻断真菌“发电厂”至关重要
真菌性疾病威胁农作物、森林乃至人体健康,许多现代杀菌剂通过切断病原体的能量供应来发挥作用。然而,直到现在,还没有人以原子级细节看清这些化学物质如何附着在真菌的靶点上。本文揭示了来自面包酵母的一个关键产能酶的三维结构,并准确展示了广泛使用的杀菌剂 bixafen 如何使这台分子机器失灵。由于该酶在许多致病真菌中高度相似,这项工作为设计更聪明的杀菌剂打开了大门——这些新型药物既能有效应对农作物和医学威胁,又对人类和环境更为安全。
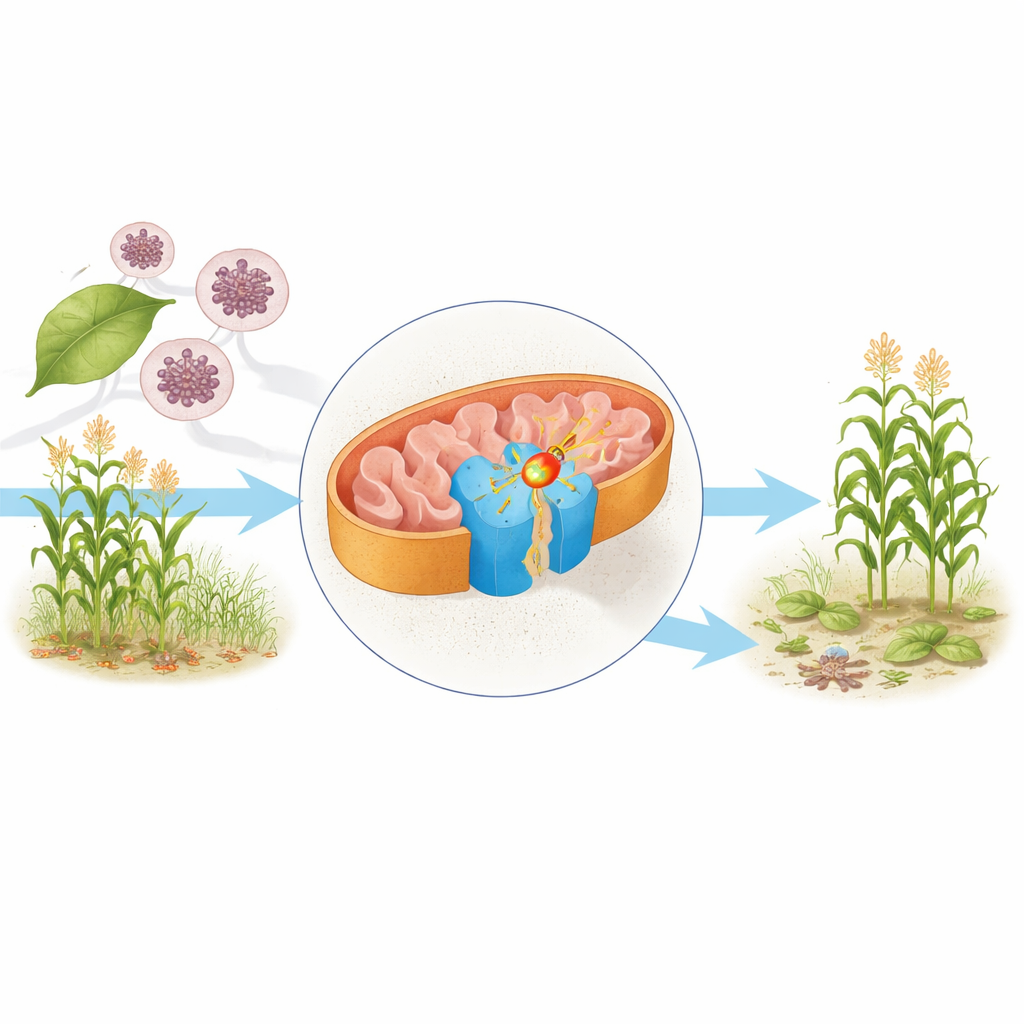
显微镜下的细胞引擎
在线粒体中——常被称为细胞的发电厂——食物分子被剥夺电子,最终用于合成 ATP,这是细胞的主要“燃料”。这一机制的一个核心组成部分是复合体 II,也称为琥珀酸脱氢酶。它将分解营养物质的 Krebs 循环与将化学能转化为可用能量的呼吸链连接起来。作者从生物学中常用的工蜂级模式生物酿酒酵母(Saccharomyces cerevisiae)中纯化了复合体 II,并用冷冻电子显微镜确定了其近原子分辨率的结构,有两种构象:一种带有其天然的电子穿梭分子泛醌(ubiquinone),另一种与杀菌剂 bixafen 结合。
熟悉的引擎却缺失了意想不到的部件
酵母的该酶与哺乳动物及其它生物的复合体 II 非常相似:两个疏水亲水的较大亚基负责化学反应,两个较小的膜嵌入亚基将复合体锚定在线粒体膜中。电子从黄素辅基通过一串铁-硫簇传递到膜区,泛醌通常在那里接受电子。然而,结构揭示了一个重大惊喜:与典型的“C 型”复合体 II 酶不同,酵母版本完全缺失血红素(heme)——这一含铁辅因子此前被认为是该家族通用的稳定化特征。相反,酵母复合体 II 借助额外的氢键、更多的疏水残基以及深埋的磷脂来粘合膜亚基,从而在没有血红素的情况下保持复合体完整。
杀菌剂在对接位点落位
研究的核心是所谓的 Q 位点,即泛醌正常结合以接收电子的口袋。在与 bixafen 结合的结构中,该口袋被杀菌剂占据,bixafen 模拟了泛醌的许多相互作用,同时还形成了额外的紧密接触。来自三个亚基的关键氨基酸通过极性与疏水相互作用共同托住抑制剂,而一个膜亚基(Sdh4)伸出的柔性延伸段折叠进入该位点并包裹住 bixafen 的疏水尾部。当天然底物存在时,Sdh4 延伸段的最尖端变得无序,为泛醌较长的侧链腾出空间,显示该口袋能根据底物或抑制剂的不同进行适应性调整。
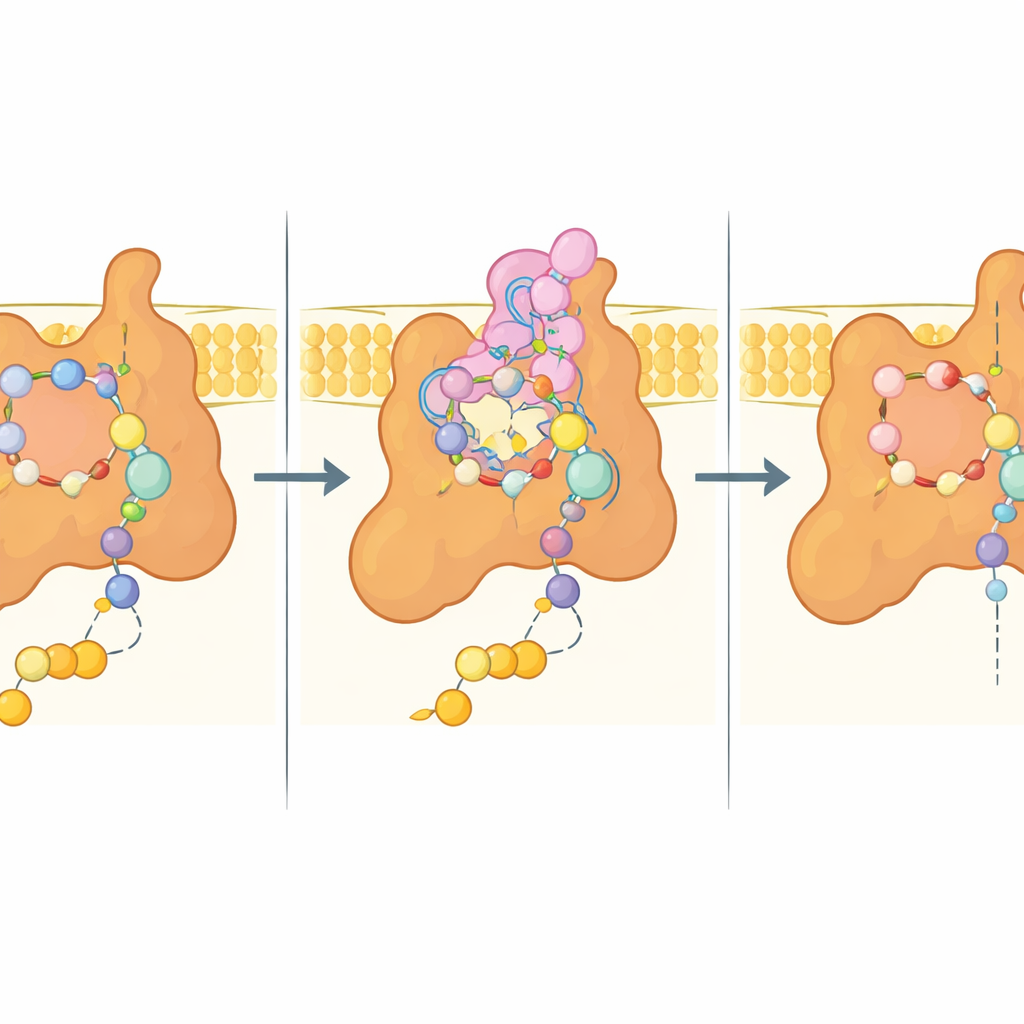
下一代杀菌剂的线索
由于许多具有农业重要性和对人类致病性的真菌在 Sdh4 序列上高度相似,尤其是在该 N 端延伸区,酵母结构很可能反映了它们的复合体 II 架构。作者利用其实验模型对数种商业化的琥珀酸脱氢酶抑制剂(SDHI)进行计算对接,揭示出一种共同的结合逻辑:一个与保守氨基酸相互作用的羧酰胺“核心”,以及可变的疏水性修饰装饰物可嵌入邻近口袋以调节结合强度和特异性。重要的是,与 bixafen 接触的几乎所有残基在多种作物病原体中均被保守,这表明微妙的序列差异可能解释为何某些物种更敏感或更不敏感——以及为什么某些突变会在田间带来抗性。
从结构图谱到实际影响
简而言之,该研究提供了关于一大类杀菌剂如何楔入并关闭真菌能量酶的详细蓝图。它还推翻了关于所谓普遍存在的血红素组分的假设,展示了酵母如何演化出替代的稳定化特征。借助这一结构图谱,研究人员现在可以有目的地修改现有杀菌剂或发明新药,以更好地利用真菌特异性特征、降低抗性发生的可能性,并将对农作物、野生动植物和人群的非靶向损害降到最低。面包酵母——长期为面包与啤酒所喜爱——因此成为构建下一代靶向抗真菌武器的强大模型。
引用: Pinotsis, N., Burn-Leefe, C., Jones, S. et al. Cryo-EM structure of bixafen-bound S. cerevisiae complex II unravels SDHI specificity against pathogenic fungi. Commun Biol 9, 517 (2026). https://doi.org/10.1038/s42003-026-09617-8
关键词: 琥珀酸脱氢酶, 杀菌剂抗性, 冷冻电子显微镜, 线粒体呼吸, SDHI 杀菌剂