Clear Sky Science · fr
Structure Cryo-EM du complexe II de S. cerevisiae lié au bixafène dévoile la spécificité des SDHI contre les champignons pathogènes
Pourquoi bloquer les centrales énergétiques fongiques importe
Les maladies fongiques menacent les récoltes, les forêts et même les humains, et de nombreux fongicides modernes agissent en coupant l’approvisionnement énergétique du pathogène. Pourtant, jusqu’ici, personne n’avait observé en détail atomique comment ces molécules s’accrochent à leurs cibles fongiques. Cet article révèle la structure tridimensionnelle d’une enzyme clé de production d’énergie chez la levure de boulanger et montre exactement comment un fongicide largement utilisé, le bixafène, bloque cette machine moléculaire. Comme cette enzyme est étroitement apparentée chez de nombreux champignons pathogènes, ce travail ouvre la voie à la conception de fongicides plus intelligents, efficaces contre les menaces agricoles et médicales tout en étant plus sûrs pour les humains et l’environnement.
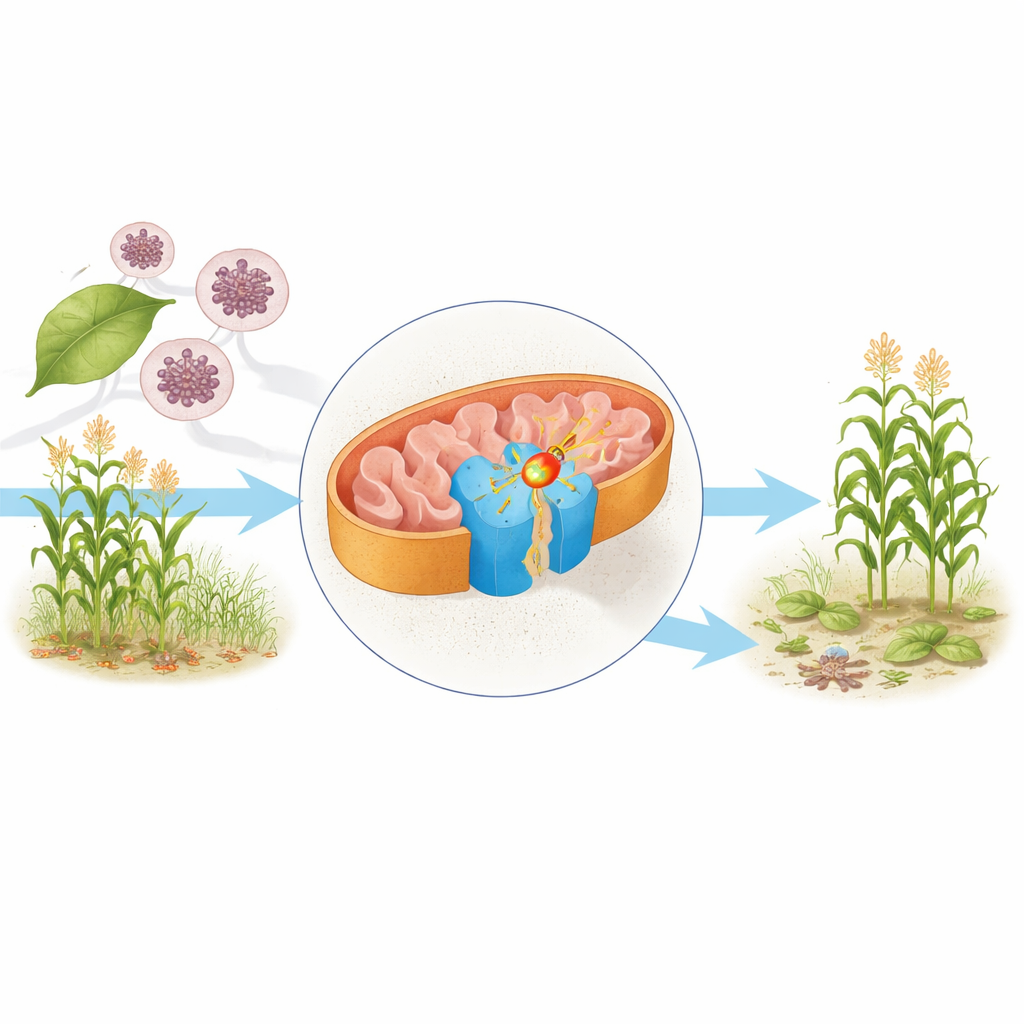
Le moteur cellulaire au microscope
À l’intérieur des mitochondries — souvent appelées centrales énergétiques de la cellule — les molécules alimentaires perdent des électrons qui finissent par aider à fabriquer l’ATP, le principal carburant cellulaire. Un composant central de cette machinerie est le complexe II, aussi appelé succinate déshydrogénase. Il relie le cycle de Krebs, qui dégrade les nutriments, à la chaîne respiratoire, qui convertit cette dégradation chimique en énergie exploitable. Les auteurs ont purifié le complexe II de la levure Saccharomyces cerevisiae, un organisme très utilisé en biologie, et ont employé la cryo‑microscopie électronique pour déterminer sa structure à une résolution quasi atomique dans deux états : l’un portant sa molécule naturelle transporteuse d’électrons, l’ubiquinone, et l’autre lié au fongicide bixafène.
Un moteur familier avec une pièce surprenante manquante
L’enzyme de la levure ressemble étroitement au complexe II des mammifères et d’autres organismes, avec deux grandes sous‑unités hydrophiles assurant la chimie et deux sous‑unités plus petites ancrées dans la membrane qui fixent le complexe dans la membrane mitochondriale. Les électrons voyagent d’un cofacteur flavine à travers une chaîne de clusters fer‑soufre vers la membrane, où l’ubiquinone les récupère normalement. Cependant, la structure révèle une surprise majeure : contrairement aux enzymes typiques du « type C » du complexe II, la version de la levure manque complètement d’un groupe hème — un cofacteur contenant du fer auparavant considéré comme une caractéristique universelle et stabilisante de cette famille. À la place, le complexe II de la levure s’appuie sur des liaisons hydrogène supplémentaires, des résidus plus hydrophobes et un phospholipide profondément enfoui pour coller ses sous‑unités membranaires et maintenir l’intégrité du complexe sans le hème.
Le fongicide dans la baie d’accostage
Au cœur de l’étude se trouve le soi‑disant site Q, la poche où l’ubiquinone s’ancre normalement pour recevoir des électrons. Dans la structure liée au bixafène, cette poche est comblée par le fongicide, qui imite nombre des interactions de l’ubiquinone mais établit aussi des contacts supplémentaires serrés. Des acides aminés clés issus de trois sous‑unités bercent l’inhibiteur par un mélange d’interactions polaires et hydrophobes, tandis qu’une extension flexible d’une sous‑unité membranaire (Sdh4) se replie dans le site et enrobe la queue hydrophobe du bixafène. Quand le substrat naturel est présent à la place, la pointe même de cette extension de Sdh4 devient désordonnée et laisse de la place pour la chaîne plus longue de l’ubiquinone, montrant que la poche peut s’adapter différemment au substrat et à l’inhibiteur.
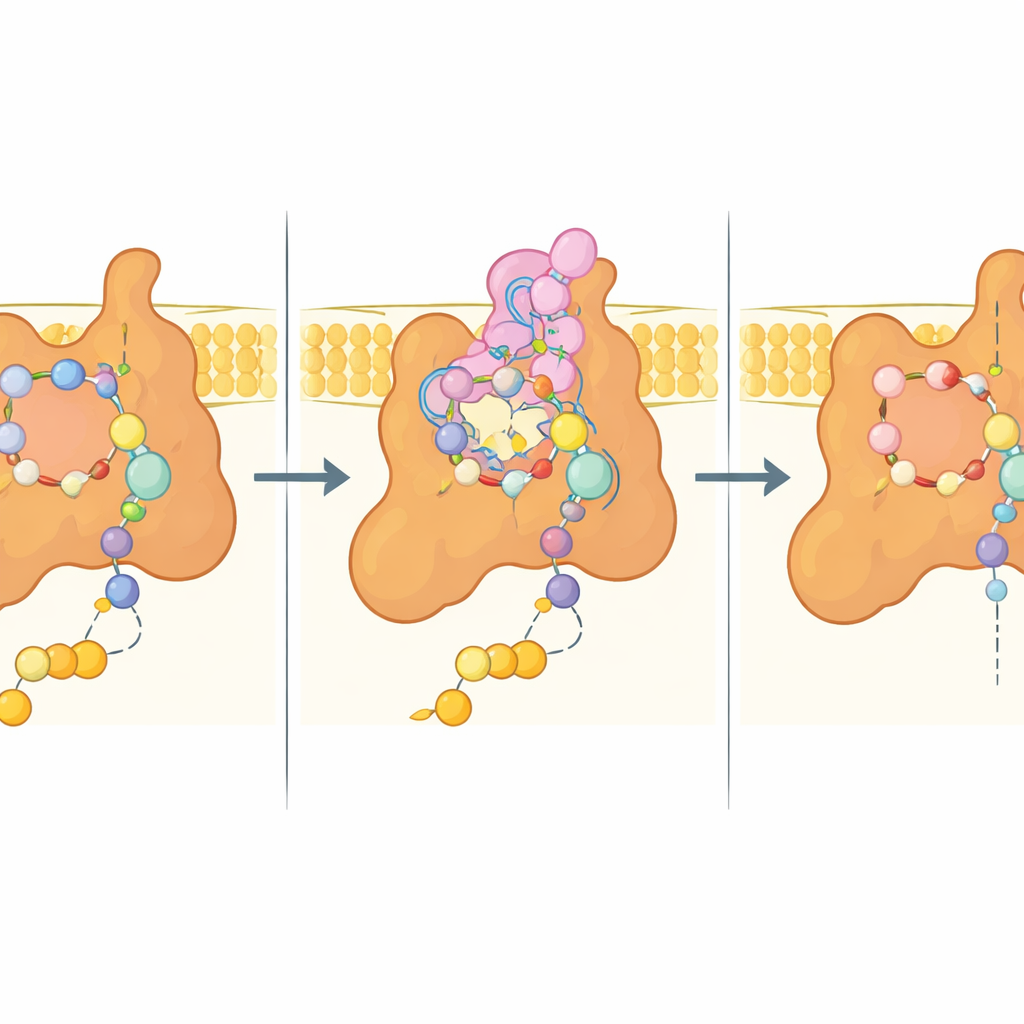
Indices pour les fongicides de nouvelle génération
Parce que de nombreux champignons d’importance agricole et pathogènes pour l’homme partagent des séquences de Sdh4 étroitement apparentées, en particulier dans cette extension N‑terminal, la structure de la levure reflète probablement l’architecture de leur complexe II. Les auteurs ont utilisé leur modèle expérimental pour effectuer des docking computationnels de plusieurs fongicides commerciaux inhibiteurs de la succinate déshydrogénase (SDHI), révélant une logique de liaison commune : un « noyau » carboxamide qui engage des acides aminés conservés, plus des décorations hydrophobes variables qui s’insèrent dans des poches voisines et modulant l’affinité et la spécificité. Il est important de noter que presque tous les résidus en contact avec le bixafène chez la levure sont conservés chez plusieurs pathogènes des cultures, ce qui suggère que des différences séquentielles subtiles pourraient expliquer pourquoi certaines espèces sont plus ou moins sensibles — et pourquoi certaines mutations confèrent une résistance sur le terrain.
De la carte structurale à l’impact pratique
En termes simples, l’étude fournit un plan détaillé de la façon dont une grande classe de fongicides s’insère dans une enzyme énergétique fongique et la désactive. Elle renverse aussi des hypothèses sur un composant hémique supposément universel et montre comment la levure a évolué des caractéristiques stabilisatrices alternatives. Avec cette carte structurale, les chercheurs peuvent maintenant ajuster de manière rationnelle des fongicides existants ou en inventer de nouveaux qui exploitent mieux des caractéristiques spécifiques aux champignons, qui réduisent les risques de résistance et qui minimisent les dommages hors cible aux cultures, à la faune et aux personnes. La levure de boulanger, longtemps appréciée pour le pain et la bière, devient ainsi un modèle puissant pour concevoir la prochaine génération d’armes antifongiques ciblées.
Citation: Pinotsis, N., Burn-Leefe, C., Jones, S. et al. Cryo-EM structure of bixafen-bound S. cerevisiae complex II unravels SDHI specificity against pathogenic fungi. Commun Biol 9, 517 (2026). https://doi.org/10.1038/s42003-026-09617-8
Mots-clés: succinate déshydrogénase, résistance aux fongicides, cryo-microscopie électronique, respiration mitochondriale, fongicides SDHI