Clear Sky Science · ar
البنية بالمجهر الإلكتروني المبرد لـ complex II في S. cerevisiae عند ارتباطه ببكسافين تكشف خصوصية SDHI تجاه الفطريات الممرِضة
لماذا يهم تعطيل مصانع طاقة الفطريات
تشكل الأمراض الفطرية تهديداً للمحاصيل والغابات وحتى للناس، وكثير من المبيدات الفطرية الحديثة تعمل عن طريق قطع مصدر الطاقة للمُمْرِض. ومع ذلك، لم يسبق لأحد أن رأى بالتفصيل الذري كيف تلتصق هذه المركبات بأهدافها الفطرية. تكشف هذه الورقة البنية ثلاثية الأبعاد لإنزيم حاسم لإنتاج الطاقة من خميرة الخَبز وتُظهر بالضبط كيف يعيق المبيد الشائع بكسافين هذه الآلة الجزيئية. ونظراً لأن هذا الإنزيم مرتبط ارتباطاً وثيقاً في العديد من الفطريات الممرِضة، فإن العمل يفتح الباب لتصميم مبيدات أكثر ذكاءً تكون فعّالة ضد تهديدات المحاصيل والطبية وفي الوقت نفسه أكثر أماناً للبشر والبيئة.
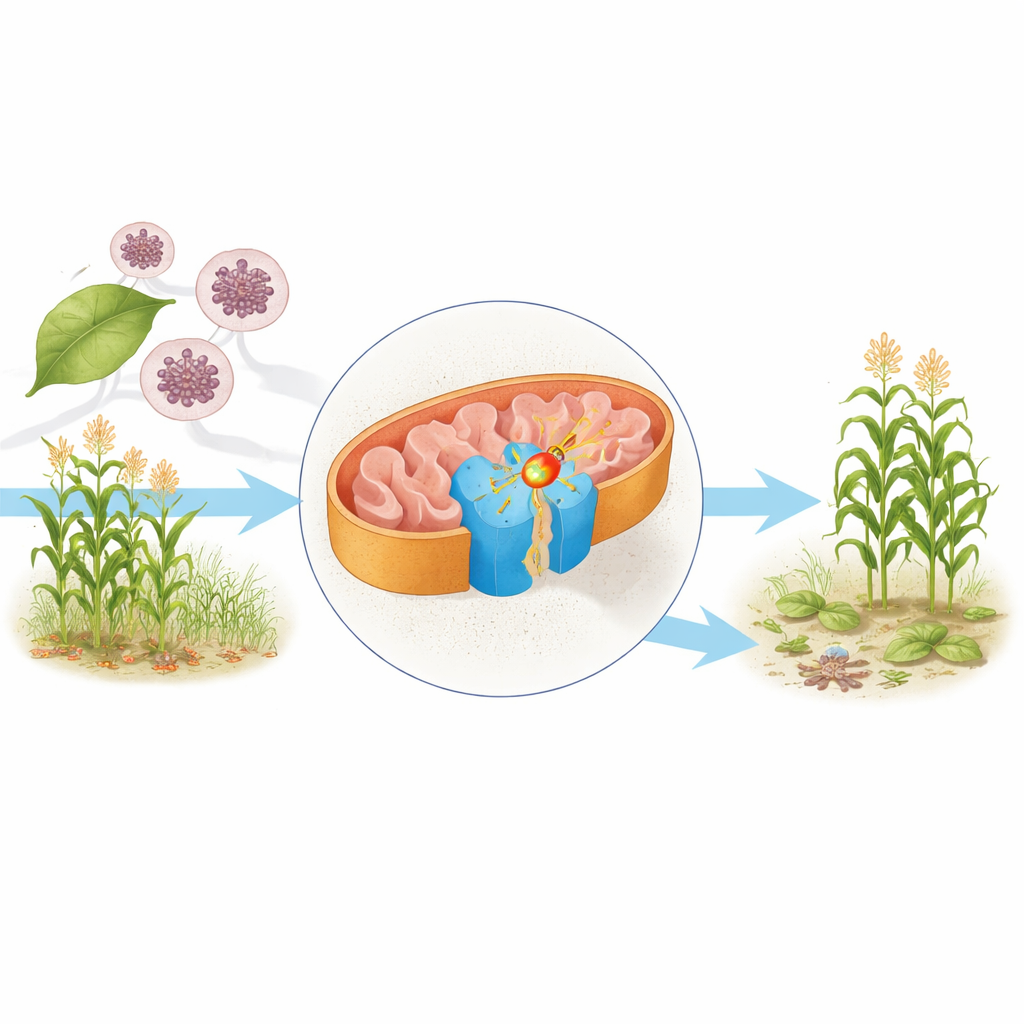
محرك الخلية تحت المجهر
داخل الميتوكوندريا—التي غالباً ما تُسمى مصانع طاقة الخلية—تُزال الإلكترونات من جزيئات الغذاء التي تساعد في نهاية المطاف على إنتاج ATP، الوقود الرئيسي للخلية. أحد المكوّنات المركزية في هذه الآلة هو المركب II، المعروف أيضاً باسم خَفَاضُ حمض السّكسينات. يربط دورة كريبس، التي تكسر المغذيات، بسلسلة التنفس التي تحول هذا التفكك الكيميائي إلى طاقة قابلة للاستخدام. نقّى المؤلفون المركب II من خميرة Saccharomyces cerevisiae، وهي كائن عمل مُستخدم على نطاق واسع في علم الأحياء، واستخدموا المجهر الإلكتروني المبرد لتحديد بنيته بدقة قُرابة ذرّية في شكلين: أحدهما محمّل بجزيء ناقل الإلكترون الطبيعي، الأوبيكوينون، والآخر مرتبط بالمبيد الفطري بكسافين.
محرك مألوف مع جزء مفقود مفاجئ
يشبه إنزيم الخميرة عن كثب المركب II في الثدييات وكائنات أخرى، مع عددين كبيرين من الوحدات المحبة للماء التي تتعامل مع التفاعلات الكيميائية ووحدتين أصغر مدمجتين في الغشاء تَرْسِخان المركب في غشاء الميتوكوندريا. تنتقل الإلكترونات من عامل فلافين عبر سلسلة من عناقيد الحديد–كبريت نحو الغشاء حيث يلتقطها عادةً الأوبيكوينون. ومع ذلك تكشف البنية عن مفاجأة كبيرة: خلافاً لإنزيمات المركب II من النوع "C" النمطية، فإن نسخة الخميرة تفتقر تماماً إلى مجموعة الهيِم—العامل الحاوي للحديد الذي كان يُعتقد سابقاً بأنه ميزة عالمية لتثبيت هذه العائلة. بدلاً من ذلك، يعتمد مركب II في الخميرة على روابط هيدروجينية إضافية وبقايا أكثر كارهة للماء وشحْم فسفوليبيدي غارق عميقاً لِلْتَصاق وحداته الغشائية معاً والحفاظ على سلامة المركب بدون الهيِم.
المبيد في حجرة التمركز
في صميم الدراسة يوجد ما يُعرف بموقع Q، الجيب الذي يرتكز فيه الأوبيكوينون عادة لالتقاط الإلكترونات. في البنية المرتبطة ببكسافين، هذا الجيب مملوء بالمبيد، الذي يحاكي العديد من تفاعلات الأوبيكوينون لكنه يُكوّن أيضاً اتصالات إضافية مُتراصّة. تُحضِن حمض أمينيّة رئيسية من ثلاث وحدات المُثبّط عبر مزيج من التفاعلات القطبية والشهِية للماء، بينما يمتد جزء مرن من إحدى الوحدات الغشائية (Sdh4) إلى داخل الموقع ويلتف حول ذيل بكسافين المحب للماء. عندما يكون الركيزة الطبيعية حاضرة بدلاً من ذلك، يصبح طرف هذا الامتداد في Sdh4 غير منظم ويترك مساحة لسلسلة الأوبيكوينون الأطول، مما يُظهر أن الجيب يمكن أن يتكيّف بطرق مختلفة مع الركيزة والمثبط.
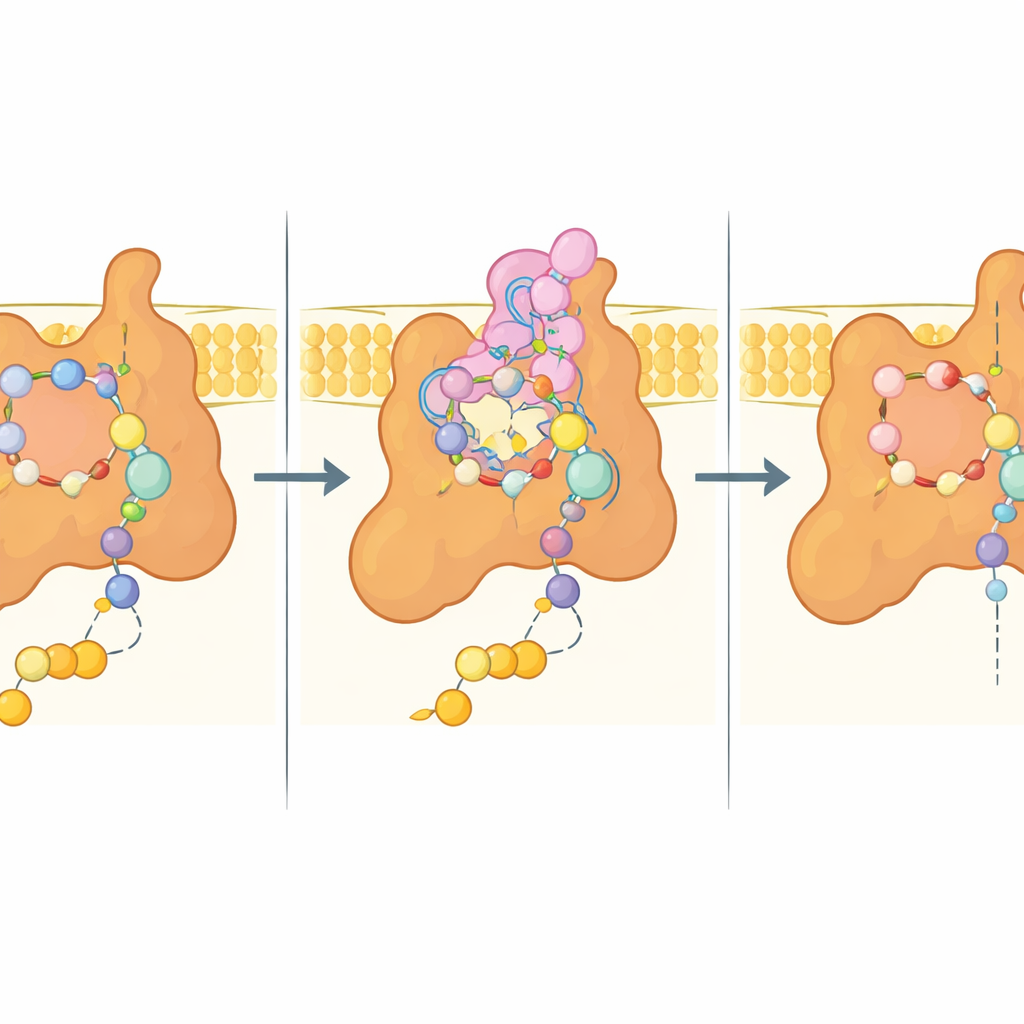
دلائل لمبيدات الجيل القادم
بما أن العديد من الفطريات المهمة زراعياً والممرِضة للإنسان تشترك في تسلسلات Sdh4 متقاربة، خصوصاً في هذا الامتداد الطرفي N، فإن بنية الخميرة على الأرجح تعكس معمارية المركب II لديهم. استخدم المؤلفون نموذجهم التجريبي لوضع عدة مبيدات تجارية مثبطة لخَفَاض حمض السّكسينات (SDHI) حسابياً، كاشفين عن منطق ربط مشترك: «لبّ» كربوكساميد يتفاعل مع أحماض أمينية محفوظة، مع زينة شهية للماء متغيرة تناسب جيوباً مجاورة وتُعدّل القوة والنوعية. ومن المهم أن شبه جميع البقايا التي تلامس بكسافين في الخميرة محفوظة في العديد من مسببات الأمراض النباتية، ما يشير إلى أن اختلافات متناهية في التسلسل قد تفسر لماذا بعض الأنواع أكثر أو أقل حساسية—ولماذا تمنح طفرات معينة مقاومة في الحقل.
من الخريطة البنائية إلى الأثر العملي
بعبارات بسيطة، توفر الدراسة مخططاً تفصيلياً لكيفية اقتحام فئة رئيسية من المبيدات الفطرية لإنزيم طاقة فطري وإيقافه. كما تُطْحِن افتراضات حول مكوّن الهيِم المفترض كأنه عالمي وتُظهر كيف طورت الخميرة ميزات تثبيت بديلة. بوجود هذه الخريطة البنائية، يمكن للباحثين الآن تعديل المبيدات الحالية بعقلانية أو ابتكار مبيدات جديدة تستغل ميزات خاصة بالفطريات، تقلل فرص المقاومة، وتحد من الضرر خارج الهدف للمحاصيل والحياة البرية والبشر. وبذلك تتحوّل خميرة الخبز، المحبوبة قديماً للخبز والبيرة، إلى نموذج قوي لبناء الجيل القادم من الأسلحة المضادّة للفطريات المستهدفة.
الاستشهاد: Pinotsis, N., Burn-Leefe, C., Jones, S. et al. Cryo-EM structure of bixafen-bound S. cerevisiae complex II unravels SDHI specificity against pathogenic fungi. Commun Biol 9, 517 (2026). https://doi.org/10.1038/s42003-026-09617-8
الكلمات المفتاحية: خَفَاضُ حمض السّكسينات, مقاومة المبيدات الفطرية, المجهر الإلكتروني المبرد, تنفّس الميتوكوندريا, مبيدات SDHI الفطرية