Clear Sky Science · es
Estructura por crio‑EM del complejo II de S. cerevisiae unido a bixafén desentraña la especificidad de los SDHI frente a hongos patógenos
Por qué importa bloquear las centrales energéticas de los hongos
Las enfermedades fúngicas amenazan cosechas, bosques e incluso a las personas, y muchos fungicidas modernos actúan cortando el suministro de energía del patógeno. Sin embargo, hasta ahora nadie había observado en detalle atómico cómo estos compuestos se fijan a sus blancos fúngicos. Este artículo revela la estructura tridimensional de una enzima clave productora de energía de la levadura de panadería y muestra exactamente cómo un fungicida de uso extendido, el bixafén, bloquea esta máquina molecular. Dado que esta enzima está íntimamente relacionada en muchos hongos patógenos, el trabajo abre la puerta a diseñar fungicidas más inteligentes que sean potentes contra amenazas agrícolas y médicas, pero más seguros para las personas y el medio ambiente.
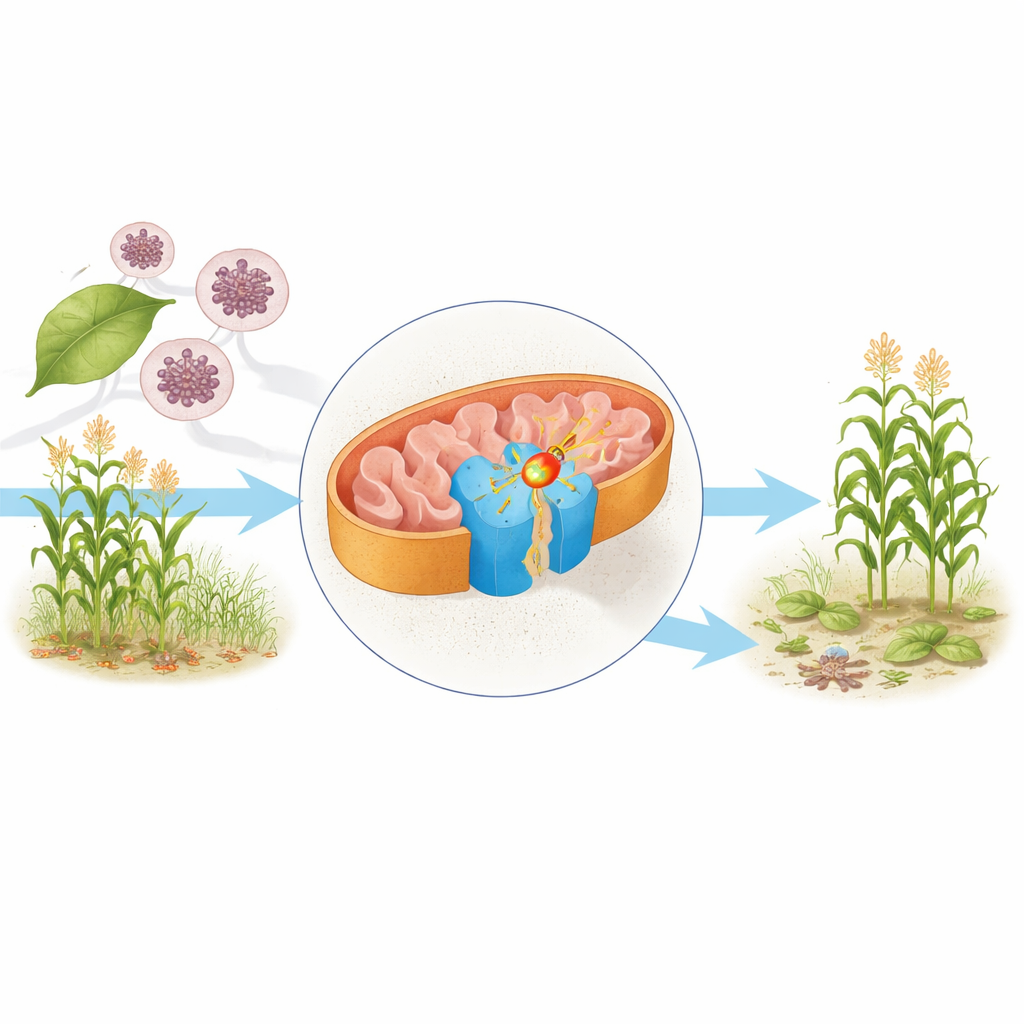
El motor celular bajo el microscopio
En el interior de las mitocondrias —a menudo llamadas las centrales energéticas de la célula— las moléculas alimenticias son despojadas de electrones que acaban ayudando a fabricar ATP, el combustible principal de la célula. Un componente central de este conjunto es el complejo II, también conocido como succinato deshidrogenasa. Conecta el ciclo de Krebs, que descompone nutrientes, con la cadena respiratoria, que convierte esa descomposición química en energía utilizable. Los autores purificaron el complejo II de la levadura Saccharomyces cerevisiae, un organismo ampliamente utilizado en biología, y emplearon crio‑microscopía electrónica para determinar su estructura a resolución cercana a la atómica en dos formas: una portando su molécula natural transportadora de electrones, la ubiquinona, y otra unida al fungicida bixafén.
Un motor conocido con una pieza sorprendentemente ausente
La enzima de la levadura se parece mucho al complejo II de mamíferos y otros organismos, con dos subunidades grandes hidrofílicas que llevan a cabo la química y dos subunidades más pequeñas incrustadas en la membrana que anclan el complejo en la membrana mitocondrial. Los electrones viajan desde un cofactor flavínico a través de una cadena de cúmulos hierro‑azufre hacia la membrana, donde la ubiquinona normalmente los recoge. Sin embargo, la estructura revela una sorpresa mayor: a diferencia de los típicos enzimas del “tipo C” del complejo II, la versión de la levadura carece por completo de un grupo hemo —un cofactor que contiene hierro que antes se pensaba era una característica estabilizadora universal de esta familia. En su lugar, el complejo II de levadura depende de enlaces de hidrógeno adicionales, residuos más hidrofóbicos y de un fosfolípido profundamente enterrado para pegar sus subunidades de membrana y mantener el complejo estable sin el hemo.
El fungicida en la bahía de acoplamiento
En el corazón del estudio está el llamado sitio Q, el bolsillo donde la ubiquinona normalmente se acopla para recibir electrones. En la estructura con bixafén, este bolsillo está ocupado por el fungicida, que imita muchas de las interacciones de la ubiquinona pero además establece contactos adjuntos más ceñidos. Aminoácidos clave de tres subunidades acunan al inhibidor mediante una mezcla de interacciones polares e hidrofóbicas, mientras que una extensión flexible de una subunidad de membrana (Sdh4) se pliega dentro del sitio y rodea la cola hidrofóbica del bixafén. Cuando está presente el sustrato natural, la punta de esta extensión N‑terminal de Sdh4 se vuelve desordenada y deja espacio para la cadena más larga de la ubiquinona, demostrando que el bolsillo puede adaptarse de distintas maneras al sustrato y al inhibidor.
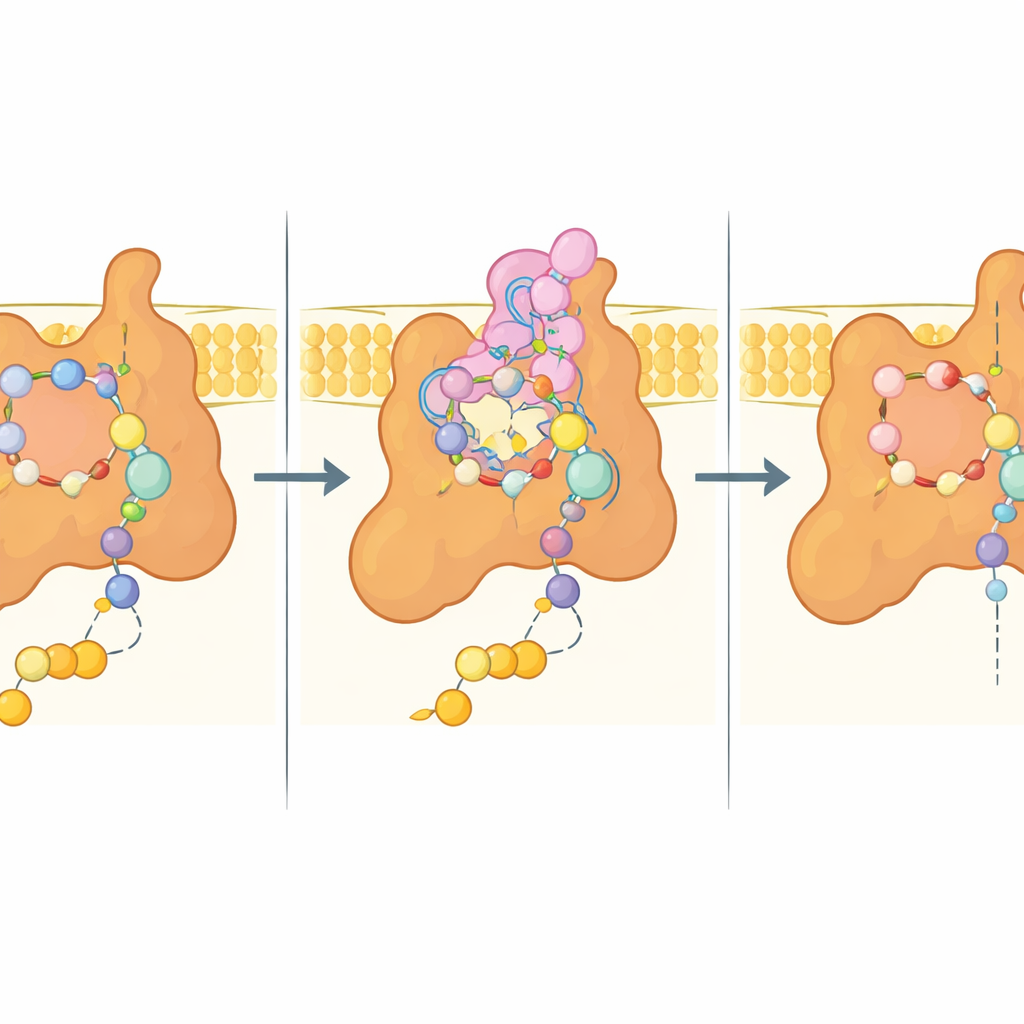
Pistas para fungicidas de próxima generación
Dado que muchos hongos importantes en agricultura y patógenos humanos comparten secuencias de Sdh4 estrechamente relacionadas, especialmente en esta extensión N‑terminal, es probable que la estructura de la levadura refleje la arquitectura de su complejo II. Los autores utilizaron su modelo experimental para acoplar por métodos computacionales varios fungicidas comerciales inhibidores de la succinato deshidrogenasa (SDHI), revelando una lógica de unión común: un “núcleo” carboxamida que interactúa con aminoácidos conservados, además de decoraciones hidrofóbicas variables que encajan en bolsillos cercanos y modulan la potencia y especificidad. Importantly, casi todos los residuos que contactan al bixafén en la levadura están conservados en múltiples patógenos de cultivos, lo que sugiere que diferencias sutiles en la secuencia podrían explicar por qué algunas especies son más o menos sensibles, y por qué ciertas mutaciones confieren resistencia en el campo.
Del mapa estructural al impacto práctico
En términos sencillos, el estudio proporciona un plano detallado de cómo una clase importante de fungicidas se introduce en una enzima energética fúngica y la bloquea. También revierte suposiciones sobre un componente hemo supuestamente universal y muestra cómo la levadura ha evolucionado características estabilizadoras alternativas. Con este mapa estructural, los investigadores pueden ahora ajustar racionalmente fungicidas existentes o inventar otros nuevos que exploten mejor rasgos específicos de los hongos, reduzcan las probabilidades de resistencia y minimicen daños fuera del objetivo a cultivos, fauna y personas. La levadura de panadería, largamente apreciada por el pan y la cerveza, se convierte así en un modelo poderoso para construir la próxima generación de armas antifúngicas dirigidas.
Cita: Pinotsis, N., Burn-Leefe, C., Jones, S. et al. Cryo-EM structure of bixafen-bound S. cerevisiae complex II unravels SDHI specificity against pathogenic fungi. Commun Biol 9, 517 (2026). https://doi.org/10.1038/s42003-026-09617-8
Palabras clave: succinato deshidrogenasa, resistencia a fungicidas, crio‑microscopía electrónica, respiración mitocondrial, fungicidas SDHI