Clear Sky Science · de
Cryo‑EM-Struktur von bixafen‑gebundenem S. cerevisiae Komplex II enthüllt SDHI‑Spezifität gegen pathogene Pilze
Warum das Stilllegen der Pilz‑Kraftwerke wichtig ist
Pilzkrankheiten bedrohen Ernten, Wälder und sogar Menschen, und viele moderne Fungizide wirken, indem sie dem Erreger die Energiezufuhr abschneiden. Bislang aber hatte noch niemand auf atomarer Ebene gesehen, wie diese Chemikalien an ihre pilzlichen Zielmoleküle andocken. Diese Arbeit legt die dreidimensionale Struktur eines zentralen Energie erzeugenden Enzyms der Bäckerhefe offen und zeigt genau, wie ein breit eingesetztes Fungizid, Bixafen, diese molekulare Maschine blockiert. Da dieses Enzym in vielen pathogenen Pilzen eng verwandt ist, eröffnet die Studie Möglichkeiten, intelligenter konzipierte Fungizide zu entwickeln, die gegen landwirtschaftliche und medizinische Bedrohungen wirksam sind, aber für Menschen und Umwelt sicherer.
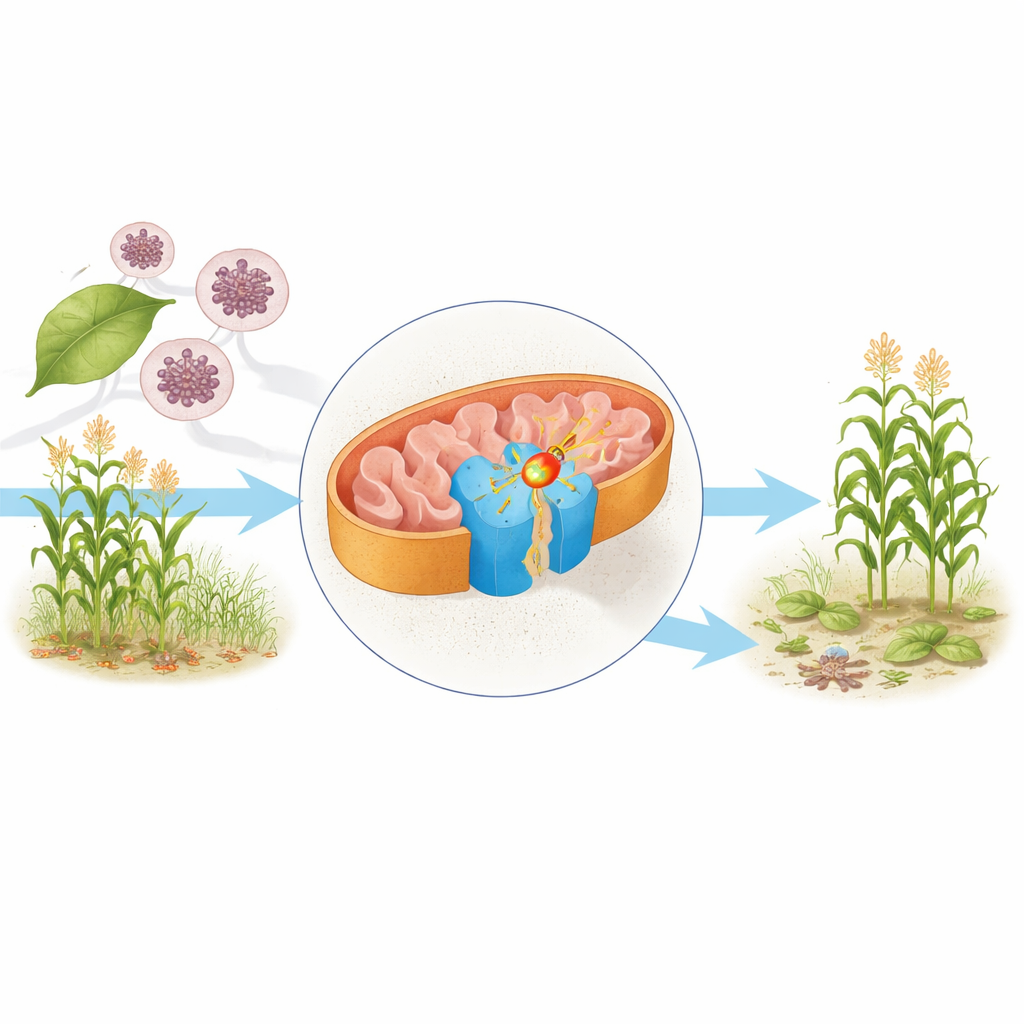
Der Zellmotor unter dem Mikroskop
In den Mitochondrien – oft als Kraftwerke der Zelle bezeichnet – werden Nahrungsmoleküle Elektronen entzogen, die schließlich helfen, ATP herzustellen, den wichtigsten Energieträger der Zelle. Ein zentrales Element dieser Maschinerie ist Komplex II, auch Succinatdehydrogenase genannt. Er verbindet den Krebs‑Zyklus, der Nährstoffe abbaut, mit der Atmungskette, die diesen chemischen Abbau in nutzbare Energie umwandelt. Die Autoren reinigten Komplex II aus der Hefe Saccharomyces cerevisiae, einem vielgenutzten Modellorganismus, und bestimmten seine Struktur mittels Kryo‑Elektronenmikroskopie in nahezu atomarer Auflösung in zwei Zuständen: einmal mit seinem natürlichen Elektronenträger Ubiquinon und einmal mit dem an das Fungizid Bixafen gebundenen Zustand.
Ein vertrauter Motor mit überraschend fehlendem Bauteil
Das Hefeenzym ähnelt dem Komplex II von Säugetieren und anderen Organismen: zwei große, wasserliebende Untereinheiten übernehmen die chemischen Reaktionen, zwei kleinere, membranverankerte Untereinheiten verankern den Komplex in der mitochondrialen Membran. Elektronen wandern von einem Flavin‑Cofaktor durch eine Kette von Eisen‑Schwefel‑Clustern zur Membran, wo normalerweise Ubiquinon sie aufnimmt. Die Struktur enthüllt jedoch eine große Überraschung: Im Gegensatz zu typischen „Typ‑C“‑Komplex‑II‑Enzymen fehlt der Hefe vollständig eine Häm‑Gruppe—ein eisenhaltiger Cofaktor, der bisher als universelles stabilisierendes Merkmal dieser Familie galt. Stattdessen stützt sich der Hefe‑Komplex II auf zusätzliche Wasserstoffbrücken, hydrophobe Aminosäurereste und ein tief eingebettetes Phospholipid, die die Membranuntereinheiten zusammenhalten und den Komplex auch ohne Häm stabilisieren.
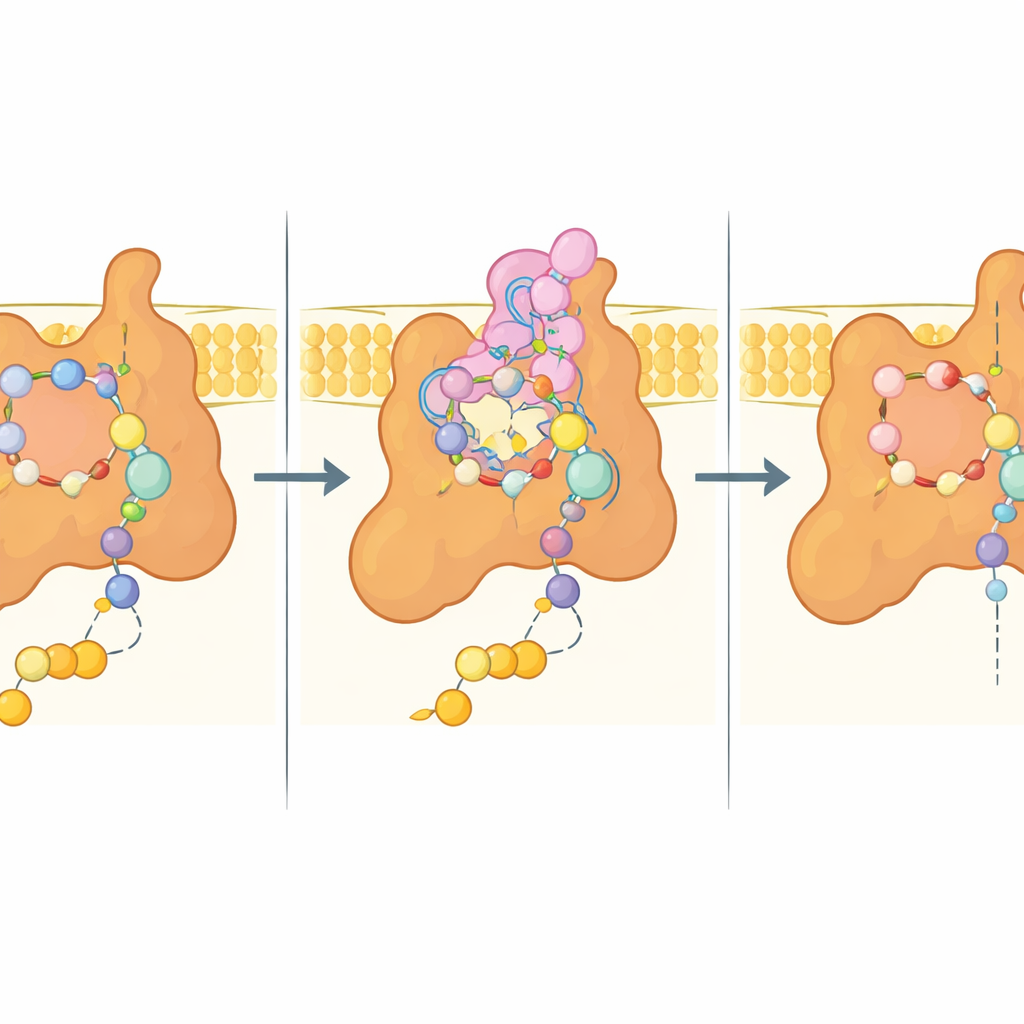
Fungizid in der Andockbucht
Im Zentrum der Studie steht die sogenannte Q‑Stelle, die Tasche, in der Ubiquinon normalerweise andockt, um Elektronen aufzunehmen. In der bixafen‑gebundenen Struktur ist diese Tasche vom Fungizid ausgefüllt, das viele der Ubiquinon‑Wechselwirkungen nachahmt, aber auch zusätzliche enge Kontakte eingeht. Schlüsselaminosäuren aus drei Untereinheiten umschließen den Inhibitor durch eine Mischung aus polaren und hydrophoben Wechselwirkungen, während eine flexible Ausstülpung einer Membranuntereinheit (Sdh4) in die Stelle einfaltet und den hydrophoben Schwanz von Bixafen umschließt. Ist stattdessen das natürliche Substrat vorhanden, wird die sehr Spitze dieser Sdh4‑Erweiterung ungeordnet und schafft Raum für die längere Kette des Ubiquinons, was zeigt, dass die Tasche sich unterschiedlich an Substrat und Inhibitor anpassen kann.
Hinweise für Fungizide der nächsten Generation
Da viele landwirtschaftlich bedeutsame und humanpathogene Pilze eng verwandte Sdh4‑Sequenzen aufweisen, insbesondere in dieser N‑terminalen Verlängerung, spiegelt die Hefe‑Struktur wahrscheinlich die Architektur ihres Komplex II wider. Die Autoren nutzten ihr experimentelles Modell, um mehrere kommerzielle Succinatdehydrogenase‑Inhibitoren (SDHIs) rechnerisch zu docken und offenbarten eine gemeinsame Bindungslogik: ein Carboxamid‑„Core“, das konservierte Aminosäuren anspricht, sowie variable hydrophobe Anhängsel, die in benachbarte Taschen passen und Wirkstärke sowie Spezifität modulieren. Wichtig ist, dass nahezu alle Reste, die in der Hefe mit Bixafen in Kontakt stehen, in mehreren Pflanzenpathogenen konserviert sind, was nahelegt, dass subtile Sequenzunterschiede erklären könnten, warum einige Arten empfindlicher oder weniger empfindlich sind – und warum bestimmte Mutationen in Feldpopulationen Resistenz vermitteln.
Von der Strukturkarte zur praktischen Wirkung
Einfach gesagt liefert die Studie einen detaillierten Bauplan, wie eine große Klasse von Fungiziden sich in ein pilzliches Energieenzym einklinkt und es lahmlegt. Sie widerlegt zudem Annahmen über ein vermeintlich universelles Häm‑Bauteil und zeigt, wie die Hefe alternative stabilisierende Merkmale entwickelt hat. Mit dieser Strukturkarte können Forschende bestehende Fungizide gezielt modifizieren oder neue entwerfen, die pilzspezifische Merkmale besser ausnutzen, die Wahrscheinlichkeit von Resistenz verringern und unerwünschte Effekte auf Nutzpflanzen, Tiere und Menschen minimieren. Die Bäckerhefe, lange geliebt für Brot und Bier, wird damit zu einem kraftvollen Modell für die Entwicklung der nächsten Generation zielgerichteter Antipilz‑Strategien.
Zitation: Pinotsis, N., Burn-Leefe, C., Jones, S. et al. Cryo-EM structure of bixafen-bound S. cerevisiae complex II unravels SDHI specificity against pathogenic fungi. Commun Biol 9, 517 (2026). https://doi.org/10.1038/s42003-026-09617-8
Schlüsselwörter: Succinatdehydrogenase, Fungizidresistenz, Cryo‑Elektronenmikroskopie, mitochondriale Atmung, SDHI‑Fungizide