Clear Sky Science · pl
Struktura Cryo-EM kompleksu II z S. cerevisiae związana z bixafenem ujawnia specyfikę SDHI wobec grzybów patogenicznych
Dlaczego blokowanie „elektrowni” grzybów ma znaczenie
Choroby grzybicze zagrażają plonom, lasom, a nawet ludziom; wiele współczesnych fungicydów działa przez odcięcie patogenowi dostępu do energii. Jednak dotąd nikt nie widział w szczegółach atomowych, jak te związki przyczepiają się do swoich grzybowych celów. Artykuł ujawnia trójwymiarową strukturę kluczowego enzymu produkującego energię z drożdży piekarskich i pokazuje dokładnie, jak powszechnie stosowany fungicyd bixafen blokuje tę molekularną maszynę. Ponieważ enzym ten jest blisko spokrewniony w wielu grzybach patogenicznych, praca otwiera drogę do projektowania mądrzejszych fungicydów, które będą skuteczne przeciwko zagrożeniom dla upraw i medycyny, a jednocześnie bezpieczniejsze dla ludzi i środowiska.
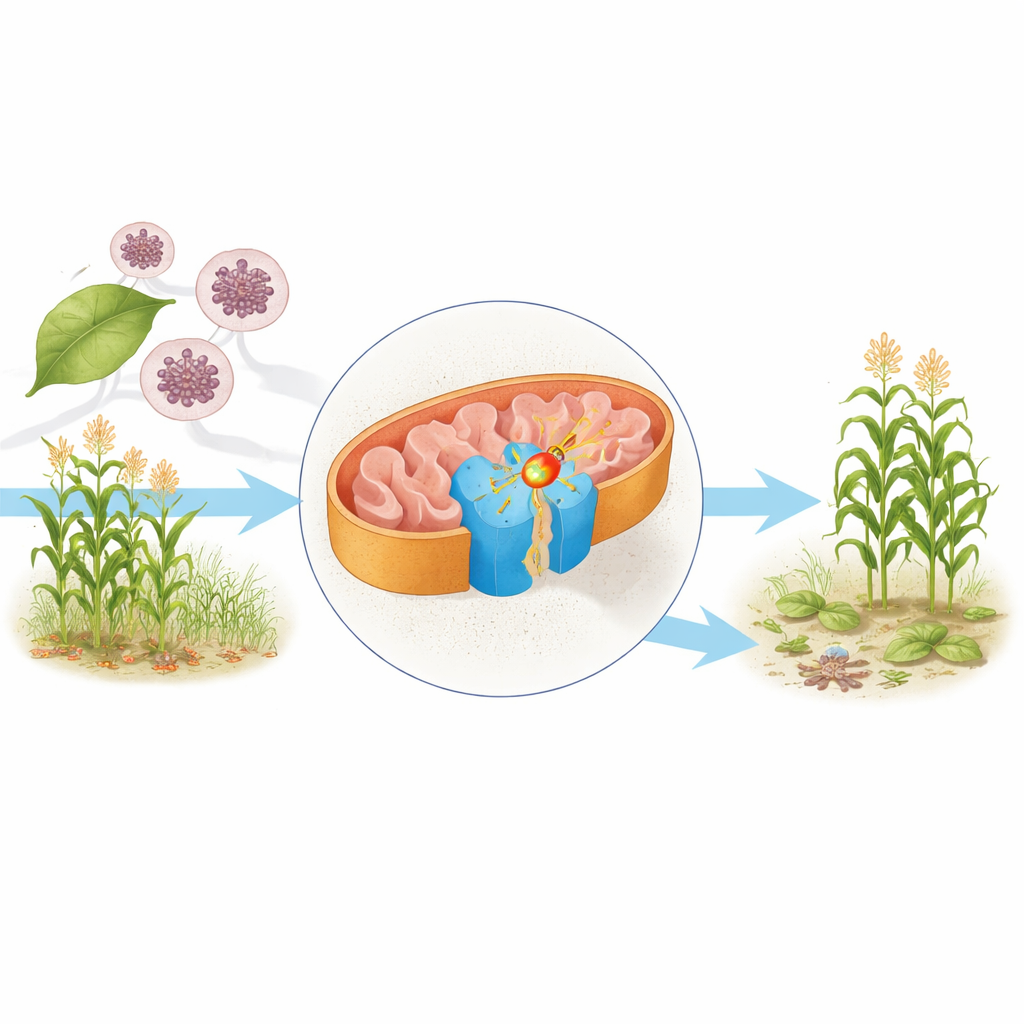
Silnik komórkowy pod mikroskopem
W mitochondriach — często nazywanych elektrowniami komórki — cząsteczki pokarmowe tracą elektrony, które ostatecznie pomagają wytwarzać ATP, główne paliwo komórki. Jednym z centralnych elementów tego układu jest kompleks II, znany również jako dehydrogenaza bursztynianowa. Łączy on cykl Krebsa, który rozkłada składniki odżywcze, z łańcuchem oddechowym, który przekształca ten rozkład w użyteczną energię. Autorzy oczyszczali kompleks II z drożdża Saccharomyces cerevisiae, organizmu powszechnie używanego w biologii, i zastosowali kriomikroskopię elektronową, aby określić jego strukturę w niemal atomowej rozdzielczości w dwóch formach: z naturalnym przenośnikiem elektronów, ubichinonem, oraz związaną z fungicydem bixafenem.
Znany „silnik” z zaskakującą brakującą częścią
Enzym drożdżowy przypomina bardzo kompleks II z ssaków i innych organizmów, z dwoma dużymi hydrofilowymi podjednostkami odpowiadającymi za reakcje chemiczne oraz dwiema mniejszymi, osadzonymi w błonie, kotwiczącymi kompleks w błonie mitochondrialnej. Elektrony przechodzą od kofaktora flawinowego przez łańcuch klastrów żelazo–siarka w kierunku błony, gdzie normalnie przejmuje je ubichinon. Jednak struktura ujawnia istotne zaskoczenie: w przeciwieństwie do typowych enzymów kompleksu II „typu C”, wersja drożdżowa całkowicie nie zawiera grupy hemowej — kofaktora zawierającego żelazo, uważanego wcześniej za uniwersalny element stabilizujący tę rodzinę. Zamiast niego kompleks II drożdży polega na dodatkowych wiązaniach wodorowych, bardziej hydrofobowych resztach i głęboko zakopanym fosfolipidzie, które sklejają podjednostki błonowe i utrzymują kompleks bez hemu.
Fungicyd w zatoce dokującej
W centrum badania znajduje się tzw. miejsce Q, kieszeń, w której ubichinon zwykle dokuje, aby odebrać elektrony. W strukturze związanej z bixafenem tę kieszeń wypełnia fungicyd, który naśladuje wiele interakcji ubichinonu, ale tworzy też dodatkowe ciasne kontakty. Kluczowe aminokwasy z trzech podjednostek obejmują inhibitor mieszanką interakcji polarnych i hydrofobowych, podczas gdy elastyczne przedłużenie jednej z podjednostek błonowych (Sdh4) składa się do wnętrza miejsca i owija wokół hydrofobowego ogona bixafenu. Gdy obecny jest naturalny substrat, sam koniec tego przedłużenia Sdh4 staje się nieuporządkowany i ustępuje miejsca dłuższemu łańcuchowi ubichinonu, co pokazuje, że kieszeń może adaptować się na różne sposoby do substratu i inhibitora.
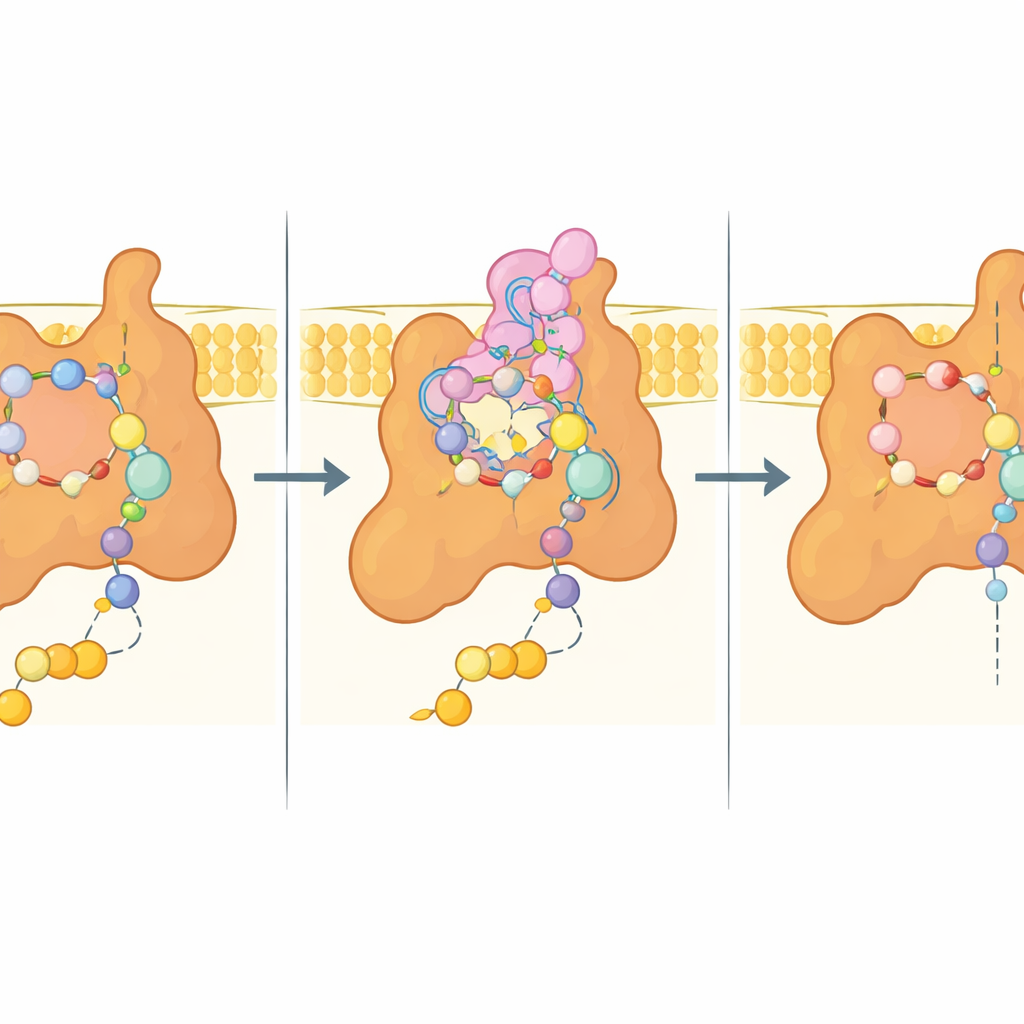
Wskazówki dla kolejnej generacji fungicydów
Ponieważ wiele ważnych rolniczo i medycznie gatunków grzybów ma ściśle spokrewnione sekwencje Sdh4, zwłaszcza w tym N‑terminalnym przedłużeniu, struktura drożdżowa prawdopodobnie odzwierciedla architekturę ich kompleksu II. Autorzy użyli modelu eksperymentalnego do obliczeniowego dokowania kilku komercyjnych inhibitorów dehydrogenazy bursztynianowej (SDHI), ujawniając wspólną logikę wiązania: karboksamidowe „jądro”, które angażuje zachowane aminokwasy, oraz zmienne hydrofobowe ozdoby, które wpasowują się w pobliskie kieszenie i modulują siłę oraz specyfikę. Co istotne, niemal wszystkie reszty kontaktujące bixafen w drożdżach są zachowane w wielu patogenach uprawnych, co sugeruje, że subtelne różnice w sekwencji mogą wyjaśniać, dlaczego niektóre gatunki są bardziej lub mniej wrażliwe — i dlaczego pewne mutacje nadają oporność w praktyce polowej.
Od mapy strukturalnej do praktycznego wpływu
Mówiąc wprost, badanie dostarcza szczegółowego planu tego, jak główna klasa fungicydów klinuje się w enzymie energetycznym grzyba i go wyłącza. Obala też założenia dotyczące rzekomo uniwersalnego komponentu hemowego i pokazuje, jak drożdże wyewoluowały alternatywne cechy stabilizujące. Dzięki tej mapie strukturalnej naukowcy mogą teraz racjonalnie modyfikować istniejące fungicydy lub tworzyć nowe, które lepiej wykorzystają unikalne cechy grzybów, zmniejszą ryzyko oporności i zminimalizują działania uboczne wobec upraw, dzikiej przyrody i ludzi. Drożdże piekarskie, od dawna cenione w chlebie i piwie, stają się potężnym modelem do budowy następnej generacji ukierunkowanych środków przeciwgrzybiczych.
Cytowanie: Pinotsis, N., Burn-Leefe, C., Jones, S. et al. Cryo-EM structure of bixafen-bound S. cerevisiae complex II unravels SDHI specificity against pathogenic fungi. Commun Biol 9, 517 (2026). https://doi.org/10.1038/s42003-026-09617-8
Słowa kluczowe: dehydrogenaza bursztynianowa, oporność na fungicydy, kriotronowa mikroskopia elektronowa, oddychanie mitochondrialne, fungicydy SDHI