Clear Sky Science · nl
Cryo-EM-structuur van bixafen-gebonden S. cerevisiae complex II onthult SDHI-specificiteit tegen pathogene schimmels
Waarom het blokkeren van schimmel‑energiecentrales ertoe doet
Schimmelziekten bedreigen oogsten, bossen en zelfs mensen, en veel moderne fungiciden werken door de energievoorziening van de ziekteverwekker af te snijden. Tot nu toe had echter nog niemand in atomair detail gezien hoe deze chemische stoffen zich vastklampen aan hun schimmeldoelen. Dit artikel onthult de driedimensionale structuur van een cruciaal energieproducerend enzym uit bakkersgist en toont precies hoe een veelgebruikt fungicide, bixafen, dit moleculaire apparaat blokkeert. Omdat dit enzym nauw verwant is aan dat van vele pathogene schimmels, opent het werk de deur naar het ontwerpen van slimere fungiciden die doeltreffend zijn tegen landbouw- en medische bedreigingen maar veiliger voor mensen en het milieu.
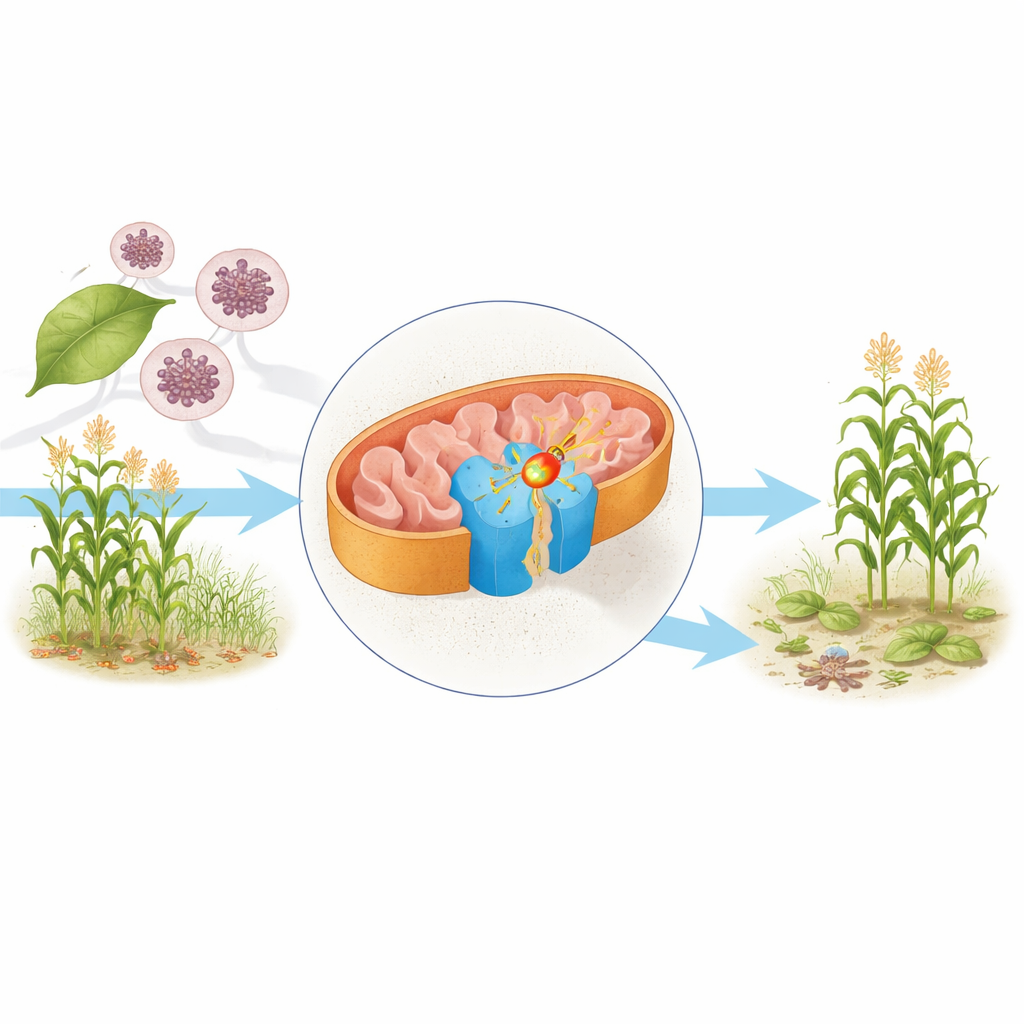
De celmotor onder de microscoop
In de mitochondriën—vaak de energiecentrales van de cel genoemd—worden voedingsmoleculen elektronen ontnomen die uiteindelijk helpen ATP te maken, de belangrijkste energiebron van de cel. Een centraal onderdeel van dit apparaat is complex II, ook bekend als succinaatdehydrogenase. Het koppelt de Krebs‑cyclus, die voedingsstoffen afbreekt, aan de ademhalingsketen, die die chemische afbraak omzet in bruikbare energie. De auteurs zuiverden complex II uit de gist Saccharomyces cerevisiae, een werkpaard in de biologie, en gebruikten cryo‑elektronenmicroscopie om de structuur bij bijna‑atomaire resolutie vast te stellen in twee vormen: één met het natuurlijke elektronen‑transportmolecuul ubiquinon en een andere gebonden aan het fungicide bixafen.
Een bekende motor met een verrassend ontbrekend onderdeel
Het gistenzym lijkt sterk op complex II uit zoogdieren en andere organismen, met twee grote hydrofiele subuniten die de chemie verzorgen en twee kleinere, in het membraan ingebedde subuniten die het complex in het mitochondriale membraan verankeren. Elektronen reizen van een flavinecofactor via een keten van ijzer‑zwavelclusters richting het membraan, waar ubiquinon ze normaal oppikt. De structuur onthult echter een grote verrassing: anders dan typische "type C" complex II‑enzymen, ontbreekt in de gistversie volledig een heemgroep—een ijzerhoudende cofactor die eerder als een universeel stabiliserend element van deze familie werd gezien. In plaats daarvan vertrouwt gist complex II op extra waterstofbruggen, meer hydrofobe residuen en een diep ingebedde fosfolipide om zijn membraansubuniten samen te lijmen en het complex zonder heem intact te houden.
Fungicide in de aanlegplaats
De kern van de studie is de zogenaamde Q‑plaats, het zakje waar ubiquinon normaal in neerstrijkt om elektronen te ontvangen. In de bixafen‑gebonden structuur is dit zakje gevuld met het fungicide, dat veel van ubiquinons interacties nabootst maar ook extra nauwe contacten maakt. Sleutelaminozuren uit drie subuniten omklemmen de remmer via een mix van polaire en hydrofobe interacties, terwijl een flexibele uitstulping van één membraansubunit (Sdh4) in de plaats vouwt en zich om de hydrofobe staart van bixafen wikkelt. Wanneer in plaats daarvan het natuurlijke substraat aanwezig is, raakt het uiterste puntje van deze Sdh4‑uitstulping gedesordend en maakt ruimte voor de langere keten van ubiquinon, wat laat zien dat het zakje zich op verschillende manieren kan aanpassen aan substraat en remmer.
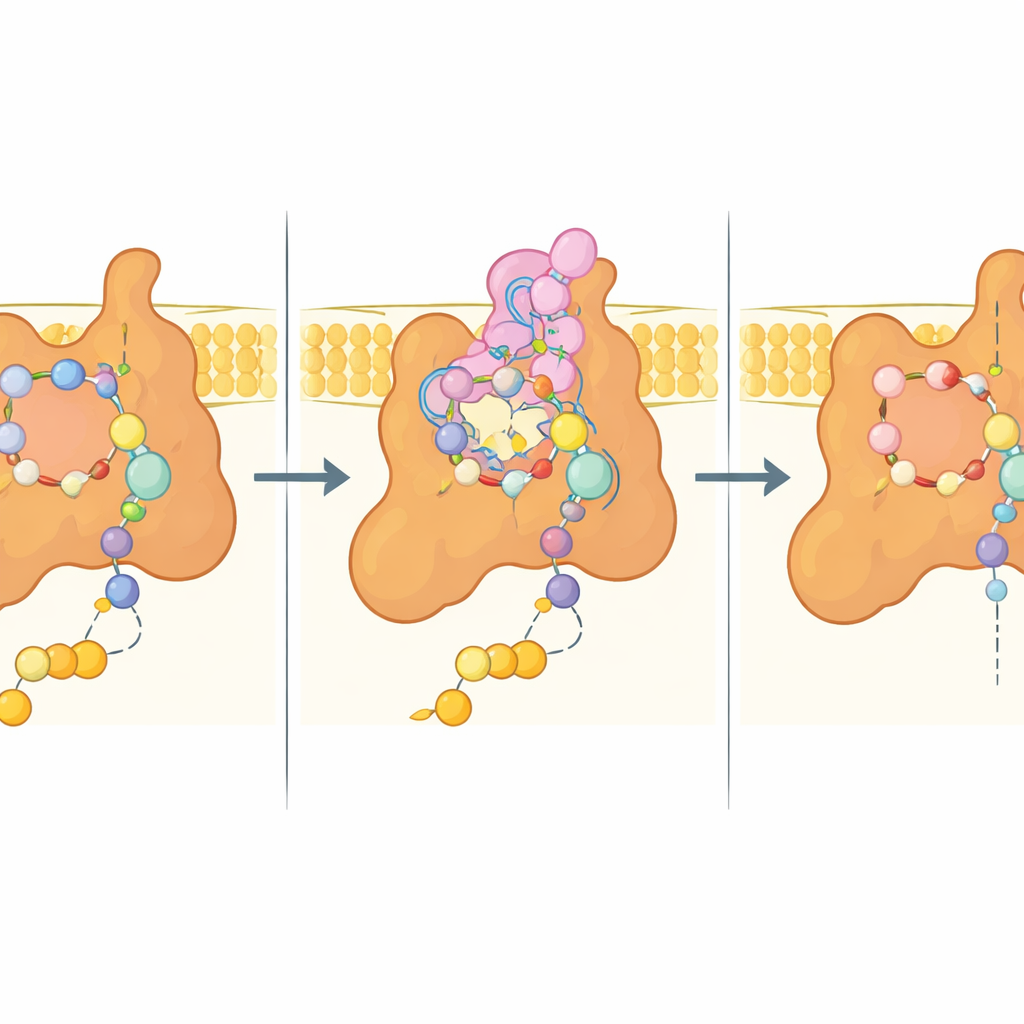
Aanwijzingen voor fungiciden van de volgende generatie
Aangezien veel agriculturieel belangrijke en door mensen ziekteverwekkende schimmels nauwe Sdh4‑sequenties delen, vooral in deze N‑terminale uitstulping, weerspiegelt de giststructuur waarschijnlijk hun complex II‑architectuur. De auteurs gebruikten hun experimentele model om verschillende commerciële succinaatdehydrogenase‑inhibitoren (SDHI) computergestuurd te docken, en onthulden een gemeenschappelijke bindingslogica: een carbamaat‑ of carboxamide"kern" die geconserveerde aminozuren aantrekt, plus variabele hydrofobe versieringen die in nabijgelegen pocketjes passen en de sterkte en specificiteit moduleren. Belangrijk is dat vrijwel alle residuen die bixafen in gist raken geconserveerd zijn in meerdere gewaspathogenen, wat suggereert dat subtiele sequentieverschillen kunnen verklaren waarom sommige soorten gevoeliger of minder gevoelig zijn—en waarom bepaalde mutaties in het veld resistentie verlenen.
Van structurele kaart naar praktische impact
Eenvoudig gezegd levert de studie een gedetailleerde blauwdruk van hoe een belangrijke klasse fungiciden zich in een schimmelenergie‑enzym wringt en het uitschakelt. Ze draait ook aannames om over een verondersteld universeel heemcomponent en toont hoe gist alternatieve stabiliserende kenmerken heeft geëvolueerd. Met deze structurele kaart kunnen onderzoekers bestaande fungiciden rationeel aanpassen of nieuwe ontwerpen die beter gebruikmaken van schimmelspecifieke kenmerken, de kans op resistentie verkleinen en ongerichte schade aan gewassen, wilde dieren en mensen minimaliseren. Bakkersgist, lang geliefd vanwege brood en bier, wordt zo een krachtig model voor het bouwen van de volgende generatie gerichte antischimmelmiddelen.
Bronvermelding: Pinotsis, N., Burn-Leefe, C., Jones, S. et al. Cryo-EM structure of bixafen-bound S. cerevisiae complex II unravels SDHI specificity against pathogenic fungi. Commun Biol 9, 517 (2026). https://doi.org/10.1038/s42003-026-09617-8
Trefwoorden: succinaatdehydrogenase, schimmelresistentie, kryo-elektronenmicroscopie, mitochondriale ademhaling, SDHI-fungiciden