Clear Sky Science · ja
ビキサフェン結合S. cerevisiae複合体IIのクライオEM構造が病原真菌に対するSDHI特異性を解き明かす
真菌の発電所を止めることが重要な理由
真菌性疾患は収穫、森林、さらには人々の健康を脅かしており、多くの現代的な殺菌剤は病原体のエネルギー供給を断つことで作用します。しかしこれまで、これらの化学物質がどのように真菌の標的に原子レベルで結合するかを詳しく観察した例はありませんでした。本論文は、出芽酵母の重要なエネルギー産生酵素の三次元構造を明らかにし、広く使われる殺菌剤ビキサフェンがこの分子機械をどのように妨害するかを正確に示します。この酵素は多くの病原真菌で類縁性が高いため、本研究は作物や医療の脅威に対して有効で、人や環境により安全なより賢い殺菌剤設計への道を開きます。
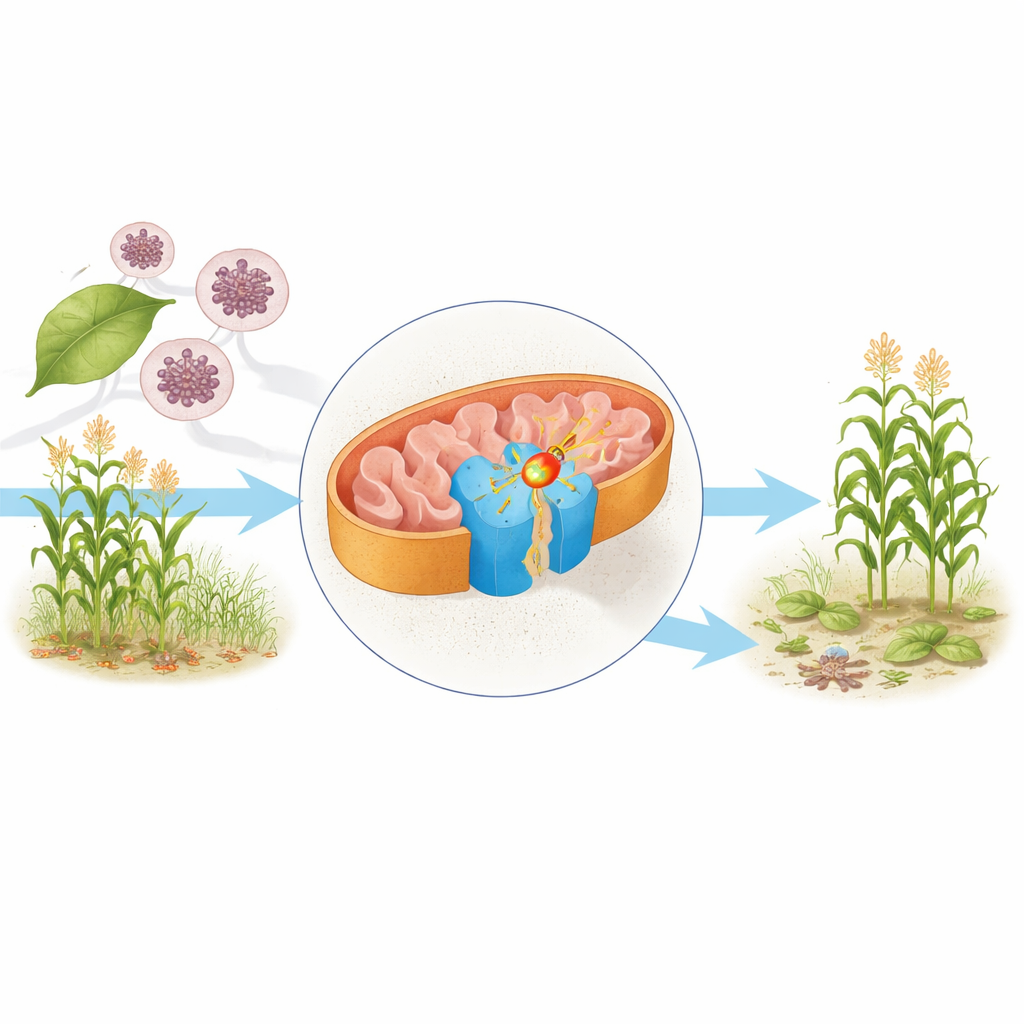
顕微鏡下の細胞エンジン
ミトコンドリアはしばしば細胞の発電所と呼ばれ、そこで食品分子は最終的にATP(細胞の主要な燃料)を作るのに使われる電子を奪われます。この機構の中心的要素の一つが複合体II、別名コハク酸デヒドロゲナーゼです。これは栄養素を分解するクレブス回路と、その化学的分解を利用可能なエネルギーに変換する呼吸鎖をつなぎます。著者らは生物学で広く用いられる働き馬である出芽酵母(Saccharomyces cerevisiae)から複合体IIを精製し、クライオ電子顕微鏡を用いて、天然の電子運搬分子であるユビキノンを含む状態と殺菌剤ビキサフェンが結合した状態の、ほぼ原子分解能の構造を決定しました。
なじみのあるエンジンにある驚きの欠落部位
酵母の酵素は、化学反応を担う大きな親水性サブユニット二つと、ミトコンドリア膜に複合体を固定する小さな膜内蔵サブユニット二つを備える点で、哺乳類や他の生物の複合体IIに非常によく似ています。電子はフラビン補因子から鉄–硫黄クラスターの鎖を通って膜へと移動し、通常はそこでユビキノンが電子を受け取ります。しかし構造は大きな驚きを示しました。典型的な「タイプC」複合体II酵素とは異なり、酵母版はヘム群を完全に欠いており、これまでこの族の普遍的で安定化に寄与する補因子と考えられていた鉄含有ヘムが存在しません。代わりに、酵母の複合体IIは余分な水素結合、より疎水性のアミノ酸残基、および深く埋め込まれたリン脂質を使って膜サブユニット同士を接着し、ヘムなしで複合体を安定化させています。
ドッキングベイにある殺菌剤
本研究の核心は、ユビキノンが通常ドッキングして電子を受け取るポケットであるいわゆるQサイトです。ビキサフェン結合構造では、このポケットが殺菌剤によって満たされており、ビキサフェンはユビキノンの多くの相互作用を模倣すると同時に、さらに密着した追加の接触を行っています。三つのサブユニット由来の重要なアミノ酸が極性および疎水性の相互作用を混在させて阻害剤を包み込み、膜サブユニットの一つ(Sdh4)からの柔軟な伸長部位がその場に折りたたまれてビキサフェンの疎水性尾部を取り巻きます。天然基質が存在する場合、このSdh4伸長部位の先端は秩序を失って位置を変え、より長い鎖をもつユビキノンのためのスペースを作ることが示され、ポケットが基質と阻害剤に応じて異なる形で適応できることを示しています。
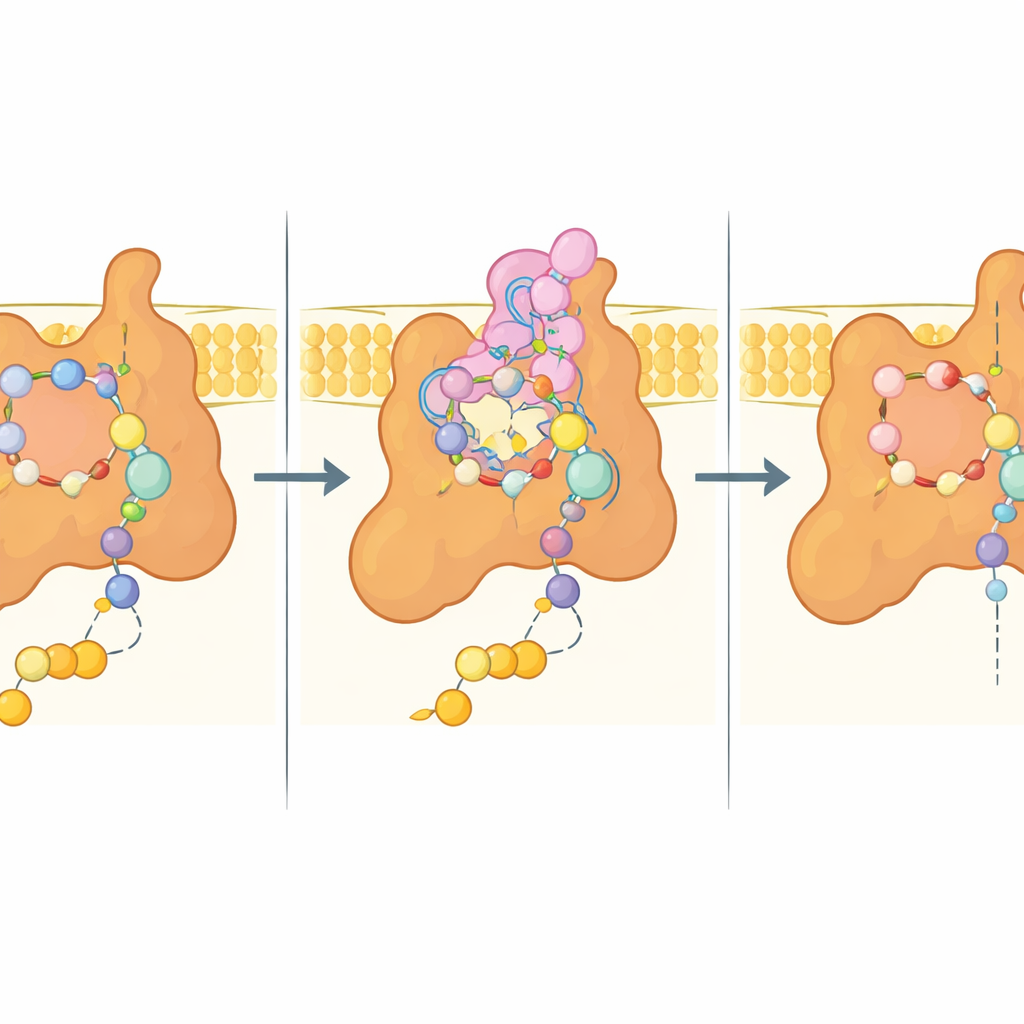
次世代殺菌剤への手がかり
多くの農業的に重要な真菌や人に病原性を示す真菌は、特にこのN末端伸長領域においてSdh4配列の類似性が高いため、酵母の構造はそれらの複合体IIの構造を反映している可能性が高いです。著者らは実験モデルを用いていくつかの市販のコハク酸デヒドロゲナーゼ阻害剤(SDHI)を計算的にドッキングし、共通の結合論理を明らかにしました:保存されたアミノ酸と相互作用するカルボキサアミドの「コア」と、近接ポケットに入って結合強度と特異性を調節する可変の疎水性修飾です。重要なのは、酵母でビキサフェンに接触する残基のほとんどが複数の作物病原体で保存されていることで、微妙な配列の違いが種ごとの感受性の差や、現場で見られる特定の突然変異による耐性の理由を説明し得ることを示唆しています。
構造地図から実用的インパクトへ
平易に言えば、本研究は主要な殺菌剤クラスが真菌のエネルギー酵素にどのように挟まり停止させるかの詳細な設計図を提供します。また、普遍的と考えられていたヘム成分に対する仮定を覆し、酵母が代替の安定化機構を進化させてきたことを示します。この構造地図をもとに、研究者は既存の殺菌剤を合理的に改良したり、真菌特有の特徴をより有効に利用して耐性の発生確率を減らし、作物や野生生物、人への非標的ダメージを最小限に抑える新薬を設計できるようになります。パンやビールで長く愛されてきた出芽酵母は、次世代の標的特異的な抗真菌戦略を構築するための強力なモデルとなります。
引用: Pinotsis, N., Burn-Leefe, C., Jones, S. et al. Cryo-EM structure of bixafen-bound S. cerevisiae complex II unravels SDHI specificity against pathogenic fungi. Commun Biol 9, 517 (2026). https://doi.org/10.1038/s42003-026-09617-8
キーワード: コハク酸デヒドロゲナーゼ, 殺菌剤耐性, クライオ電子顕微鏡法, ミトコンドリア呼吸, SDHI殺菌剤