Clear Sky Science · it
Struttura cryo-EM del complesso II di S. cerevisiae legato a bixafen svela la specificità degli SDHI contro i funghi patogeni
Perché bloccare le centrali energetiche fungine è importante
Le malattie fungine minacciano raccolti, foreste e persino le persone, e molti fungicidi moderni agiscono interrompendo la fornitura di energia del patogeno. Tuttavia, fino ad ora, nessuno aveva osservato in dettaglio atomico come queste molecole si leghino ai loro bersagli fungini. Questo studio rivela la struttura tridimensionale di un enzima cruciale per la produzione di energia del lievito da panificazione e mostra esattamente come un fungicida ampiamente usato, il bixafen, inceppi questa macchina molecolare. Poiché questo enzima è strettamente correlato in molti funghi patogeni, il lavoro apre la strada a progettare fungicidi più intelligenti, efficaci contro minacce agricole e mediche ma più sicuri per gli esseri umani e per l’ambiente.
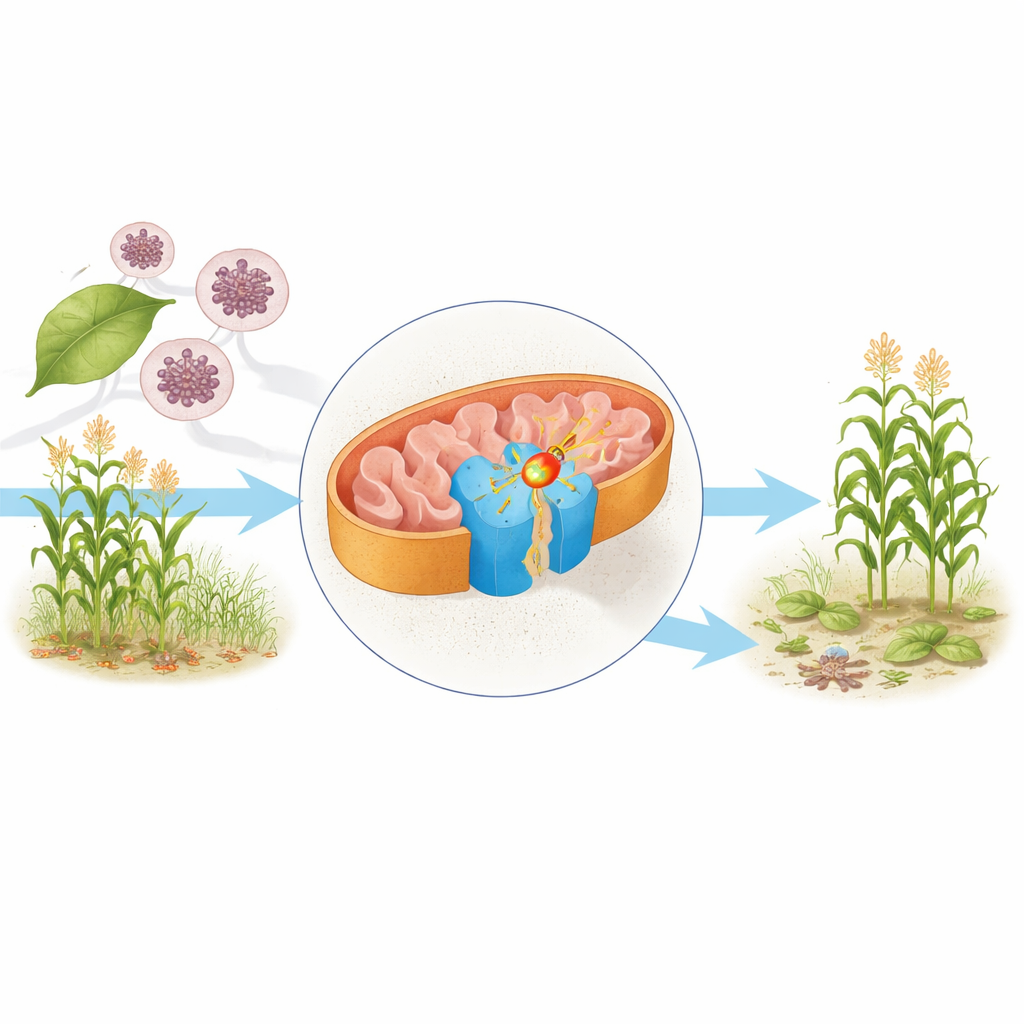
Il motore cellulare sotto il microscopio
All’interno dei mitocondri—spesso chiamati le centrali energetiche della cellula—le molecole nutritive perdono elettroni che finiscono per aiutare a produrre ATP, il carburante principale della cellula. Uno dei componenti centrali di questo apparato è il complesso II, noto anche come succinato deidrogenasi. Collega il ciclo di Krebs, che scompone i nutrienti, alla catena respiratoria, che converte quella scomposizione chimica in energia utilizzabile. Gli autori hanno purificato il complesso II da Saccharomyces cerevisiae, un organismo di riferimento in biologia, e hanno usato la crio-microscopia elettronica per determinarne la struttura a risoluzione quasi atomica in due forme: una con la sua molecola trasportatrice di elettroni naturale, l’ubiquinone, e l’altra legata al fungicida bixafen.
Un motore familiare con una sorprendente assenza
L’enzima del lievito somiglia molto al complesso II dei mammiferi e di altri organismi, con due grandi subunità idrofile che gestiscono la chimica e due subunità più piccole inserite nella membrana che ancorano il complesso nella membrana mitocondriale. Gli elettroni viaggiano da un cofattore flavinico attraverso una catena di cluster ferro-zolfo verso la membrana, dove l’ubiquinone normalmente li riceve. Tuttavia, la struttura rivela una sorpresa importante: a differenza dei tipici enzimi del complesso II di “tipo C”, la versione del lievito è completamente priva di un gruppo eme—un cofattore contenente ferro ritenuto in precedenza una caratteristica universale e stabilizzante di questa famiglia. Invece, il complesso II del lievito si affida a legami idrogeno supplementari, residui più idrofobici e a un fosfolipide profondamente sepolto per unire le sue subunità di membrana e mantenere il complesso integro senza l’eme.
Il fungicida nella baia di attracco
Al centro dello studio c’è il cosiddetto sito Q, la tasca dove l’ubiquinone normalmente si posiziona per ricevere gli elettroni. Nella struttura legata a bixafen questa tasca è occupata dal fungicida, che imita molte delle interazioni dell’ubiquinone ma stabilisce anche contatti aggiuntivi e stretti. Aminoacidi chiave di tre subunità cullano l’inibitore tramite una combinazione di interazioni polari e idrofobiche, mentre un’estensione flessibile di una subunità di membrana (Sdh4) si ripiega nel sito e avvolge la coda idrofobica del bixafen. Quando è presente il substrato naturale, la punta di questa estensione di Sdh4 diventa disordinata per fare spazio alla catena più lunga dell’ubiquinone, mostrando che la tasca può adattarsi in modo diverso a substrato e inibitore.
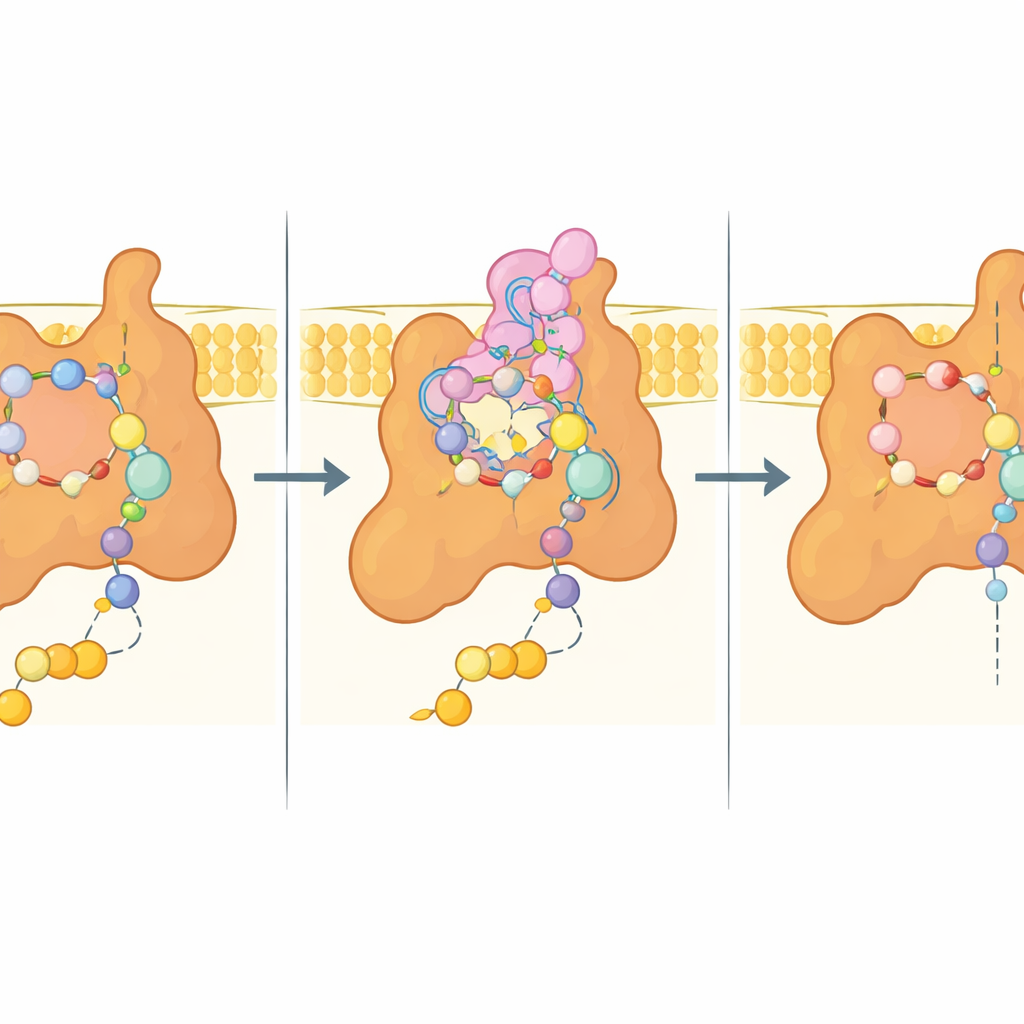
Indizi per i fungicidi di nuova generazione
Poiché molti funghi di rilevanza agricola e patogeni per l’uomo condividono sequenze di Sdh4 strettamente correlate, in particolare in questa estensione N-terminale, la struttura del lievito probabilmente rispecchia l’architettura del loro complesso II. Gli autori hanno utilizzato il loro modello sperimentale per posizionare computazionalmente diversi fungicidi commerciali inibitori della succinato deidrogenasi (SDHI), rivelando una logica di legame comune: un “core” carbossammidico che interagisce con aminoacidi conservati, più decorazioni idrofobiche variabili che si inseriscono in tasche vicine e modulano potenza e specificità. È importante notare che quasi tutti i residui che contattano il bixafen nel lievito sono conservati in diversi patogeni delle colture, suggerendo che differenze di sequenza sottili potrebbero spiegare perché alcune specie sono più o meno sensibili—e perché certe mutazioni conferiscono resistenza in campo.
Dalla mappa strutturale all’impatto pratico
In termini semplici, lo studio fornisce una mappa dettagliata di come una grande classe di fungicidi si incunea in un enzima energetico fungino e lo spegne. Smentisce inoltre assunzioni su un presunto componente eme universale e mostra come il lievito abbia evoluto caratteristiche stabilizzanti alternative. Con questa mappa strutturale, i ricercatori possono ora modificare razionalmente i fungicidi esistenti o inventarne di nuovi che sfruttino meglio le caratteristiche specifiche dei funghi, riducano le probabilità di resistenza e minimizzino i danni fuori bersaglio a colture, fauna e persone. Il lievito da panificazione, a lungo amato per pane e birra, diventa così un potente modello per costruire la prossima generazione di armi antifungine mirate.
Citazione: Pinotsis, N., Burn-Leefe, C., Jones, S. et al. Cryo-EM structure of bixafen-bound S. cerevisiae complex II unravels SDHI specificity against pathogenic fungi. Commun Biol 9, 517 (2026). https://doi.org/10.1038/s42003-026-09617-8
Parole chiave: succinato deidrogenasi, resistenza ai fungicidi, crio microscopia elettronica, respirazione mitocondriale, fungicidi SDHI