Clear Sky Science · ru
Крио-ЭМ структура комплекса II S. cerevisiae, связанного с бисафеном, раскрывает специфичность SDHI против патогенных грибов
Почему важно блокировать «электростанции» грибов
Грибковые болезни угрожают урожаям, лесам и даже людям, и многие современные фунгициды действуют, отсекая у патогена источник энергии. До сих пор никто не видел в атомных подробностях, как эти вещества закрепляются на грибковых мишенях. В этой работе показана трёхмерная структура ключевого фермента выработки энергии из дрожжей хлебопекарных и точно продемонстрировано, как широко используемый фунгицид бисафен заклинивает этот молекулярный механизм. Поскольку этот фермент тесно связан у многих патогенных грибов, результаты открывают путь к разработке более умных фунгицидов, эффективных против сельскохозяйственных и медицинских угроз, но более безопасных для людей и окружающей среды.
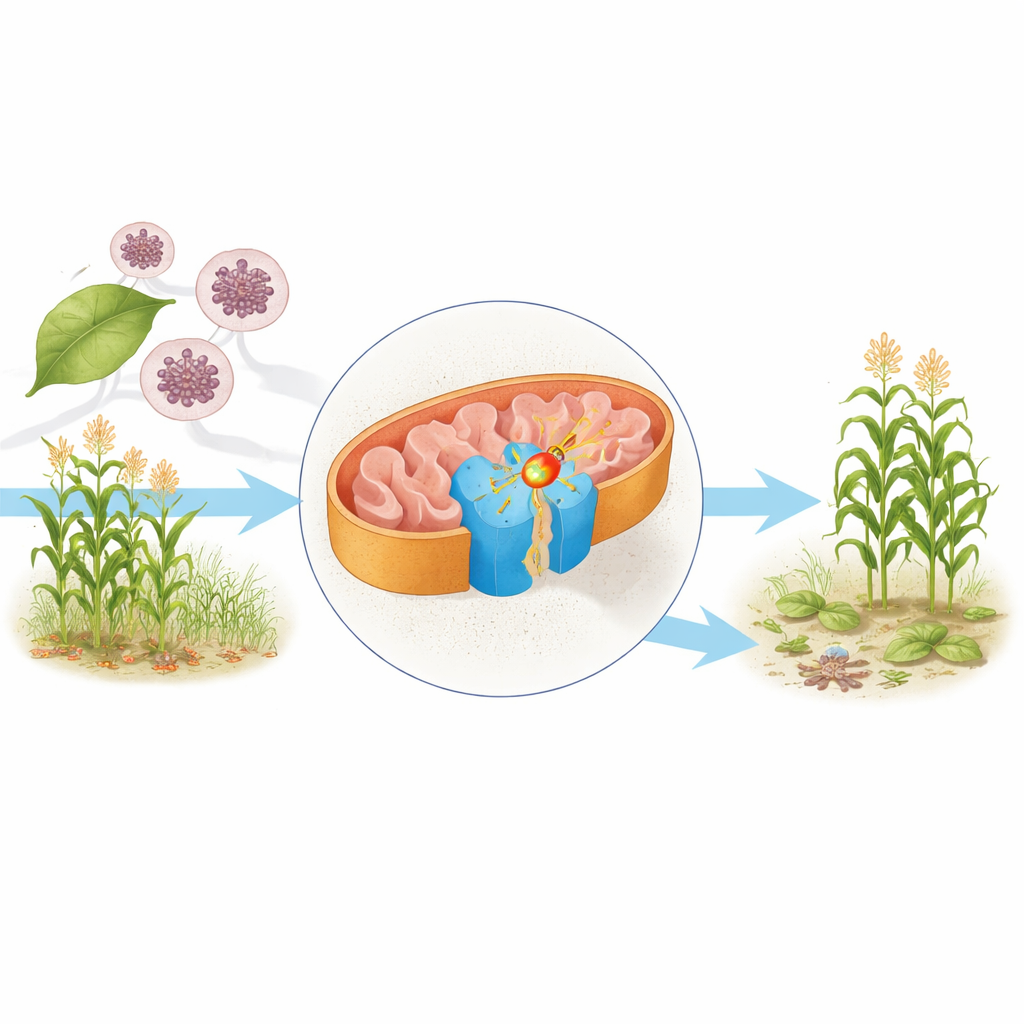
Клеточный двигатель под микроскопом
Внутри митохондрий — часто называемых «электростанциями» клетки — молекулы пищи теряют электроны, которые в конце концов помогают синтезировать ATP, главный энергетический носитель клетки. Одним из центральных компонентов этого аппарата является комплекс II, также известный как сукцинатдегидрогеназа. Он связывает цикл Кребса, расщепляющий питательные вещества, с дыхательной цепью, превращающей это химическое окисление в доступную энергию. Авторы очистили комплекс II из дрожжей Saccharomyces cerevisiae, широко используемого модельного организма, и с помощью криоэлектронной микроскопии определили его структуру с почти атомным разрешением в двух состояниях: одно несёт свой естественный переносчик электронов убихинон, другое связано с фунгицидом бисафеном.
Знакомый двигатель с неожиданной недостающей деталью
Фермент дрожжей близко похож на комплекс II у млекопитающих и других организмов: две большие гидрофильные субъединицы выполняют каталитическую работу, а две меньшие, интегрированные в мембрану, закрепляют комплекс в митохондриальной мембране. Электроны переходят от флавинового кофактора через цепочку железо‑сульфидных кластеров к мембране, где обычно их принимает убихинон. Однако структура выявляет важный сюрприз: в отличие от типичных ферментов «типа C», дрожжевой вариант полностью лишён гемовой группы — содержащего железо кофактора, который ранее считали универсальной стабилизирующей чертой этого семейства. Вместо гема комплекс II дрожжей опирается на дополнительные водородные связи, более гидрофобные остатки и глубоко погружённый фосфолипид, которые «склеивают» его мембранные субъединицы и поддерживают целостность без гема.
Фунгицид в докинговой камере
В центре исследования находится так называемый Q‑сайт — карман, куда обычно садится убихинон, чтобы принять электроны. В структуре, связанной с бисафеном, этот карман заполнен фунгицидом: он имитирует многие взаимодействия убихинона, но также образует дополнительные плотные контакты. Ключевые аминокислоты из трёх субъединиц охватывают ингибитор смесью полярных и гидрофобных взаимодействий, тогда как гибкое удлинение одной мембранной субъединицы (Sdh4) сворачивается в сайт и обвивает гидрофобный хвост бисафена. Когда в кармане присутствует естественный субстрат, кончик этого удлинения Sdh4 теряет упорядоченность и освобождает место для более длинной цепи убихинона, что показывает способность кармана адаптироваться к различным субстратам и ингибиторам.
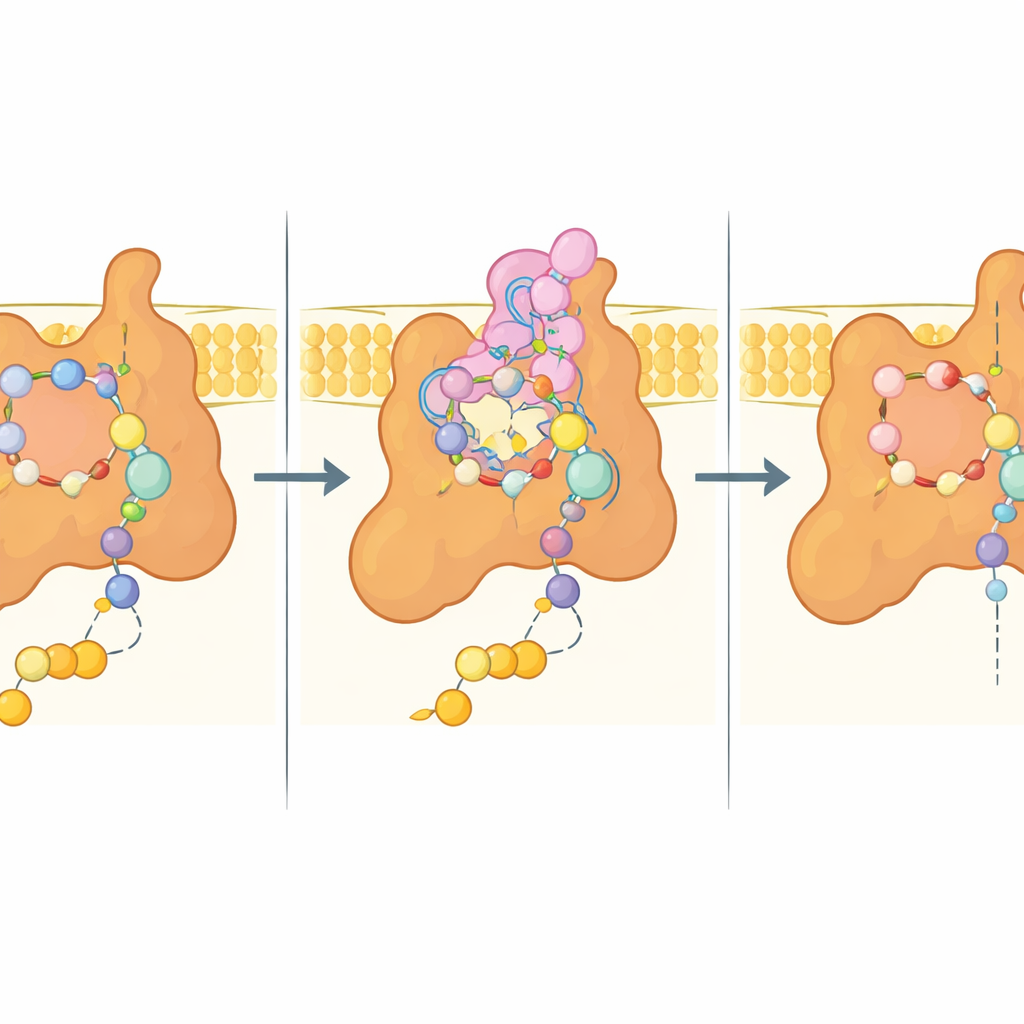
Подсказки для фунгицидов следующего поколения
Поскольку у многих сельскохозяйственно значимых и патогенных для человека грибов последовательности Sdh4 схожи, особенно в этой N‑концевой вставке, структура дрожжей, вероятно, отражает архитектуру их комплекса II. Авторы использовали экспериментальную модель для вычислительного докинга ряда коммерческих ингибиторов сукцинатдегидрогеназы (SDHI), выявив общую логику связывания: карбоксамидное «ядро», взаимодействующее с консервативными аминокислотами, и вариативные гидрофобные «декорации», которые заполняют соседние карманы и модулируют силу и специфичность. Важно, что почти все остатки, контактирующие с бисафеном в дрожжах, консервативны у множества патогенов растений, что указывает на то, что тонкие различия в последовательностях могут объяснять, почему одни виды более чувствительны, а другие — менее, и почему определённые мутации дают устойчивость в полевых условиях.
От структурной карты к практическому эффекту
Проще говоря, исследование даёт детализированный план того, как крупный класс фунгицидов врезается в фермент энергетического обмена грибов и блокирует его работу. Оно также опровергает предположение о якобы универсальном компоненте‑геме и показывает, как дрожжи эволюционировали альтернативные стабилизирующие элементы. Имея эту структурную карту, исследователи теперь могут рационально модифицировать существующие фунгициды или создавать новые, лучше использующие грибоспецифические особенности, уменьшающие риск развития устойчивости и минимизирующие побочные эффекты для сельхозкультур, дикой природы и людей. Хлебопекарные дрожжи, долгое время любимые за хлеб и пиво, таким образом становятся мощной моделью для создания следующего поколения целевых противогрибковых средств.
Цитирование: Pinotsis, N., Burn-Leefe, C., Jones, S. et al. Cryo-EM structure of bixafen-bound S. cerevisiae complex II unravels SDHI specificity against pathogenic fungi. Commun Biol 9, 517 (2026). https://doi.org/10.1038/s42003-026-09617-8
Ключевые слова: сукцинатдегидрогеназа, устойчивость к фунгицидам, криоэлектронная микроскопия, митохондриальное дыхание, фунгициды класса SDHI