Clear Sky Science · pt
Estrutura por crio‑EM do complexo II de S. cerevisiae ligado à bixafen revela a especificidade dos SDHIs contra fungos patogênicos
Por que bloquear as usinas de energia dos fungos importa
Doenças fúngicas ameaçam colheitas, florestas e até pessoas, e muitos fungicidas modernos atuam cortando o suprimento de energia do patógeno. No entanto, até agora ninguém havia observado em detalhe atômico como esses compostos se prendem aos seus alvos fúngicos. Este artigo revela a estrutura tridimensional de uma enzima crucial na produção de energia da levedura de padaria e mostra exatamente como um fungicida amplamente usado, a bixafen, trava essa máquina molecular. Como essa enzima é intimamente relacionada em muitos fungos patogênicos, o trabalho abre caminho para projetar fungicidas mais inteligentes — potentes contra ameaças agrícolas e médicas, porém mais seguros para humanos e para o meio ambiente.
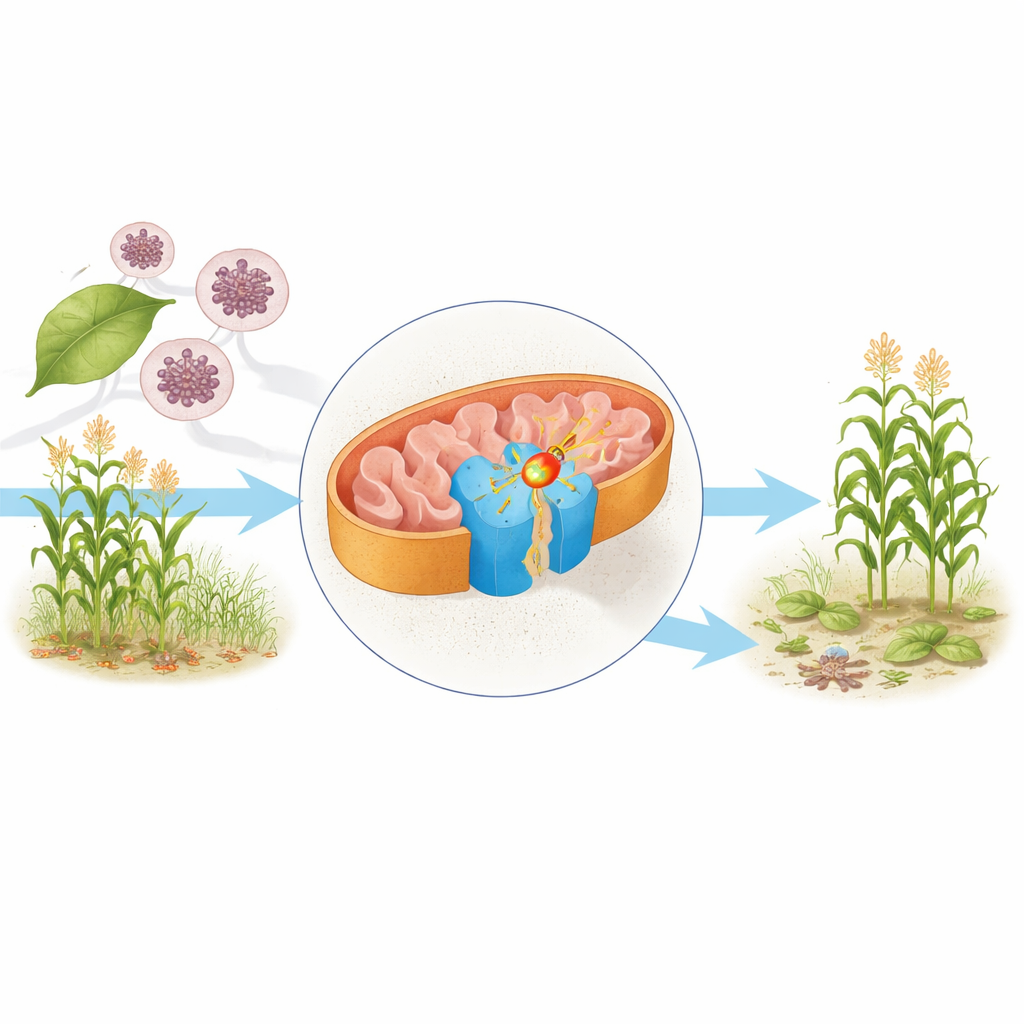
O motor celular sob o microscópio
Dentro das mitocôndrias — frequentemente chamadas de usinas de energia da célula — moléculas alimentares têm elétrons removidos que, em última instância, ajudam a produzir ATP, o combustível principal da célula. Um componente central dessa maquinaria é o complexo II, também conhecido como succinato desidrogenase. Ele conecta o ciclo de Krebs, que quebra nutrientes, à cadeia respiratória, que converte essa degradação química em energia utilizável. Os autores purificaram o complexo II da levedura Saccharomyces cerevisiae, um organismo‑modelo na biologia, e usaram crio‑microscopia eletrônica para determinar sua estrutura em resolução quase atômica em duas formas: uma carregando sua molécula natural transportadora de elétrons, a ubiquinona, e outra ligada ao fungicida bixafen.
Um motor familiar com uma peça surpreendentemente ausente
A enzima da levedura assemelha‑se fortemente ao complexo II de mamíferos e outros organismos, com duas grandes subunidades hidrofílicas responsáveis pela química e duas subunidades menores embebidas na membrana ancorando o complexo na membrana mitocondrial. Elétrons viajam de um cofator flavínico através de uma cadeia de clusters ferro‑enxofre em direção à membrana, onde a ubiquinona normalmente os captura. Entretanto, a estrutura revela uma surpresa importante: ao contrário dos típicos complexos II do “tipo C”, a versão da levedura carece completamente de um grupo heme — um cofator contendo ferro anteriormente considerado uma característica estabilizadora universal dessa família. Em vez disso, o complexo II da levedura depende de ligações de hidrogênio adicionais, resíduos mais hidrofóbicos e de um fosfolipídio profundamente enterrado para unir suas subunidades de membrana e manter o complexo íntegro sem o heme.
O fungicida na baía de acoplagem
No cerne do estudo está o chamado sítio Q, o bolso onde a ubiquinona normalmente se acomoda para receber elétrons. Na estrutura ligada à bixafen, esse bolso está ocupado pelo fungicida, que imita muitas das interações da ubiquinona, mas também estabelece contatos adicionais e mais apertados. Aminoácidos-chave de três subunidades envolvem o inibidor por uma mistura de interações polares e hidrofóbicas, enquanto uma extensão flexível de uma subunidade de membrana (Sdh4) se dobra no sítio e envolve a cauda hidrofóbica da bixafen. Quando o substrato natural está presente, a ponta dessa extensão de Sdh4 torna‑se desordenada e libera espaço para a cadeia mais longa da ubiquinona, mostrando que o bolso pode se adaptar de maneiras diferentes ao substrato e ao inibidor.
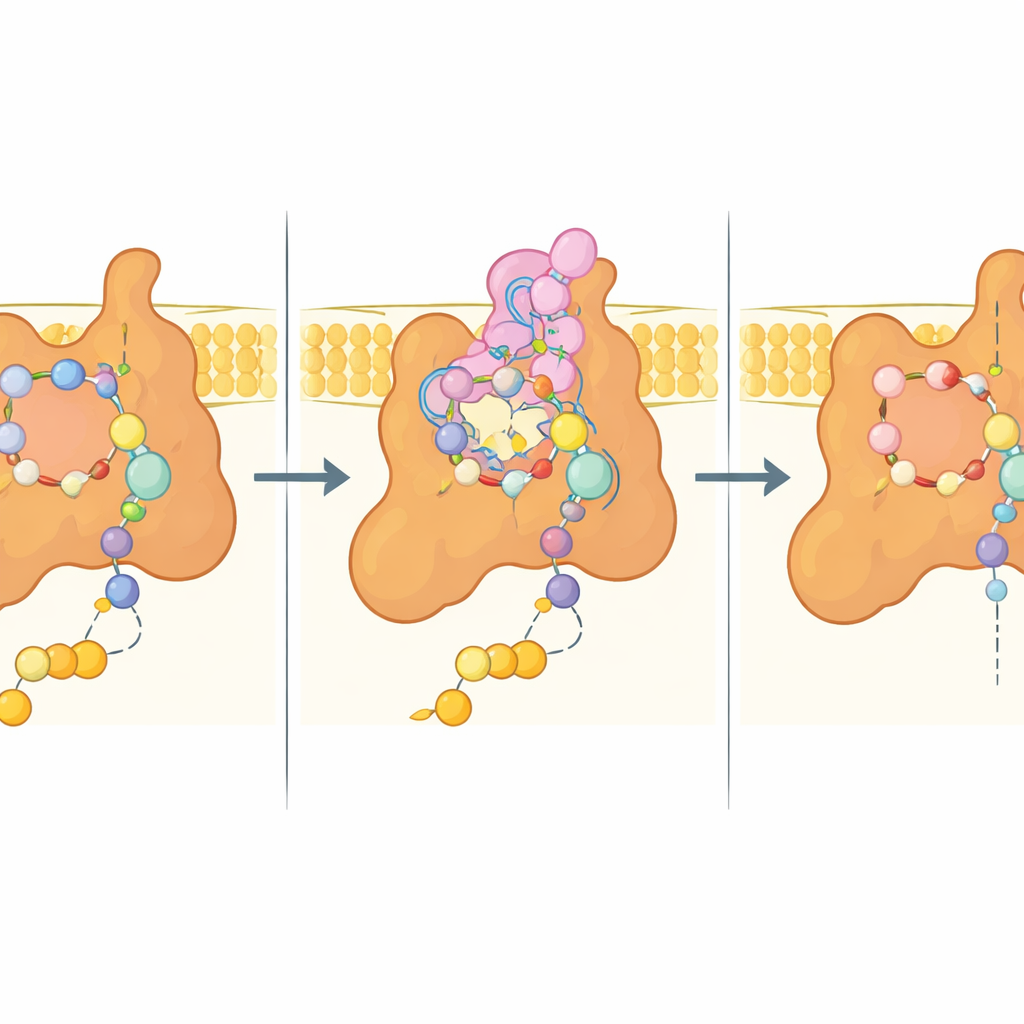
Pistas para fungicidas de próxima geração
Como muitos fungos de importância agrícola e patogênicos para humanos compartilham sequências de Sdh4 intimamente relacionadas, especialmente nessa extensão N‑terminal, a estrutura da levedura provavelmente reflete a arquitetura do complexo II deles. Os autores usaram seu modelo experimental para encaixar computacionalmente vários fungicidas comerciais inibidores da succinato desidrogenase (SDHIs), revelando uma lógica comum de ligação: um “núcleo” carboxamida que interage com aminoácidos conservados, além de decorações hidrofóbicas variáveis que se ajustam a bolsões próximos e modulam afinidade e especificidade. Importante: quase todos os resíduos que contatam a bixafen na levedura são conservados em diversos patógenos de culturas, sugerindo que diferenças sutis na sequência podem explicar por que algumas espécies são mais ou menos sensíveis — e por que certas mutações conferem resistência no campo.
Do mapa estrutural ao impacto prático
De forma direta, o estudo fornece um plano detalhado de como uma classe importante de fungicidas se encaixa em uma enzima energética fúngica e a desliga. Também derruba suposições sobre um suposto componente heme universal e mostra como a levedura evoluiu características estabilizadoras alternativas. Com esse mapa estrutural, pesquisadores podem agora ajustar racionalmente fungicidas existentes ou inventar novos que explorem melhor características específicas de fungos, reduzam as chances de resistência e minimizem danos fora do alvo a plantações, vida selvagem e pessoas. A levedura de padaria, há muito querida para pão e cerveja, torna‑se assim um modelo poderoso para construir a próxima geração de armas antifúngicas dirigidas.
Citação: Pinotsis, N., Burn-Leefe, C., Jones, S. et al. Cryo-EM structure of bixafen-bound S. cerevisiae complex II unravels SDHI specificity against pathogenic fungi. Commun Biol 9, 517 (2026). https://doi.org/10.1038/s42003-026-09617-8
Palavras-chave: succinato desidrogenase, resistência a fungicidas, crio microscopia eletrônica, respiração mitocondrial, fungicidas SDHI