Clear Sky Science · sv
Cryo-EM-struktur av bixafen-bundet S. cerevisiae komplex II avslöjar SDHI-specificitet mot patogena svampar
Varför det spelar roll att blockera svampars kraftverk
Svampsjukdomar hotar skördar, skogar och även människor, och många moderna fungicider fungerar genom att skära av patogenens energiförsörjning. Ändå hade ingen tidigare sett i atomär detalj hur dessa kemikalier fäster vid sina svamptargets. Denna artikel avslöjar tredimensionell struktur av ett centralt energiproducerande enzym från jäst (bagerijäst) och visar exakt hur ett ofta använt fungicid, bixafen, sätter igen denna molekylära maskin. Eftersom detta enzym är nära besläktat i många patogena svampar öppnar arbetet möjligheter att designa smartare fungicider som är potenta mot jordbruks- och medicinska hot men säkrare för människor och miljö.
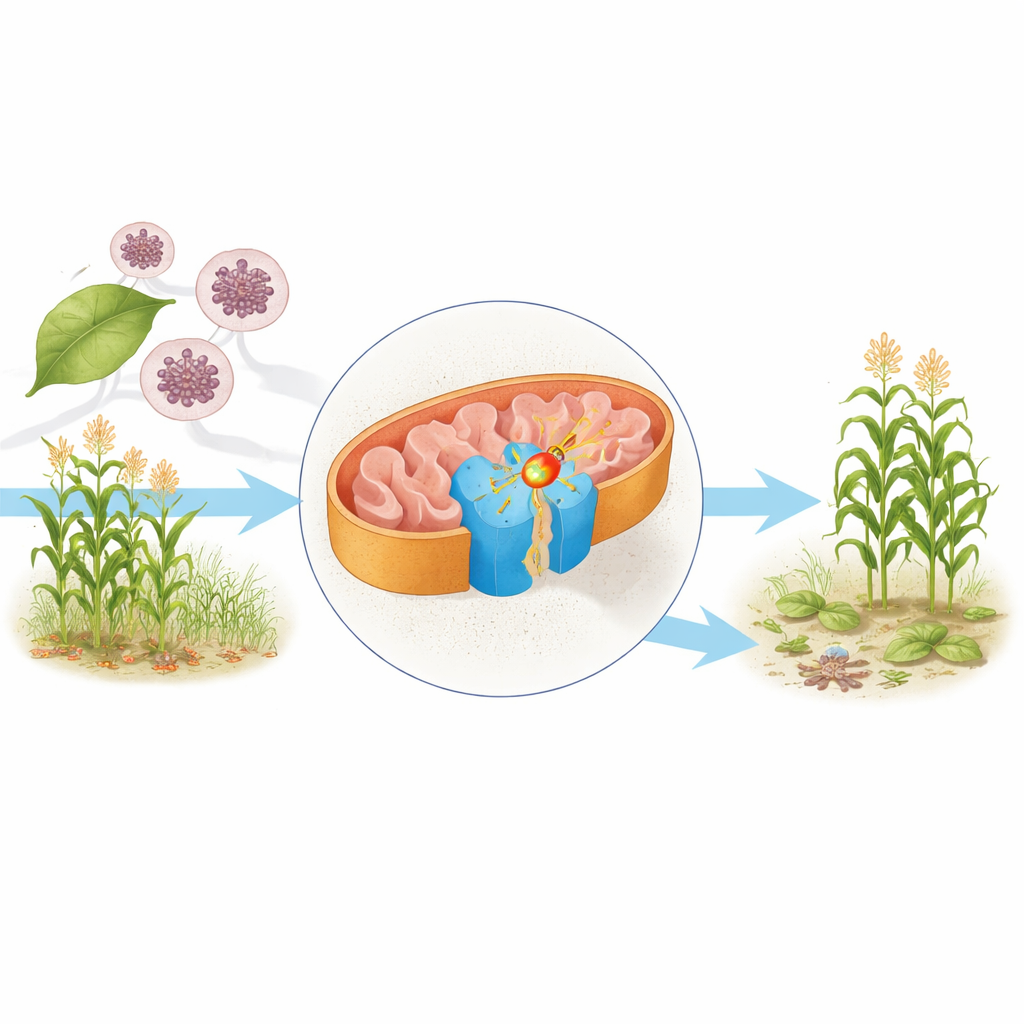
Cellmotorn under mikroskopet
Inuti mitokondrierna—ofta kallade cellens kraftverk—avlägsnas elektroner från näringsmolekyler som i slutändan hjälper till att bilda ATP, cellens viktigaste bränsle. En central komponent i detta maskineri är komplex II, också känt som succinatdehydrogenas. Det länkar citronsyracykeln, som bryter ner näringsämnen, till respirationskedjan, som omvandlar den kemiska nedbrytningen till användbar energi. Författarna renade komplex II från jästen Saccharomyces cerevisiae, en arbetsmyra i biologin, och använde kryo-elektronmikroskopi för att bestämma dess struktur i nära atomupplösning i två former: en med sitt naturliga elektronbärande molekyl, ubikinon, och en annan bunden till fungicidet bixafen.
En bekant motor med en överraskande saknad del
Jästenzymet liknar starkt komplex II från däggdjur och andra organismer, med två stora vattenälskande subenheter som sköter kemin och två mindre membranbundna subenheter som förankrar komplexet i mitokondriemembranet. Elektroner färdas från en flavin‑cofaktor genom en kedja av järn–svavel‑kluster mot membranet, där ubikinon normalt tar emot dem. Strukturen avslöjar dock en stor överraskning: till skillnad från typiska "typ C" komplex II‑enzymer saknar jästversionen helt ett hemgrupp—en järnhaltig cofaktor som tidigare antagits vara ett universellt stabiliserande inslag i denna familj. Istället förlitar sig jästkomplex II på extra vätebindningar, fler hydrofoba rester och ett djupt begravt fosfolipid för att hålla ihop sina membransubenheter och bibehålla komplexet utan hem.
Fungicid i dockningsfacket
I hjärtat av studien ligger så kallade Q‑siten, fickan där ubikinon normalt dockar för att ta emot elektroner. I strukturen med bixafen är denna ficka fylld av fungicidet, som imiterar många av ubikinons interaktioner men också gör ytterligare täta kontakter. Nyckelaminosyror från tre subenheter omfamnar hämmaren genom en blandning av polära och hydrofoba interaktioner, medan en flexibel förlängning från en membransubenhet (Sdh4) viker sig in i sittet och sveper runt bixafens hydrofoba svans. När den naturliga substratet istället är närvarande blir just spetsen av denna Sdh4‑förlängning oordnad och ger plats åt ubikinons längre kedja, vilket visar att fickan kan anpassa sig på olika sätt till substrat och inhibitor.
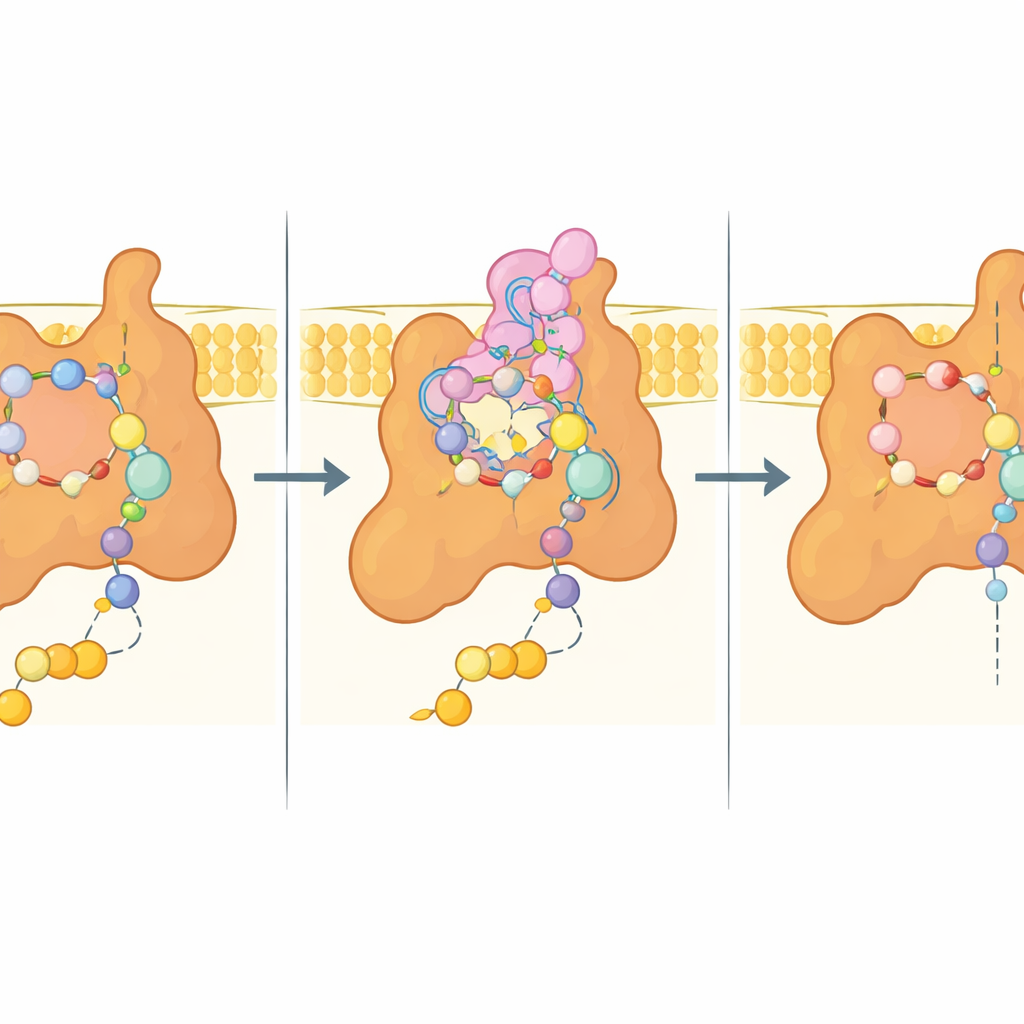
Ledtrådar för nästa generations fungicider
Eftersom många jordbruks‑ och mänskliga patogena svampar har nära besläktade Sdh4‑sekvenser, särskilt i denna N‑terminala förlängning, speglar sannolikt jäststrukturen deras komplex II‑arkitektur. Författarna använde sin experimentella modell för att datorsimulera dockning av flera kommersiella succinatdehydrogenas‑hämmare (SDHI), vilket avslöjar en gemensam bindningslogik: en karboxamid "kärna" som engagerar konserverade aminosyror, plus varierande hydrofoba dekorationer som passar in i närliggande fickor och påverkar styrka och specificitet. Viktigt är att nästan alla rester som kontaktar bixafen i jäst är bevarade i flera växtpatogener, vilket tyder på att subtila sekvensskillnader kan förklara varför vissa arter är mer eller mindre känsliga—och varför vissa mutationer ger upphov till resistens i fältet.
Från strukturkarta till praktisk påverkan
För att uttrycka det enkelt ger studien en detaljerad ritning av hur en stor klass fungicider kilas in i ett svampars energienzym och stänger ner det. Den kullkastar också antaganden om en föreslagen universell hemkomponent och visar hur jäst har utvecklat alternativa stabiliserande drag. Med denna strukturkarta kan forskare nu rationellt justera befintliga fungicider eller uppfinna nya som utnyttjar svampspecifika egenskaper bättre, minskar risken för resistens och begränsar icke‑målade skador på grödor, djurliv och människor. Bagerijästen, länge älskad för bröd och öl, blir därmed en kraftfull modell för att bygga nästa generations riktade svampbekämpningsmedel.
Citering: Pinotsis, N., Burn-Leefe, C., Jones, S. et al. Cryo-EM structure of bixafen-bound S. cerevisiae complex II unravels SDHI specificity against pathogenic fungi. Commun Biol 9, 517 (2026). https://doi.org/10.1038/s42003-026-09617-8
Nyckelord: succinatdehydrogenas, svampmedelsresistens, kryoelektronmikroskopi, mitokondriell respiration, SDHI-fungicider