Clear Sky Science · zh
N-丙基磺酰基吲哚连接的肼羰基硫酰胺的合成、生物学评价及分子对接研究,作为选择性ecto-5′-核苷酸酶和NTPD酶抑制剂
这项研究对未来癌症治疗为何重要
我们的免疫系统不断巡逻以发现癌细胞,但肿瘤已经进化出巧妙的手段来关闭这些防御。其中一种手段利用由ATP产生的化学信使——这正是为细胞提供能量的分子。本文描述了一类新型小分子,旨在打断这种化学伎俩,长期目标是帮助免疫系统更好地识别并攻击肿瘤。
使免疫细胞沉默的化学开关
细胞通过多种信号相互交流,其中一个重要通道基于核苷酸,如ATP及其分解产物腺苷。细胞外膜上有一系列酶持续将ATP转化为腺苷。两个关键蛋白,称为CD39和CD73,常在缺氧的肿瘤组织中过度表达。在那里,它们将受损或死亡细胞释放的ATP迅速转化为腺苷,腺苷对邻近免疫细胞起到类似化学“镇静剂”的作用。高水平的腺苷抑制T细胞活性、促进血管生成并助长肿瘤扩散。因此,阻断产生腺苷的酶成为现代癌症免疫治疗中的有吸引力策略。
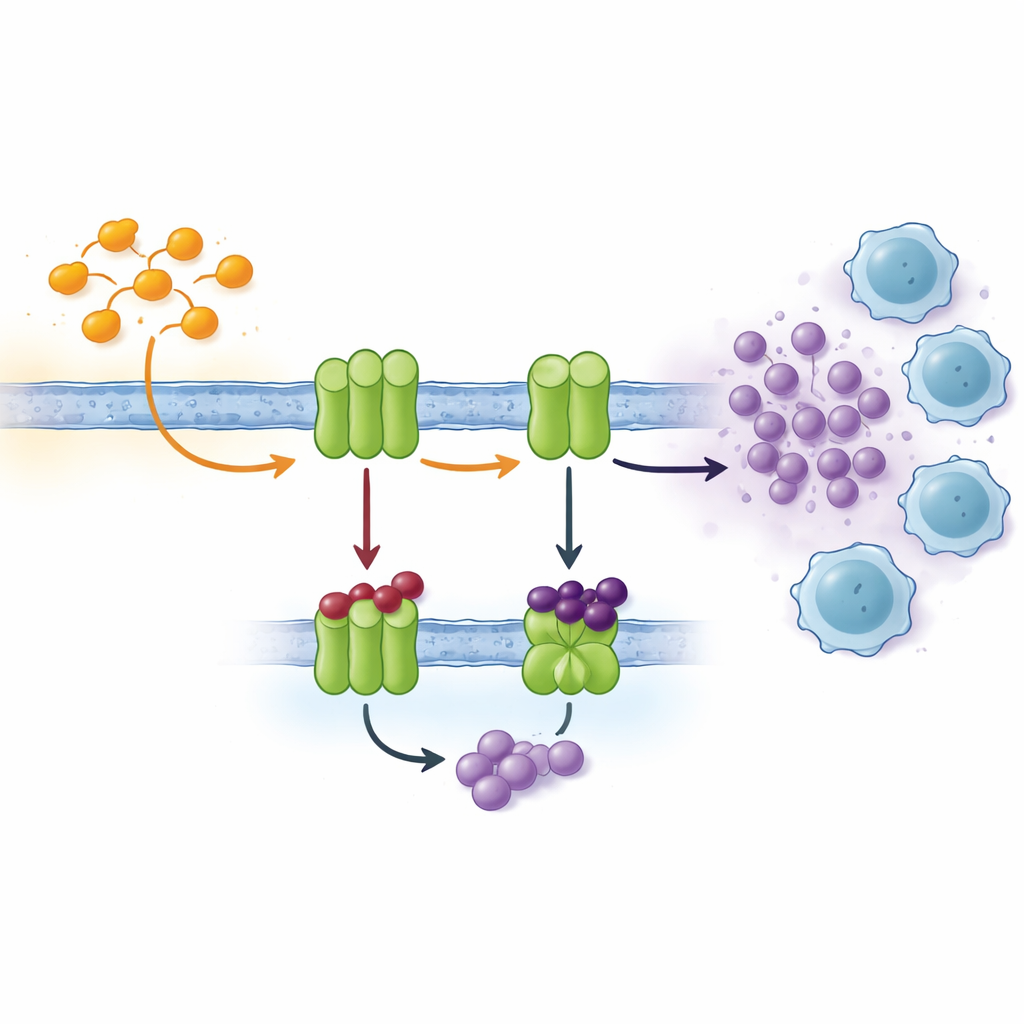
利用已证实的环状骨架设计更聪明的阻断剂
药物设计者常从已被证明具有医学价值的环状骨架出发。吲哚环是若干获批抗癌药中常见的一种结构。另一个有用的片段是硫代半胱腙,它能配位金属并与多种生物靶点强相互作用。在本研究中,研究者将这两种基元结合为单一混合骨架,并通过连接不同的化学基团进行微调,构建了包含22种相关化合物的小型库。他们改变了硫代半胱腙单元在吲哚环上的连接位置,并变换侧基,以观察这些变化如何影响对CD73及若干相关NTPD酶的抑制能力。
测试哪些分子作用于哪些酶
团队首先使用红外和核磁共振光谱、质谱和高效液相色谱等标准实验室技术确认了所有新分子的结构与纯度。随后在体外测定了每种化合物对五种人源酶的抑制能力:CD73和四种NTPD酶(1、2、3和8)。该系列中的若干化合物在低微摩尔浓度下即能抑制其靶标,效力远高于常用参比抑制剂。不同的化学修饰使每个化合物对特定酶型有偏好。例如,标为5f的分子对NTPDase2和NTPDase8尤为有效,而5i更偏好NTPDase1。两种相关分子5n和5o在对CD73及选定NTPD酶的强效作用上表现突出,将它们标记为尤其有前景的先导候选物。
在计算机上窥探结合口袋
为了解为何某些分子表现更佳,研究者采用了详细的计算机模拟。他们重点研究了CD73,因为该酶有高分辨率的三维结构可用。虚拟对接实验显示,活性化合物以一致的方式插入酶的催化口袋,吲哚环与芳香族氨基酸发生堆积相互作用,硫代半胱腙部分与关键残基形成氢键。结合能计算表明,紧密的疏水接触和范德华力是5n和5o强结合的主要贡献因素。每次持续半微秒的长分子动力学模拟表明,这些复合物保持稳定,蛋白与抑制剂位置随时间仅有小幅波动。
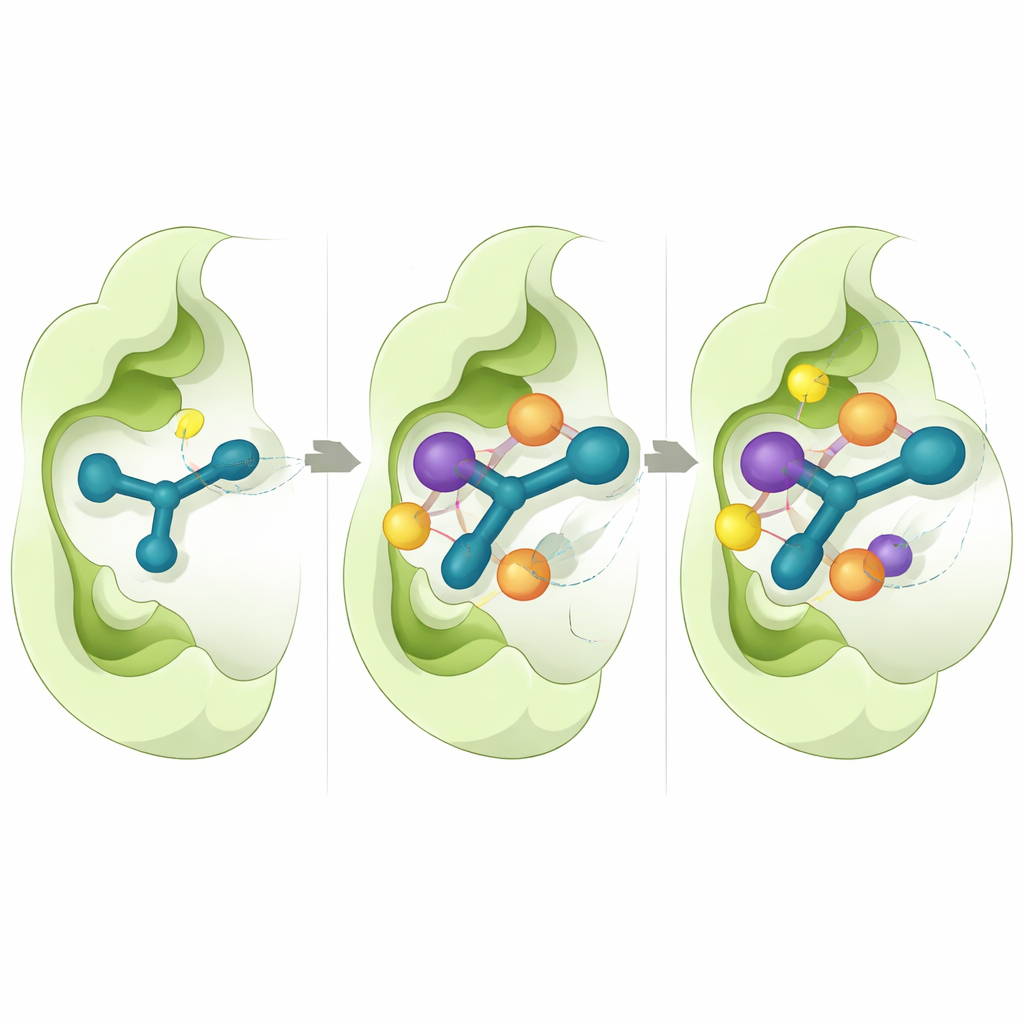
药物样行为的早期迹象
除了作用靶点外,潜在药物还必须在体内具有合适的转运和分布特性。因此,作者在计算中预测了吸收、分布及其他药代动力学属性。该系列大多数化合物,尤其是5n和5o,显示出尺寸、溶解性与膜通透性的有利平衡,预测具有良好的口服摄取性且仅有少量经验性规则的轻微违例。这些数据与它们强而选择性的酶抑制作用及模拟中稳定的结合相结合,支持将5n和5o视为进一步优化的起点,而非最终药物候选物。
这对患者可能意味着什么
当肿瘤利用CD39和CD73将周围环境充斥腺苷时,免疫细胞会变得迟缓、攻杀能力下降。本研究介绍了一组新的基于吲哚的分子,它们在体外选择性干扰该通路,并在计算模型中表现令人鼓舞。尽管仍需大量工作——包括细胞、动物乃至最终的人体试验——这些发现表明该化学骨架有望被改造为未来的药物,以帮助解除肿瘤对免疫系统施加的化学“刹车”,有可能提高现有癌症疗法的疗效。
引用: Batool, Z., Dutt, S.M., al-Rashida, M. et al. Synthesis, biological evaluation and molecular docking studies of N-propylsulfonyl indole-linked hydrazinecarbothioamides as selective ecto-5′-nucleotidase and NTPDase inhibitors. Sci Rep 16, 14419 (2026). https://doi.org/10.1038/s41598-026-50728-3
关键词: ecto-5-核苷酸酶 抑制, NTPD酶 抑制剂, 腺苷 信号传导, 癌症 免疫治疗, 吲哚 硫代半胱腙