Clear Sky Science · pl
Synteza, ocena biologiczna i badania dokowania molekularnego N-propylosulfonylowych indolowo‑powiązanych hydrazynokarbotiomamidów jako selektywnych inhibitorów ecto-5′-nukleotydazy i NTPDaz
Dlaczego te badania mają znaczenie dla przyszłych terapii przeciwnowotworowych
Nasz układ odpornościowy nieustannie patroluje w poszukiwaniu komórek nowotworowych, ale guzy wykształciły sprytne mechanizmy wyłączające te mechanizmy obronne. Jednym z takich zabiegów jest wykorzystanie przekaźników chemicznych powstających z ATP — tej samej cząsteczki, która napędza nasze komórki. W artykule opisano nową rodzinę małych cząsteczek zaprojektowanych do przerwania tego chemicznego triku, z długoterminowym celem umożliwienia układowi odpornościowemu lepszego rozpoznawania i atakowania guzów.
Chemiczny przełącznik, który usypia komórki odpornościowe
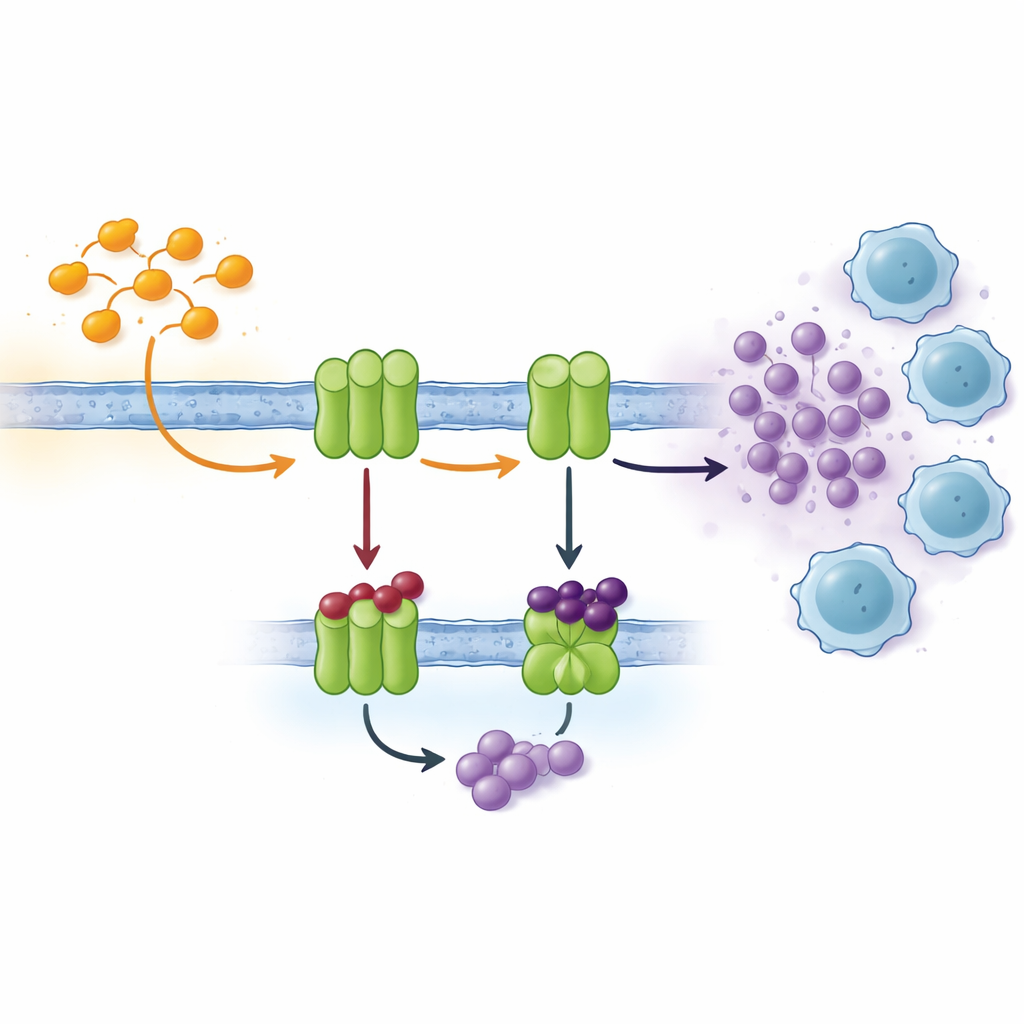
Komórki komunikują się wieloma sygnałami, a jednym z istotnych kanałów są nukleotydy takie jak ATP i jego produkt rozpadu, adenozyna. Na zewnątrz komórki łańcuch enzymów zakotwiczonych w błonie komórkowej stopniowo przekształca ATP w adenozynę. Dwoma kluczowymi graczami, znanymi jako CD39 i CD73, jest często nadmierna ekspresja w niedotlenionej tkance nowotworowej. Tam szybko przekształcają ATP uwolnione przez stresowane lub umierające komórki w adenozynę, która działa jak chemiczny „uspokajacz” wobec pobliskich komórek odpornościowych. Wysokie stężenia adenozyny tłumią aktywność limfocytów T, sprzyjają tworzeniu naczyń krwionośnych i ułatwiają rozsiewanie guza. Blokowanie enzymów tworzących adenozynę jest więc atrakcyjną strategią we współczesnej immunoterapii przeciwnowotworowej.
Projektowanie inteligentniejszych blokerów z użyciem sprawdzonego układu pierścieniowego
Projektanci leków często zaczynają od układów pierścieniowych, które już wykazały wartość medyczną. Pierścień indolowy, występujący w kilku zatwierdzonych lekach przeciwnowotworowych, jest takim elementem. Innym przydatnym składnikiem jest tiosemikarbazon, który może wiązać metale i silnie oddziałuje z wieloma celami biologicznymi. W tej pracy badacze połączyli te dwa motywy w jeden hybrydowy szkielet i dopracowali go, przyłączając różne grupy chemiczne, tworząc małą bibliotekę 22 powiązanych związków. Zmieniali miejsce przyłączenia jednostki tiosemikarbazonowej do pierścienia indolowego oraz modyfikowali grupy boczne, aby zobaczyć, jak te zmiany wpływają na zdolność blokowania CD73 i kilku pokrewnych enzymów zwanych NTPDazami.
Testowanie, które cząsteczki trafiają które enzymy
Zespół najpierw potwierdził strukturę i czystość wszystkich nowych cząsteczek przy użyciu standardowych technik laboratoryjnych, takich jak spektroskopia w podczerwieni i magnetycznego rezonansu jądrowego, spektrometria mas oraz wysokosprawna chromatografia cieczowa. Następnie zmierzyli, jak dobrze każdy związek spowalnia pracę pięciu ludzkich enzymów w testach probówkowych: CD73 oraz czterech typów NTPDaz (1, 2, 3 i 8). Kilka związków z serii blokowało swoje cele w niskich stężeniach mikromolowych, co oznacza, że były znacznie bardziej aktywne niż powszechnie stosowane inhibitory referencyjne. Różne chemiczne modyfikacje szkieletonu kierowały każdy związek ku określonym typom enzymów. Na przykład związek oznaczony jako 5f był szczególnie skuteczny wobec NTPDazy2 i NTPDazy8, podczas gdy 5i faworyzował NTPDazę1. Dwa spokrewnione związki, 5n i 5o, wyróżniały się silnym działaniem na CD73 i wybrane NTPDazy, co czyni je obiecującymi kandydatami wyjściowymi.
Zaglądanie do kieszeni wiążącej za pomocą komputera
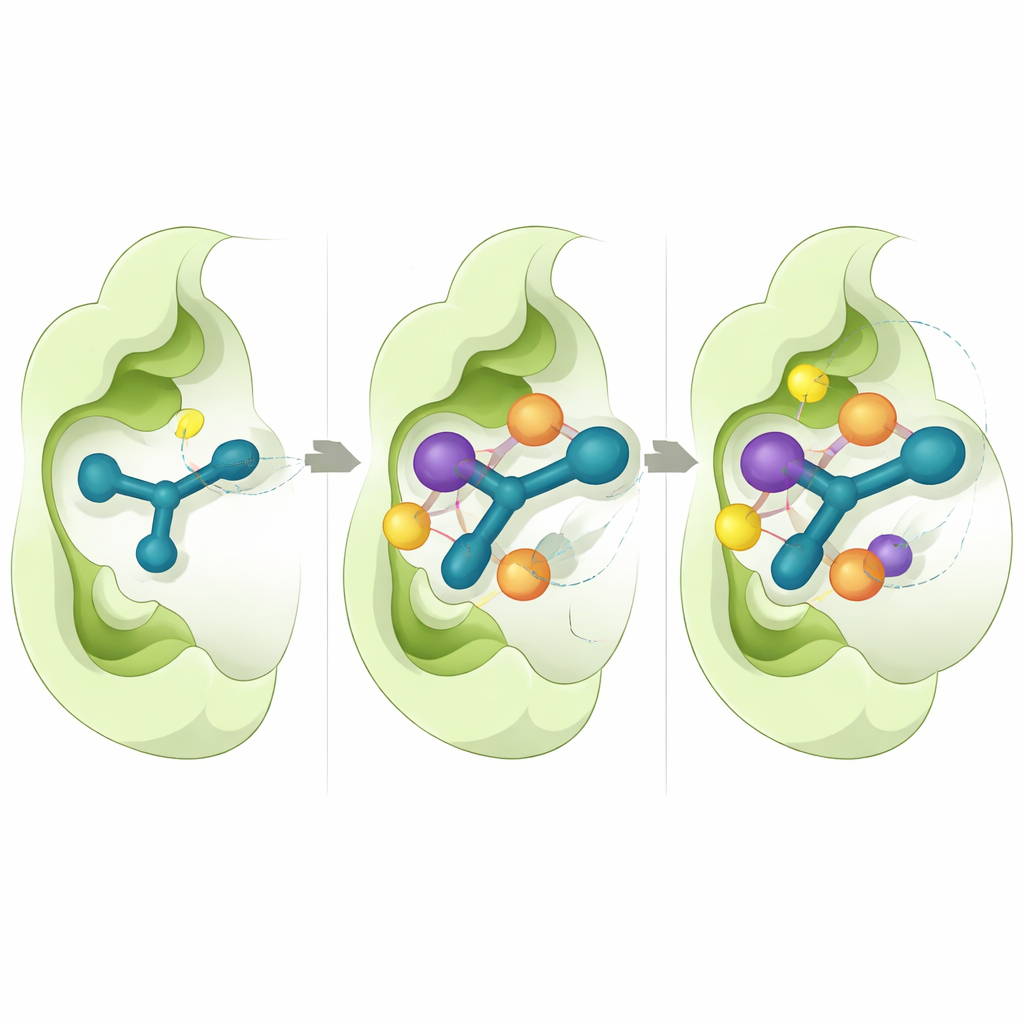
Aby zrozumieć, dlaczego niektóre cząsteczki działały lepiej od innych, badacze użyli szczegółowych symulacji komputerowych. Skoncentrowali się na CD73, ponieważ dostępna jest wysokorozdzielcza trójwymiarowa struktura tego enzymu. Wirtualne eksperymenty dokowania pokazały, że aktywne związki wsuwają się do kieszeni katalitycznej enzymu w spójny sposób, gdzie pierścień indolowy układa się w stos z aromatycznymi aminokwasami, a fragment tiosemikarbazonowy tworzy wiązania wodorowe z kluczowymi resztami. Obliczenia energii wiązania sugerowały, że ciasne kontakty hydrofobowe i siły van der Waalsa są głównymi czynnikami przyczyniającymi się do silnego wiązania obserwowanego dla 5n i 5o. Długie symulacje dynamiki molekularnej, każda śledząca ruch atomów przez pół mikrosekundy, wskazały, że kompleksy te pozostają stabilne, z jedynie niewielkimi fluktuacjami zarówno białka, jak i pozycji inhibitora w czasie.
Wczesne wskazówki dotyczące zachowania podobnego do leku
Ponad samym trafianiem w cele, potencjalne leki muszą poruszać się po organizmie w odpowiedni sposób. Autorzy przewidzieli więc in silico właściwości farmakokinetyczne, takie jak wchłanianie i dystrybucja. Większość związków z serii, a zwłaszcza 5n i 5o, wykazała korzystną równowagę wielkości, rozpuszczalności i przepuszczalności błonowej, z dobrym przewidywanym wchłanianiem doustnym i tylko niewielkimi naruszeniami prostych reguł farmakopealnych. Te dane, połączone z ich silną i selektywną inhibicją enzymów oraz stabilnym wiązaniem w symulacjach, wspierają traktowanie 5n i 5o jako punktów wyjściowych do dalszej optymalizacji, a nie jako gotowych kandydatów na leki.
Co to może znaczyć dla pacjentów
Kiedy guzy wykorzystują CD39 i CD73 do zalania swojego otoczenia adenozyną, komórki odpornościowe stają się ospałe i mniej zdolne do ataku. Badanie przedstawia nowy zestaw związków opartych na indolu, które selektywnie zakłócają tę ścieżkę w testach probówkowych i zachowują się obiecująco w modelach komputerowych. Choć przed nami wiele pracy — w tym testy w komórkach, modelach zwierzęcych i ostatecznie u ludzi — wyniki sugerują, że ten szkielet chemiczny może zostać ukształtowany w przyszłe leki pomagające zdjąć chemiczne „hamulce”, jakie guzy nakładają na układ odpornościowy, potencjalnie zwiększając skuteczność istniejących terapii przeciwnowotworowych.
Cytowanie: Batool, Z., Dutt, S.M., al-Rashida, M. et al. Synthesis, biological evaluation and molecular docking studies of N-propylsulfonyl indole-linked hydrazinecarbothioamides as selective ecto-5′-nucleotidase and NTPDase inhibitors. Sci Rep 16, 14419 (2026). https://doi.org/10.1038/s41598-026-50728-3
Słowa kluczowe: inhibicja ecto-5-nukleotydazy, inhibitory NTPDaz, sygnalizacja adenozynowa, immunoterapia przeciwnowotworowa, indolowe tiosemikarbazony