Clear Sky Science · he
סינתזה, הערכה ביולוגית ולימודי הדוקינג מולקולרי של N‑פרופילסולפוניל אינדול‑קשור הידראזינקרבוטיואמידים כמעכבים סלקטיביים של ecto‑5′‑nucleotidase ו‑NTPDase
מדוע מחקר זה חשוב לטיפולים עתידיים בסרטן
מערכת החיסון שלנו סורקת כל העת אחר תאים סרטניים, אבל הגידולים פיתחו טריקים חכמים כדי לכבות את ההגנות הללו. אחד הטריקים משתמש במתווכים כימיים שמקורם ב‑ATP, המולקולה שמזינה את התאים שלנו. מאמר זה מתאר משפחה חדשה של מולקולות זעירות שמטרתן לקטוע את הטריק הכימי הזה, במטרה ארוכת‑טווח לסייע למערכת החיסון לזהות ולהתקיף טוב יותר גידולים.
המתג הכימי שמרגיע תאי חיסון
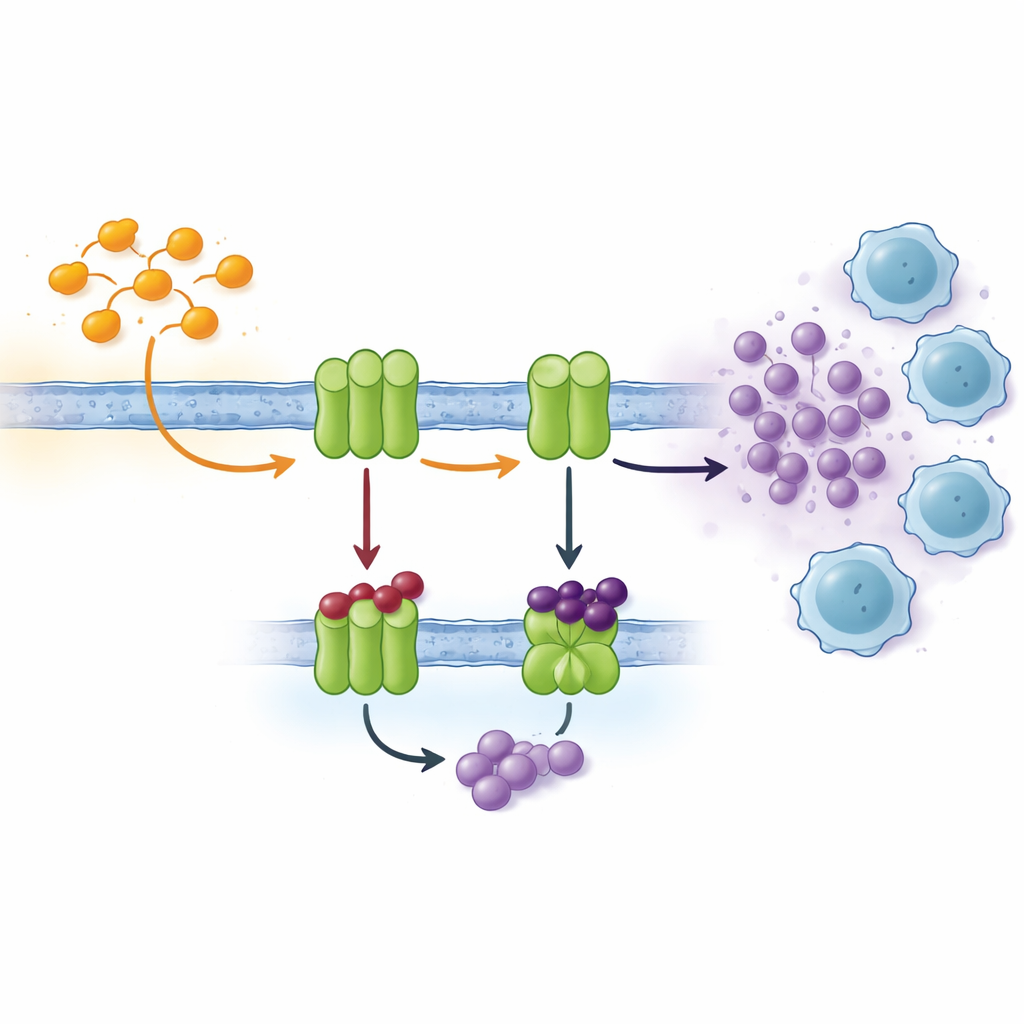
תאים מתקשרים באמצעות שורה ארוכה של אותות, ואחד הערוצים החשובים מבוסס על נוקלאוטידים כמו ATP ומוצר השבר שלו, אדנוזין. מחוץ לתא, שרשרת אנזימים הממוקמת בממברנת התא ממירה בהדרגה ATP לאדנוזין. שני שחקנים מרכזיים, המכונים CD39 ו‑CD73, מיוצרים לעתים יתר ברקמות סרטניות עניות חמצן. שם הם מהירים בהמרת ATP שמשתחרר מתאים מותשים או מתים לאדנוזין, שפועל כמו "מרגיע" כימי על תאי החיסון הסמוכים. רמות גבוהות של אדנוזין מרככות פעילות תאי T, מקדמות יצירת כלי דם ועוזרות להפצת הגידול. חסימת האנזימים שיוצרים אדנוזין היא אפוא אסטרטגיה אטרקטיבית באימונותרפיה מודרנית של סרטן.
עיצוב מעכבים חכמים באמצעות ליבת טבעת מוכחת
מעצבי תרופות מתחילים לעתים קרובות ממערכות טבעת שהראו כבר ערך רפואי. טבעת האינדול, שנמצאת בכמה תרופות נגד סרטן מאושרות, היא אחת מהמבנים הללו. מרכיב שימושי נוסף, תיוסמי‑קארבזון, יכול לקשור מתכות ומתקשר בעוצמה עם מטרות ביולוגיות רבות. בעבודה זו החוקרים שילבו את שני המוטיבים האלה לתבנית היברידית אחת וכיוונו אותה באמצעות הצמדת קבוצות כימיות שונות, ובנו ספריה קטנה של 22 תרכובות קרובות. הם שינו את המיקום של יחידת התיוסמי‑קארבזון על טבעת האינדול וגיוונו את קבוצות הצד המצורפות כדי לבדוק כיצד שינויים אלה משפיעים על היכולת לעכב את CD73 ומספר אנזימים קשורים שנקראים NTPDases.
בדיקה אילו מולקולות פוגעות באיזה אנזים
הצוות אישר תחילה את המבנה והטיוליות של כל המולקולות החדשות בעזרת טכניקות מעבדה סטנדרטיות כגון ספקטרוסקופיית אינפרא‑אדום וגרעין‑מגנטי (NMR), ספקטרומטריית מסה וגז כרומטוגרפיה נוזלית ביצועים גבוהים. לאחר מכן מדדו עד כמה כל תרכובת האטה חמישה אנזימים אנושיים במבחנות: CD73 וארבעה סוגי NTPDase (1, 2, 3 ו‑8). כמה חברים בסדרה עיכבו את מטרותיהם בריכוזים מיקרומולריים נמוכים, כלומר היו בעלי עוצמה רבה יותר ממעכבים ייחוס נפוצים. קישוטים כימיים שונים על התבנית הנחו כל תרכובת לכיוון סוגי אנזים מסוימים. למשל, מולקולה מסומנת 5f הייתה יעילה במיוחד נגד NTPDase2 ו‑NTPDase8, בעוד 5i נטתה ל‑NTPDase1. שתי מולקולות קשורות, 5n ו‑5o, בלטו בפעילות החזקה שלהן על CD73 ועל NTPDases נבחרים, מה שמציין אותן כמועמדות מובילות ומבטיחות במיוחד.
התבוננות לכיס הקשירה על מחשב
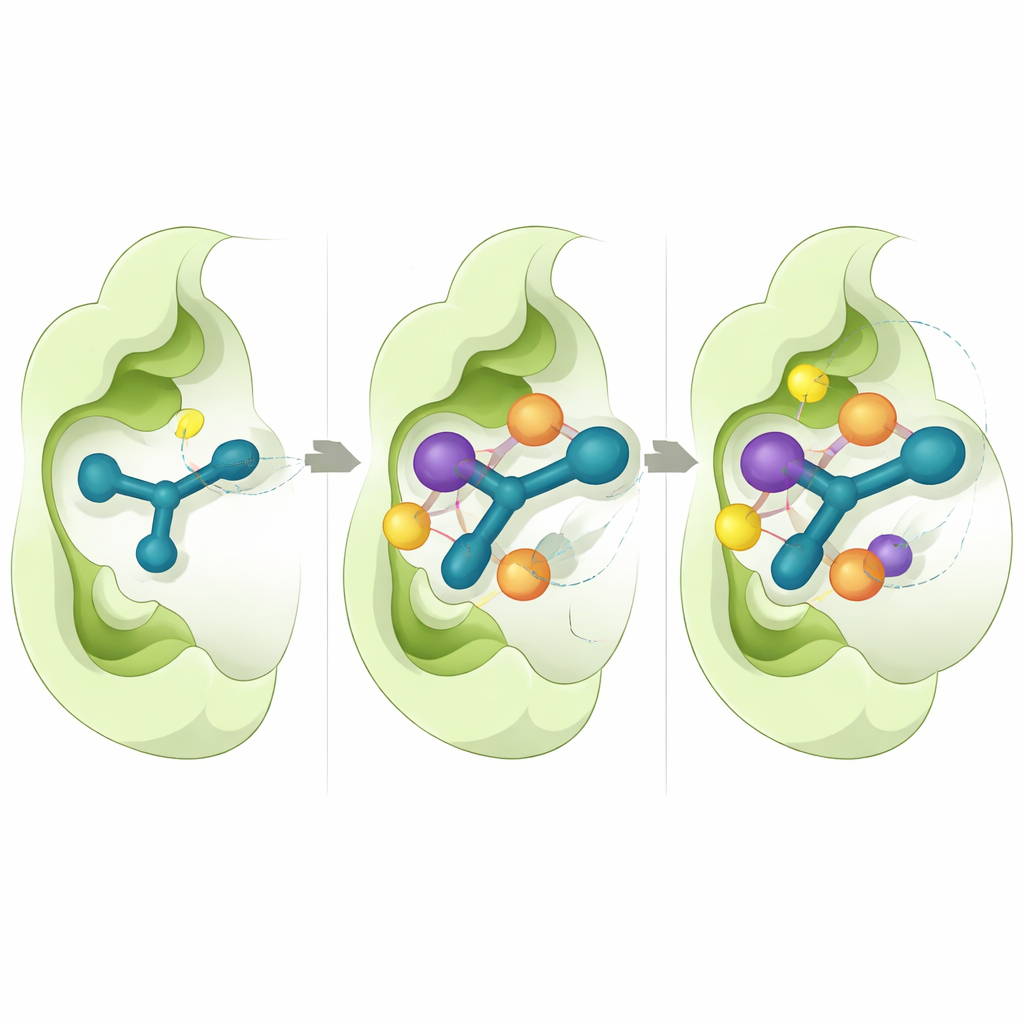
כדי להבין מדוע חלק מהמולקולות עבדו טוב יותר מאחרות, החוקרים השתמשו בסימולציות ממוחשבות מפורטות. הם התרכזו ב‑CD73, מאחר שמבנה תלת‑ממדי ברזולוציה גבוהה של האנזים זמין. ניסויי דוקינג וירטואליים הראו שהתרכובות הפעילות מתיישבות בכיס הקטליטי של האנזים בצורה עקבית, כאשר טבעת האינדול מתסננת אל מול חומצות אמינו ארומטיות וקטע התיוסמי‑קארבזון יוצר קשרי מימן עם שרשראות מפתח. חישובי אנרגיית קשירה הצביעו על כך כי מגעים הידרופוביים הדוקים וכוחות ואן‑דר‑וולס הם תורמים מרכזיים לקשירה החזקה שנצפתה ב‑5n ו‑5o. סימולציות דינמיקת מולקולות ארוכות, שכל אחת הריצה את תנועת האטומים למשך חצי מיקרו‑שנייה, הצביעו על כך שמורכבים אלה נשארים יציבים, עם תנודות קטנות בלבד הן בחלבון והן במיקומי המעכב לאורך הזמן.
רמזים ראשוניים להתנהגות בדומה לתרופה
מעבר ליכולת לעכב את המטרות, תרופות פוטנציאליות צריכות לנוע בגוף באופן מתאים. לכן המחברים חזו תכונות ספיגה, התפוצה ותכונות פרמקוקינטיות נוספות בחישוב. רוב התרכובות בסדרה, ובמיוחד 5n ו‑5o, הראו איזון חיובי של גודל, מסיסות וחלחול ממברנית, עם ספיגה אורלית חזויה טובה ולהפרות כללים קלות בלבד. נתונים אלה, בשילוב עם עיכוב חזק וסלקטיבי של אנזימים וקשירה יציבה בסימולציות, תומכים בהתייחסות ל‑5n ו‑5o כנקודות התחלה לאופטימיזציה נוספת ולא כמועמדות תרופתיות גמורות.
מה זה עשוי להצביע עבור מטופלים
כשגידולים משתמשים ב‑CD39 ו‑CD73 להצפת סביבתם באדנוזין, תאי החיסון נעשים מנומנמים ופחות מסוגלים לתקוף. המחקר מציג מערך חדש של מולקולות מבוססות אינדול שמתערבות סלקטיבית בדרך זו במבחנה ומתנהגות בעידוד במודלים ממוחשבים. בעוד שנותר עוד עבודה רבה — כולל בדיקות בתאים, בבעלי חיים ולבסוף בבני אדם — הממצאים מרמזים כי תבנית כימית זו ניתנת לעיצוב לתרופות עתידיות שעשויות להסיר את "הבלמים" הכימיים שהגידולים מפעילים על המערכת החיסונית, ובכך לשפר פוטנציאלית את היעילות של טיפולי סרטן קיימים.
ציטוט: Batool, Z., Dutt, S.M., al-Rashida, M. et al. Synthesis, biological evaluation and molecular docking studies of N-propylsulfonyl indole-linked hydrazinecarbothioamides as selective ecto-5′-nucleotidase and NTPDase inhibitors. Sci Rep 16, 14419 (2026). https://doi.org/10.1038/s41598-026-50728-3
מילות מפתח: עיכוב ecto‑5‑נוקלאוטידאז, מעכבי NTPDase, אותות אדנוזין, אימונותרפיה של סרטן, אינדול תיוסמי‑קארבזונים