Clear Sky Science · ru
Синтез, биологическая оценка и молекулярное докирование N-пропилсульфонил-индол-связанных гидразинокарботиоамидов как селективных ингибиторов эпто-5′-нуклеотидазы и NTPDase
Почему это исследование важно для будущего лечения рака
Наша иммунная система постоянно контролирует наличие раковых клеток, но опухоли выработали изощрённые механизмы, чтобы подавлять эти защиты. Одна из таких стратегий использует химические сигналы, образуемые из АТФ — той же молекулы, которая снабжает энергией клетки. В этой статье описана новая семья малых молекул, разработанных для вмешательства в этот химический приём, с долгосрочной целью помочь иммунной системе лучше распознавать и атаковать опухоли.
Химический переключатель, усыпляющий иммунные клетки
Клетки общаются между собой с помощью множества сигналов, и одним из важных каналов являются нуклеотиды, такие как АТФ, и его продукт распада — аденозин. Снаружи клетки цепочка ферментов, находящихся в мембране, непрерывно превращает АТФ в аденозин. Два ключевых игрока, известные как CD39 и CD73, часто избыточно экспрессируются в тканях опухолей с дефицитом кислорода. Там они быстро превращают АТФ, выделяемый стрессовыми или умирающими клетками, в аденозин, который действует как химический «транквилизатор» для соседних иммунных клеток. Повышенные уровни аденозина подавляют активность Т‑клеток, способствуют росту сосудов и помогают распространению опухоли. Блокирование ферментов, создающих аденозин, поэтому выглядит привлекательной стратегией современной иммунотерапии рака.
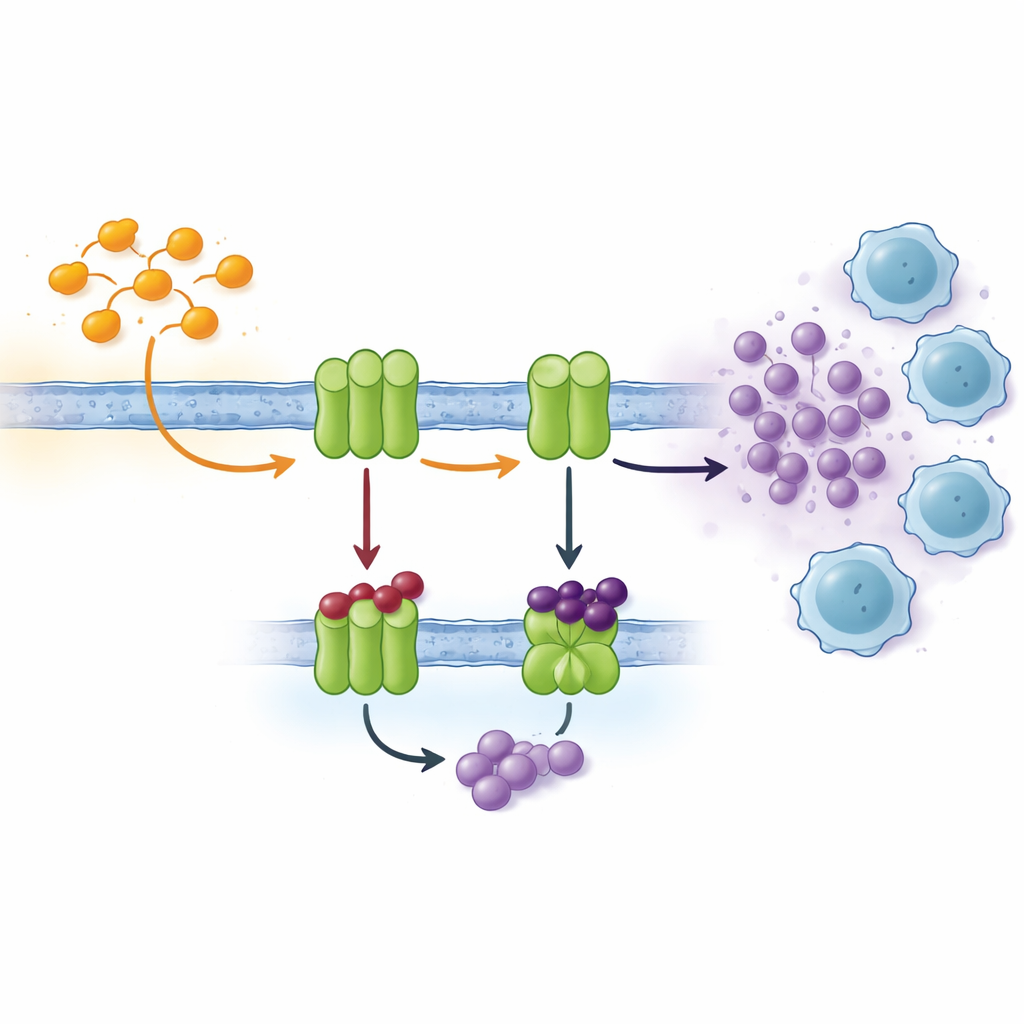
Проектирование более умных блокаторов на базе проверенного кольца
Дизайнеры лекарств часто начинают с циклических систем, которые уже показали медицинскую ценность. Индольное кольцо, присутствующее в нескольких одобренных противораковых препаратах, — одна из таких структур. Другой полезный компонент — тиосемикарбазон — способен координировать металлы и активно взаимодействует со множеством биологических мишеней. В этой работе исследователи объединили оба мотива в единый гибридный каркас и тонко настроили его, присоединяя различные химические группы, создав небольшую библиотеку из 22 родственных соединений. Они варьировали положение тиосемикарбазоновой единицы на индольном кольце и изменяли присоединённые заместители, чтобы оценить, как эти изменения влияют на способность блокировать CD73 и несколько родственных ферментов — NTPDase.
Тестирование, какие молекулы действуют на какие ферменты
Команда сначала подтвердила структуру и чистоту всех новых молекул с помощью стандартных лабораторных методов, таких как ИК‑ и ЯМР‑спектроскопия, масс‑спектрометрия и ВЭЖХ. Затем они измеряли, насколько каждая молекула замедляет работу пяти человеческих ферментов в тест‑трубных анализах: CD73 и четырёх типов NTPDase (1, 2, 3 и 8). Несколько членов серии подавляли свои мишени в низком микромолярном диапазоне, что означает существенно большую активность по сравнению с обычно используемыми референтными ингибиторами. Разные химические «украшения» на каркасе направляли каждое соединение к определённым типам ферментов. Например, молекула под маркировкой 5f оказалась особенно эффективной против NTPDase2 и NTPDase8, тогда как 5i предпочитала NTPDase1. Два родственных соединения, 5n и 5o, выделялись сильным действием на CD73 и выбранные NTPDase, что делает их особенно перспективными кандидатами в лид‑соединения.
Заглядывая в посадочное карман на компьютере
Чтобы понять, почему некоторые молекулы работали лучше других, исследователи использовали подробные компьютерные симуляции. Они сосредоточились на CD73, поскольку доступна высоко‑разрешающая трёхмерная структура этого фермента. Виртуальные докинг‑эксперименты показали, что активные соединения встраиваются в каталитический карман фермента единообразно: индольное кольцо располагается в штабеле рядом с ароматическими аминокислотами, а тиосемикарбазоновый фрагмент образует водородные связи с ключевыми остатками. Расчёты энергии связывания указывают, что плотные гидрофобные контакты и ван‑дер‑ваальсовы силы являются главными вкладчиками в сильное связывание, наблюдаемое для 5n и 5o. Длительные молекулярно‑динамические симуляции, каждая из которых моделировала движение атомов в течение полумикросекунды, показали, что эти комплексы остаются стабильными, с незначительными флуктуациями как в белке, так и в положении ингибитора с течением времени.
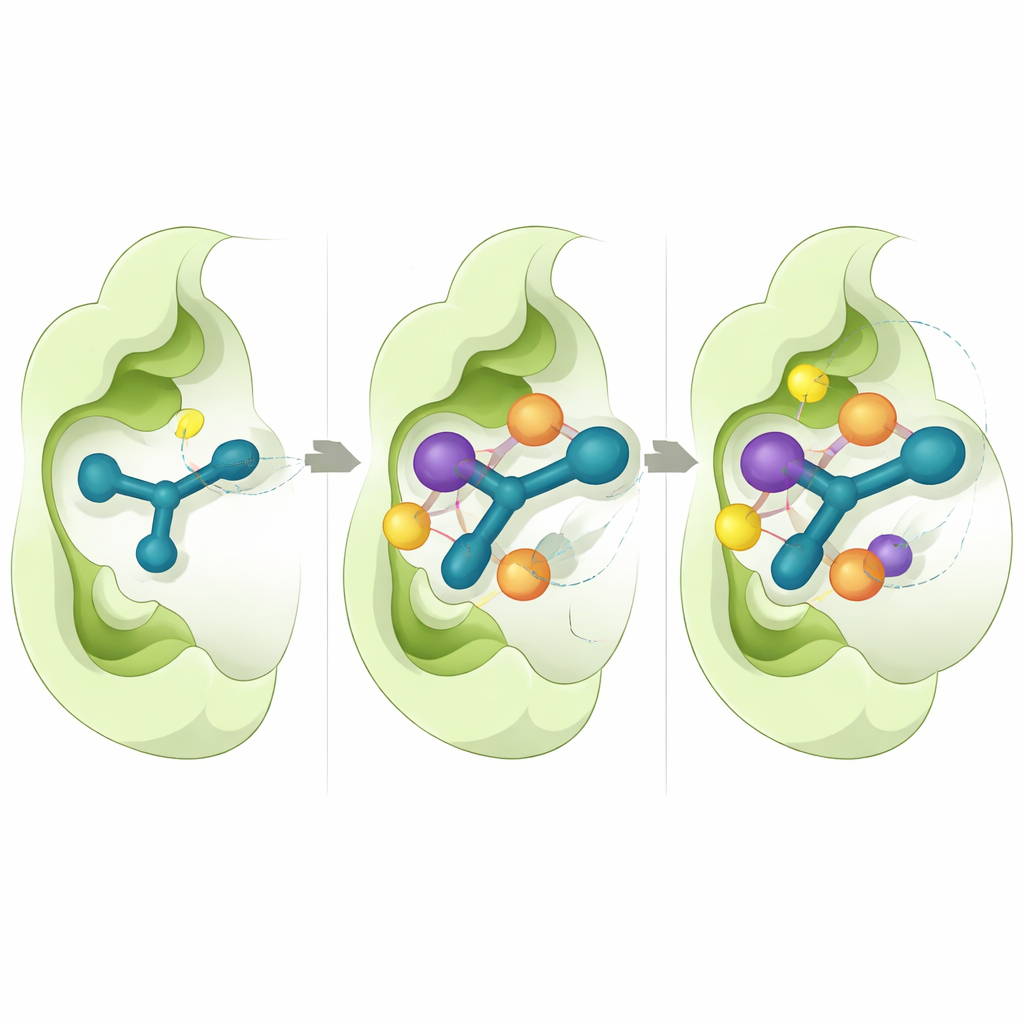
Ранние признаки лекароподобного поведения
Помимо воздействия на мишени, потенциальные лекарства должны подходящим образом перемещаться по организму. Авторы поэтому предсказали абсорбцию, распределение и другие фармакокинетические свойства in silico. Большинство соединений серии, особенно 5n и 5o, показали благоприятный баланс размера, растворимости и проницаемости мембраны, с хорошим прогнозируемым пероральным всасыванием и лишь незначительными нарушениями эмпирических правил. Эти данные в сочетании с их сильным и селективным ингибированием ферментов и устойчивым связыванием в симуляциях поддерживают взгляд на 5n и 5o как на отправные точки для дальнейшей оптимизации, а не как на завершённые лекарственные кандидаты.
Что это может означать для пациентов
Когда опухоли используют CD39 и CD73, чтобы залить своё окружение аденозином, иммунные клетки замедляются и хуже справляются с атакой. Это исследование представляет новый набор индо́л‑основанных молекул, которые избирательно вмешиваются в этот путь в тест‑трубных экспериментах и демонстрируют обнадёживающее поведение в компьютерных моделях. Несмотря на то что предстоит ещё значительная работа — включая тесты в клетках, на животных и, в конечном счёте, на людях — полученные результаты указывают, что этот химический каркас может быть преобразован в будущие лекарства, помогающие снять химические «тормоза», которые опухоли накладывают на иммунную систему, и потенциально повышать эффективность существующих противораковых терапий.
Цитирование: Batool, Z., Dutt, S.M., al-Rashida, M. et al. Synthesis, biological evaluation and molecular docking studies of N-propylsulfonyl indole-linked hydrazinecarbothioamides as selective ecto-5′-nucleotidase and NTPDase inhibitors. Sci Rep 16, 14419 (2026). https://doi.org/10.1038/s41598-026-50728-3
Ключевые слова: ингибирование эпто-5-нуклеотидазы, ингибиторы NTPDase, аденозиновая сигнализация, иммунотерапия рака, индо́ловые тиосемикарбазоны