Clear Sky Science · sv
Syntes, biologisk utvärdering och molekylär dockningsstudier av N-propylsulfonyl indol-länkade hydrazincarbothioamider som selektiva hämmare av ecto-5′-nukleotidas och NTPDaser
Varför denna forskning är viktig för framtida cancerbehandlingar
Vårt immunsystem patrullerar ständigt efter cancerceller, men tumörer har utvecklat listiga strategier för att stänga av dessa försvar. En av dessa strategier använder kemiska budbärare härledda från ATP, samma molekyl som driver våra celler. Denna artikel beskriver en ny familj av små molekyler utformade för att störa denna kemiska strategi, med det långsiktiga målet att hjälpa immunsystemet att bättre känna igen och angripa tumörer.
Den kemiska brytaren som lugnar immunceller
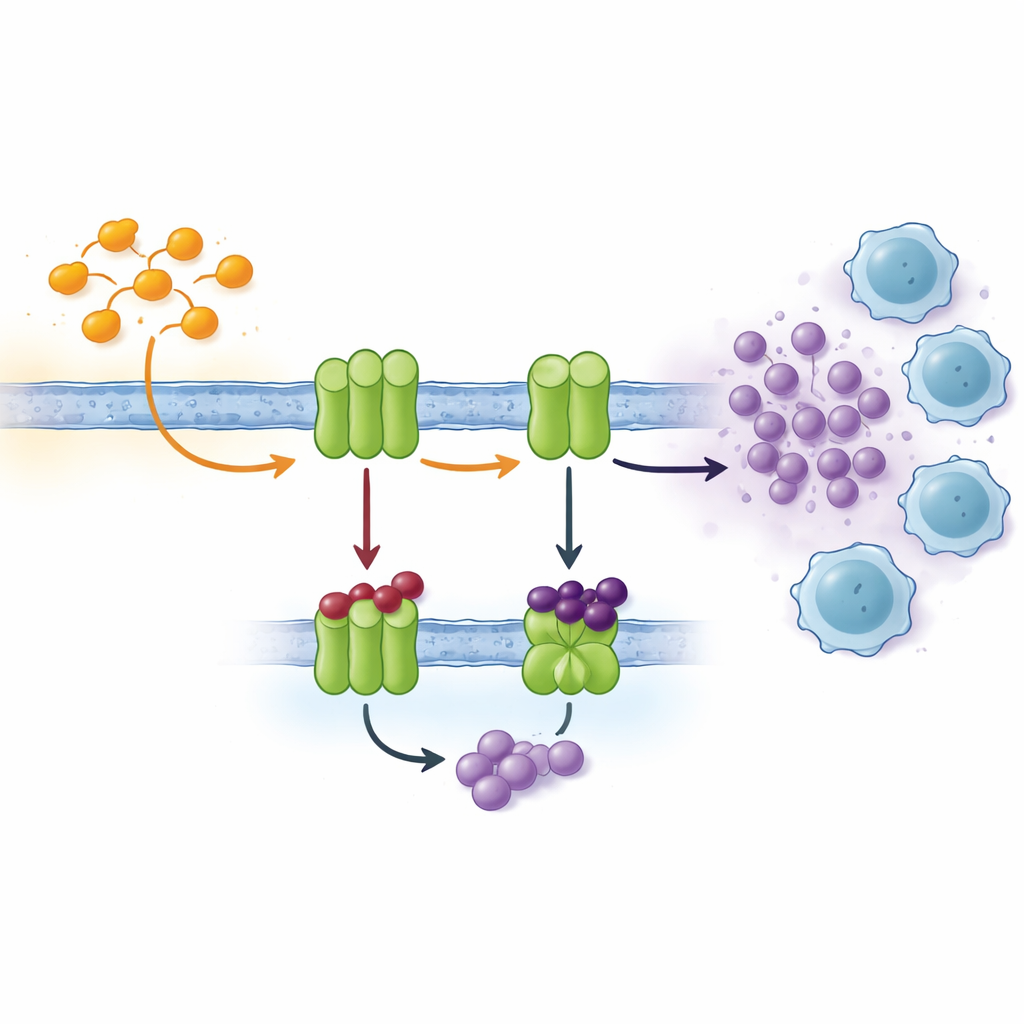
Celler kommunicerar med varandra via många signaler, och en viktig kanal bygger på nukleotider såsom ATP och dess nedbrytningsprodukt adenosin. Utanför cellen omvandlar en kedja av enzymer i cellmembranet kontinuerligt ATP till adenosin. Två nyckelspelare, kända som CD39 och CD73, överproduceras ofta i syrefattig tumörvävnad. Där omvandlar de snabbt ATP som frisätts av stressade eller döende celler till adenosin, vilket fungerar som ett kemiskt ”lugnande medel” på närliggande immunceller. Höga adenosinnivåer dämpar T‑cellsaktivitet, främjar blodkärlsbildning och underlättar tumörspridning. Att blockera enzymerna som skapar adenosin är därför en attraktiv strategi inom modern cancerimmunoterapi.
Att designa smartare blockare med ett beprövat ringsystem
Läkemedelsutvecklare börjar ofta från ringsystem som redan visat medicinskt värde. Indolringen, som finns i flera godkända cancerläkemedel, är en sådan struktur. En annan användbar komponent, thiosemicarbazon, kan binda metaller och interagerar starkt med många biologiska mål. I detta arbete kombinerade forskarna dessa två motiv i ett enda hybrid‑scaffold och finslipade det genom att fästa olika kemiska grupper, vilket skapade ett litet bibliotek med 22 besläktade föreningar. De varierade var på indolringen thiosemicarbazon‑enheten sitter och ändrade sidogrupperna för att se hur dessa förändringar påverkade förmågan att blockera CD73 och flera relaterade enzymer kallade NTPDaser.
Testning av vilka molekyler som påverkar vilka enzymer
Teamet bekräftade först struktur och renhet hos alla nya molekyler med standardlaboratorietekniker som infraröd och nukleär magnetresonansspektroskopi, massespektrometri och högupplöst vätskekromatografi. De mätte sedan hur väl varje förening saktade ner fem humana enzymer i provrörsassayer: CD73 och fyra NTPDase‑typer (1, 2, 3 och 8). Flera medlemmar i serien hämmade sina mål vid låga mikromolära koncentrationer, vilket innebär att de var betydligt mer potenta än vanliga referenshämmare. Olika kemiska dekorationer på scaffoldet styrde varje förening mot specifika enzymtyper. Till exempel var en molekyl betecknad 5f särskilt effektiv mot NTPDase2 och NTPDase8, medan 5i favoriserade NTPDase1. Två besläktade molekyler, 5n och 5o, utmärkte sig genom sin starka aktivitet mot CD73 och utvalda NTPDaser, vilket gör dem särskilt lovande som ledande kandidater.
Inblick i bindningsfickan med datorhjälp
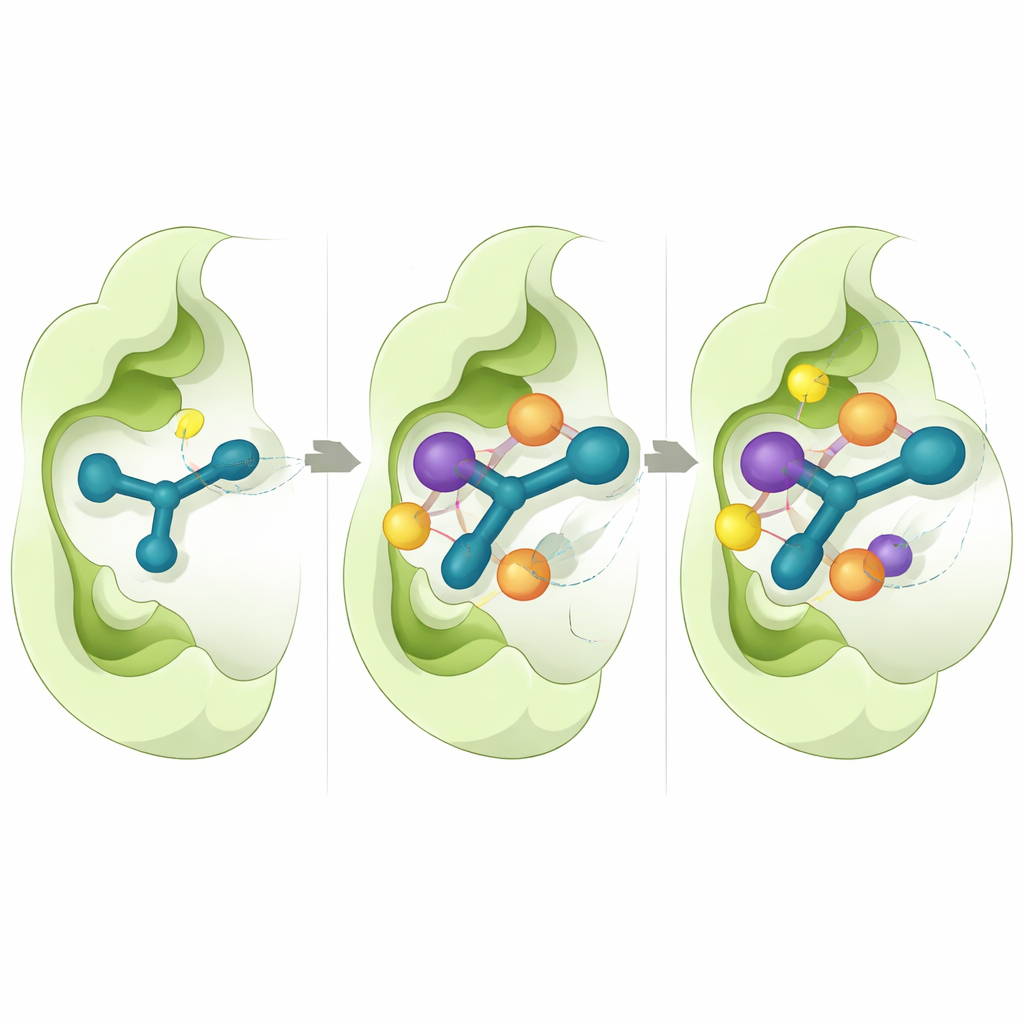
För att förstå varför vissa molekyler fungerade bättre än andra använde forskarna detaljerade datorsimuleringar. De fokuserade på CD73 eftersom en högupplöst tredimensionell struktur av detta enzym finns tillgänglig. Virtuella dockningsexperiment visade att de aktiva föreningarna glider in i enzymets katalytiska ficka på ett konsekvent sätt, där indolringen staplas mot aromatiska aminosyror och thiosemicarbazon‑segmentet bildar vätebindningar med nyckelrester. Beräkningar av bindningsenergi antydde att täta hydrofoba kontakter och van der Waals‑krafter är stora bidragsgivare till den starka bindningen som observerades för 5n och 5o. Långa molekylärdynamiska simuleringar, där atomrörelser följdes över en halv mikrosekund, indikerade att dessa komplex förblir stabila med endast små fluktuationer i både proteinet och inhibitorns positioner över tiden.
Tidiga tecken på läkemedelselikt beteende
Utöver att påverka sina mål måste potentiella läkemedel röra sig i kroppen på ett lämpligt sätt. Författarna predikterade därför absorption, distribution och andra farmakokinetiska egenskaper in silico. Majoriteten av föreningarna i serien, särskilt 5n och 5o, visade en gynnsam balans av storlek, löslighet och membranpermeabilitet, med god förväntad oral upptagning och bara mindre avvikelser från tumregler. Dessa data, tillsammans med deras starka och selektiva enzymhämning och stabila bindning i simuleringar, stödjer att betrakta 5n och 5o som startpunkter för vidare optimering snarare än färdiga läkemedelskandidater.
Vad detta kan innebära för patienter
När tumörer använder CD39 och CD73 för att översvämma sin omgivning med adenosin blir immunceller slöa och mindre kapabla att angripa. Denna studie introducerar en ny uppsättning indol‑baserade molekyler som selektivt stör denna väg i provrör och uppvisar lovande beteende i datormodeller. Mycket arbete återstår — inklusive tester i celler, djur och så småningom människor — men resultaten tyder på att detta kemiska scaffold kan formas till framtida läkemedel som hjälper till att lyfta de kemiska ”bromsar” tumörer placerar på immunsystemet, vilket potentiellt kan göra befintliga cancerbehandlingar mer effektiva.
Citering: Batool, Z., Dutt, S.M., al-Rashida, M. et al. Synthesis, biological evaluation and molecular docking studies of N-propylsulfonyl indole-linked hydrazinecarbothioamides as selective ecto-5′-nucleotidase and NTPDase inhibitors. Sci Rep 16, 14419 (2026). https://doi.org/10.1038/s41598-026-50728-3
Nyckelord: hämmning av ecto-5-nukleotidas, NTPDase-hämmare, adenosinsignalering, cancerimmunterapi, indol-thiosemicarbazoner